硫酸生产中炉气转化反应为:2SO2(g)+O2(g) 2SO3(g)。研究发现,SO3的体积分数(SO3%)随温度(T)的变化如曲线Ⅰ所示。下列判断正确的是
2SO3(g)。研究发现,SO3的体积分数(SO3%)随温度(T)的变化如曲线Ⅰ所示。下列判断正确的是
 2SO3(g)。研究发现,SO3的体积分数(SO3%)随温度(T)的变化如曲线Ⅰ所示。下列判断正确的是
2SO3(g)。研究发现,SO3的体积分数(SO3%)随温度(T)的变化如曲线Ⅰ所示。下列判断正确的是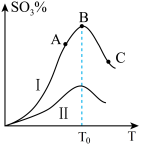
| A.该反应的正反应为放热反应 |
| B.曲线Ⅰ上A、C两点反应速率的关系是:vA>vC |
| C.反应达到B点时,2v正(O2)= v逆(SO3) |
| D.已知V2O5的催化效果比Fe2O3好,若Ⅰ表示用V2O5作催化剂的曲线,则Ⅱ可表示为Fe2O3作催化剂的曲线 |
更新时间:2019-10-26 10:13:24
|
相似题推荐
多选题
|
适中
(0.65)
名校
【推荐1】关于合成氨工业:N2(g)+3H2(g)⇌2NH3(g);ΔH=-akJ/mol(a>0)下列说法正确的是
| A.1molN2和3molH2的总键能大于2molNH3的总键能 |
| B.使用铁触媒作为催化剂对ΔH值的大小无影响 |
| C.用水吸收NH3后,剩余N2和H2循环利用提高原料利用率 |
| D.反应采用高温条件,可以用勒夏特列原理解释 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】Cu—Ce—Ox固溶体作为金属催化剂,能有效促进电化学还原,反应产生CH4和C2H4的共同中间体*CO在催化剂表面的反应机理如图所示。下列说法错误的是
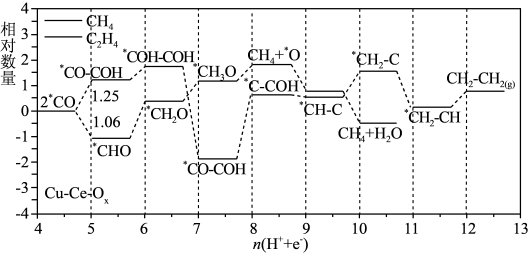

| A.Cu—Ce—Ox固溶体催化剂对生成CH4有较高选择性 |
| B.制约CO2还原为C2H4反应速率的是*COH—COH→*CH—COH |
| C.由*CO生成*OH的反应为*CO+5H++5e-=CH4+*OH |
| D.*CH2O→*CH3O只有化学键的形成 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐3】我国科学家发现了一种新型的CO2电化学还原催化剂——二维锑片(Sb),在酸性条件下人工固碳装置中反应物在二维锑片表面催化竞争反应,生成产物甲酸、一氧化碳的反应历程如图所示(图中吸附在催化剂表面的中间活性产物全部为电中性,用*标注)。下列叙述正确的是
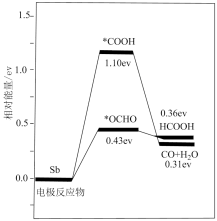

| A.产物CO+H2O能量最低,所以该反应最易进行 |
| B.该电极表面生成CO的反应为:*CO2+H2O+2e-=CO+2OH- |
| C.酸性条件下,生成甲酸的决速步骤反应为:*CO2+H++e-=*OCHO |
| D.该催化剂对两个反应的选择性效果为:甲酸>一氧化碳 |
您最近一年使用:0次
【推荐1】某温度下,将2molH2和2molI2充入密闭的刚性容器中发生反应H2(g)+I2(g) 2HI(g),该反应的v-t图像如图所示,t1时刻测定容器内HI的物质的量为1mol,t2时刻保持等温等容,抽走0.5molHI。下列有关叙述不正确的是
2HI(g),该反应的v-t图像如图所示,t1时刻测定容器内HI的物质的量为1mol,t2时刻保持等温等容,抽走0.5molHI。下列有关叙述不正确的是
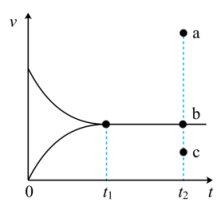
 2HI(g),该反应的v-t图像如图所示,t1时刻测定容器内HI的物质的量为1mol,t2时刻保持等温等容,抽走0.5molHI。下列有关叙述不正确的是
2HI(g),该反应的v-t图像如图所示,t1时刻测定容器内HI的物质的量为1mol,t2时刻保持等温等容,抽走0.5molHI。下列有关叙述不正确的是
A.该温度下2HI(g) H2(g)+I2(g)的平衡常数K=2.25 H2(g)+I2(g)的平衡常数K=2.25 |
| B.反应过程中,可以利用气体的平均摩尔质量保持不变来判断是否达到平衡 |
| C.t2时刻,抽取HI的瞬间,v′(逆)在图像上的变化应该是a点 |
| D.t2时刻,抽取HI后再次达到平衡后H2的百分含量不变 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐2】甲烷制取氢气的反应方程式为CH4(g)+H2O(g) CO(g)+3H2(g),在三个容积均为1 L的恒温恒容密闭容器中,按表中起始数据投料(忽略副反应)。甲烷的平衡转化率与温度、压强的关系如下图所示。
CO(g)+3H2(g),在三个容积均为1 L的恒温恒容密闭容器中,按表中起始数据投料(忽略副反应)。甲烷的平衡转化率与温度、压强的关系如下图所示。
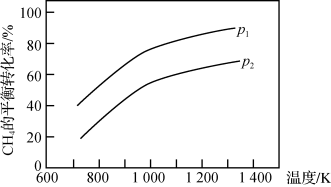
下列说法正确的是
 CO(g)+3H2(g),在三个容积均为1 L的恒温恒容密闭容器中,按表中起始数据投料(忽略副反应)。甲烷的平衡转化率与温度、压强的关系如下图所示。
CO(g)+3H2(g),在三个容积均为1 L的恒温恒容密闭容器中,按表中起始数据投料(忽略副反应)。甲烷的平衡转化率与温度、压强的关系如下图所示。| 容器 | 起始物质的量/mol | CH4的平衡转化率 | |||
| CH4 | H2O | CO | H2 | ||
| Ⅰ | 0.1 | 0.1 | 0 | 0 | 50% |
| Ⅱ | 0.1 | 0.1 | 0.1 | 0.3 | / |
| Ⅲ | 0 | 0.1 | 0.2 | 0.6 | / |

下列说法正确的是
| A.起始时,容器Ⅱ中甲烷的正反应速率大于甲烷的逆反应速率 |
| B.该反应为吸热反应,压强:p2>p1 |
| C.达到平衡时,容器Ⅰ、Ⅱ中CO的物质的量满足:n(CO)Ⅱ<n(CO)Ⅰ |
| D.达到平衡时,容器Ⅱ、Ⅲ中总压强:pⅢ>pⅡ |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐3】某温度下,将2mol H2和2molI2充入密闭的刚性容器中发生反应H2(g)+I2(g) 2HI(g),该反应的v-t图象如图所示,t1时刻测定容器内HI的物质的量为1mol,t2时刻保持等温等容,抽走0.5mol HI.下列有关叙述正确的是
2HI(g),该反应的v-t图象如图所示,t1时刻测定容器内HI的物质的量为1mol,t2时刻保持等温等容,抽走0.5mol HI.下列有关叙述正确的是

 2HI(g),该反应的v-t图象如图所示,t1时刻测定容器内HI的物质的量为1mol,t2时刻保持等温等容,抽走0.5mol HI.下列有关叙述正确的是
2HI(g),该反应的v-t图象如图所示,t1时刻测定容器内HI的物质的量为1mol,t2时刻保持等温等容,抽走0.5mol HI.下列有关叙述正确的是
A.该温度下H2(g)+I2(g) 2HI(g)的平衡常数 2HI(g)的平衡常数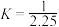 |
| B.反应过程中,可以利用气体的总压强保持不变来判断是否达到平衡 |
| C.t2时刻,抽取HI的瞬间,v′(逆)在图象上的变化应该是c点 |
| D.t2时刻,抽取HI后达到平衡后H2的百分含量减少 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐1】已知反应:
 ,将一定量的
,将一定量的 充入注射器后封口,如图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小),下列说法正确的是
充入注射器后封口,如图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小),下列说法正确的是
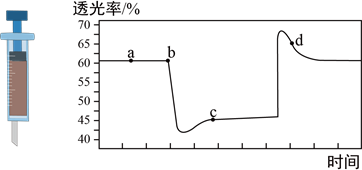

 ,将一定量的
,将一定量的 充入注射器后封口,如图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小),下列说法正确的是
充入注射器后封口,如图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小),下列说法正确的是
| A.a点反应处于平衡状态 |
| B.b点的操作为拉伸注射器 |
C.c点与a点相比,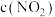 增大, 增大,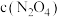 减小 减小 |
D.若容器绝热(与外界无热量交换),则平衡常数 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】在一定温度下,将等物质的量的A和B两种气体混合于2L恒容密闭容器中,发生如下反应: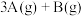
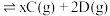 。2min末该反应达平衡,生成0.8
。2min末该反应达平衡,生成0.8 D,
D,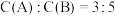 ,C的平均反应速率是0.1
,C的平均反应速率是0.1 。下列判断正确的是
。下列判断正确的是
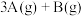
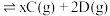 。2min末该反应达平衡,生成0.8
。2min末该反应达平衡,生成0.8 D,
D,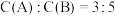 ,C的平均反应速率是0.1
,C的平均反应速率是0.1 。下列判断正确的是
。下列判断正确的是A. |
B.2min内B的反应速率为0.2 |
| C.A的转化率为50% |
| D.混合气体的密度不变或平均相对分子质量不变,都可以表明该反应已达到平衡状态 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐3】N2O5 是一种新型硝化剂,一定温度下发生反应2N2O5(g) 4NO2(g)+O2(g) ΔH>0,T1 温度下的部分实验数据为:
4NO2(g)+O2(g) ΔH>0,T1 温度下的部分实验数据为:
下列说法不正确的是
 4NO2(g)+O2(g) ΔH>0,T1 温度下的部分实验数据为:
4NO2(g)+O2(g) ΔH>0,T1 温度下的部分实验数据为:| t/s | 0 | 500 | 1 000 | 1 500 |
| c(N2O5)/(mol·L-1) | 5.00 | 3.52 | 2.50 | 2.50 |
| A.反应进行到1000s时,该反应已经达到了化学平衡状态 |
| B.T1温度下的平衡常数为K1=125,1 000s时N2O5的转化率为 50% |
| C.其他条件不变时,T2 温度下反应到1000s时测得 N2O5(g)浓度为 2.98 mol·L-1,则有T1<T2 |
| D.T1温度下的平衡常数为 K1,T2 温度下的平衡常数为 K2,若T1>T2,则有 K1<K2 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐1】甲、乙是体积均为 1.0 L 的恒容密闭容器,向甲容器中加入 0.1mol CO2 和 0.3 mol 碳粉,向乙容器中加入 0.4 mol CO,在不同温度下发生反应:CO2(g)+C(s)⇌2CO(g)。达到平衡时 CO 的物质的量浓度随温度的变化如图所示。下列说法正确的是


| A.曲线 II 对应的是乙容器 |
| B.a、b 两点对应平衡体系中的压强之比:pa:pb<14:9 |
| C.b 点对应的平衡体系中,CO 的体积分数小于 4/7 |
D.900 K 时,起始向容器乙中加入 CO、CO2、碳粉各 1 mol,此时  正< 正< 逆 逆 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
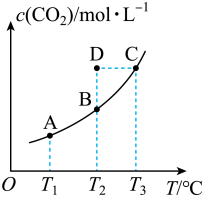
【推荐2】在恒容密闭容器中存在下列平衡:CO(g)+H2O(g) CO2(g)+H2(g)。CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示。下列说法错误的是( )
CO2(g)+H2(g)。CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示。下列说法错误的是( )
 CO2(g)+H2(g)。CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示。下列说法错误的是( )
CO2(g)+H2(g)。CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示。下列说法错误的是( )
A.反应CO(g)+H2O(g) CO2(g)+H2(g)的ΔH<0 CO2(g)+H2(g)的ΔH<0 |
| B.在T2时,若反应处于状态D,则一定有v正<v逆 |
| C.平衡状态A与C相比,平衡状态A的c(CO)大 |
| D.使用合适的催化剂能提高CO的转化率 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列图示与对应的叙述正确的是()


A.a表示反应4CO(g)+2NO2(g) N2(g)+4CO2(g)保持其他条件不变,改变CO的物质的量,平衡时N2的体积分数变化情况,由图可知,NO2的转化率:cba N2(g)+4CO2(g)保持其他条件不变,改变CO的物质的量,平衡时N2的体积分数变化情况,由图可知,NO2的转化率:cba |
| B.b表示25℃时,分别加水稀释体积均为100mL、pH=2的CH3COOH溶液和HX溶液,则25℃时HX的电离平衡常数大于CH3COOH的电离平衡常数 |
| C.c是一定条件下,向含有一定量A的容器中逐渐加入B时的图象,压强p1p2 |
| D.d是在平衡体系的溶液中溶入少量KCl固体后化学反应速率随时间变化的图象 |
您最近一年使用:0次



