在实验室里,用足量的浓盐酸与一定量的高锰酸钾反应(不加热),来制取氯气。
反应:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O
(1)“双线桥法”标出电子转移情况________ 。
(2)若生成2.24L标准状况时的氯气,请计算(写出必要的计算过程):
①理论上需要多少克KMnO4参加反应?________ 。
②被氧化的HCl的物质的量为多少?________ 。
反应:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O
(1)“双线桥法”标出电子转移情况
(2)若生成2.24L标准状况时的氯气,请计算(写出必要的计算过程):
①理论上需要多少克KMnO4参加反应?
②被氧化的HCl的物质的量为多少?
更新时间:2019/12/16 10:52:04
|
相似题推荐
【推荐1】 又称百毒净,可用于水的净化和纸张、纺织品的漂白等。用如图所示装置(夹持装置和加热装置省略)制备
又称百毒净,可用于水的净化和纸张、纺织品的漂白等。用如图所示装置(夹持装置和加热装置省略)制备 并探究
并探究 的某些性质,已知
的某些性质,已知 浓度较大时易分解爆炸。
浓度较大时易分解爆炸。
(1)通入空气的目的为_______ 。
(2)补充并配平实验中制备 的化学方程式:
的化学方程式:_______ 。
_______ _______
_______ _______
_______ _______
_______ _______
_______ _______+_______
_______+_______
工业上也可用 氧化
氧化 溶液制取
溶液制取 ,写出该反应的离子方程式,并用单线桥法标出电子转移的方向和数目:
,写出该反应的离子方程式,并用单线桥法标出电子转移的方向和数目:_______ 。
(3)关闭止水夹②,打开止水夹①③,通入空气一段时间后,装置C中生成了 和气体,反应中
和气体,反应中 表现出
表现出_______ (填“氧化”或“还原”)性;若关闭止水夹③,打开止水夹②,B中可观察到的现象为_______ 。
(4)D装置的作用是_______ 、_______ 。
(5) 和
和 在水处理过程中分别被还原为
在水处理过程中分别被还原为 和
和 。如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么
。如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么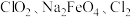 三种消毒杀菌剂的消毒效率由高到低的顺序是
三种消毒杀菌剂的消毒效率由高到低的顺序是_______ (填化学式)。
 又称百毒净,可用于水的净化和纸张、纺织品的漂白等。用如图所示装置(夹持装置和加热装置省略)制备
又称百毒净,可用于水的净化和纸张、纺织品的漂白等。用如图所示装置(夹持装置和加热装置省略)制备 并探究
并探究 的某些性质,已知
的某些性质,已知 浓度较大时易分解爆炸。
浓度较大时易分解爆炸。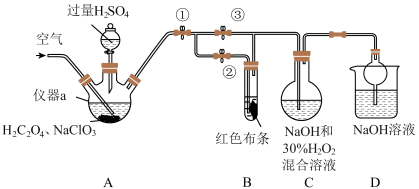
(1)通入空气的目的为
(2)补充并配平实验中制备
 的化学方程式:
的化学方程式:_______
 _______
_______ _______
_______ _______
_______ _______
_______ _______+_______
_______+_______
工业上也可用
 氧化
氧化 溶液制取
溶液制取 ,写出该反应的离子方程式,并用单线桥法标出电子转移的方向和数目:
,写出该反应的离子方程式,并用单线桥法标出电子转移的方向和数目:(3)关闭止水夹②,打开止水夹①③,通入空气一段时间后,装置C中生成了
 和气体,反应中
和气体,反应中 表现出
表现出(4)D装置的作用是
(5)
 和
和 在水处理过程中分别被还原为
在水处理过程中分别被还原为 和
和 。如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么
。如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么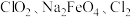 三种消毒杀菌剂的消毒效率由高到低的顺序是
三种消毒杀菌剂的消毒效率由高到低的顺序是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】实验室中可用MnO2或KMnO4固体制备氯气,反应的化学方程式如下:
①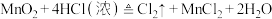
②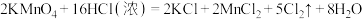
回答下列问题:
(1)对比反应①和②的反应原理,下列作为反应②的发生装置的是_______ (填字母序号)。

(2)反应①和②中,浓盐酸均体现出_______ 性和_______ 性。
(3)用双线桥法,标出下列反应中的电子转移情况_______ 。
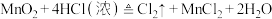
(4)若反应②在水溶液中进行,将反应②改写成离子方程式_______ 。
(5)化学实验中经常提到“酸性高锰酸钾溶液”,这里的“酸性”是因为配制高锰酸钾溶液时加入了_______ (填“硫酸”或“盐酸”)的缘故。
(6)1868年狄肯和洪特发明了用氯化铜作催化剂,在加热到450℃时,用空气中的氧气来氧化氯化氢气体制取氯气的方法——地康法。根据信息,写出该反应的化学方程式_______ 。
①
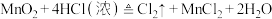
②
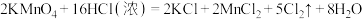
回答下列问题:
(1)对比反应①和②的反应原理,下列作为反应②的发生装置的是

(2)反应①和②中,浓盐酸均体现出
(3)用双线桥法,标出下列反应中的电子转移情况
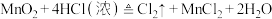
(4)若反应②在水溶液中进行,将反应②改写成离子方程式
(5)化学实验中经常提到“酸性高锰酸钾溶液”,这里的“酸性”是因为配制高锰酸钾溶液时加入了
(6)1868年狄肯和洪特发明了用氯化铜作催化剂,在加热到450℃时,用空气中的氧气来氧化氯化氢气体制取氯气的方法——地康法。根据信息,写出该反应的化学方程式
您最近一年使用:0次
【推荐3】虽然氟元素早在1810年就被发现,但170多年来化学家试图用化学方法制取氟单质的尝试一直未获成功。直到1986年,化学家Karl Christe首次用化学方法制得了F2.他提出的三步反应如下(反应①、②里氟元素化合价不变):
①KMnO4+KF+H2O2+HF→K2MnF6+___________ +H2O
②SbCl5+HF→SbF5+ ___________
③2K2MnF6+ 4SbF5→ 4KSbF6+2MnF3+F2↑
请根据以上反应回答问题:
(1)反应①中空格上应填物质的化学式为___________ 。
(2)完成反应②:___________ 。
(3)反应③中的氧化剂为___________ ,被氧化的元素为___________ 。
(4)配平反应①,并用单线桥标出电子转移的方向和数目:___________ 。
①KMnO4+KF+H2O2+HF→K2MnF6+___________ +H2O
②SbCl5+HF→SbF5+ ___________
③2K2MnF6+ 4SbF5→ 4KSbF6+2MnF3+F2↑
请根据以上反应回答问题:
(1)反应①中空格上应填物质的化学式为
(2)完成反应②:
(3)反应③中的氧化剂为
(4)配平反应①,并用单线桥标出电子转移的方向和数目:
您最近一年使用:0次
【推荐1】物质的类别和核心元素的化合价是研究物质性质的两个基本视角。
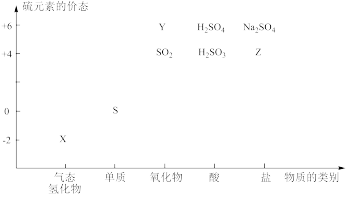
(1)图中X的电子式为_________ ;其水溶液长期在空气中放置容易变浑浊,写出该反应的化学方程式_________ 。
(2)下列物质用于Na2S2O3的制备,从氧化还原反应的角度,理论上有可能的是______ (填字母序号)。
a. Na2S +S b. Z+S c. Na2SO3+Y d. NaHS+NaHSO3
(3)治理含CO、SO2的烟道气,可以将其在催化剂作用下转化为单质S和无毒的气体。
已知:①CO(g)+ O2(g)=CO2(g) ΔH=-283 kJ·mol-1
O2(g)=CO2(g) ΔH=-283 kJ·mol-1
②S(s)+ O2(g)=SO2(g) ΔH=-296 kJ·mol-1
①则治理烟道气反应的热化学方程式为__________ 。
②一定条件下,将CO与SO2以体积比为4∶1置于恒容密闭容器中发生上述反应,下列选项能说明反应达到平衡状态的是__________ (填写字母序号)。
a.v (CO) ∶v(SO2) = 2∶1 b.c(CO)∶c(SO2)∶c(CO2) =2∶1∶2
c.气体密度不变 d.CO2和SO2的体积比保持不变
测得上述反应达平衡时,混合气体中CO的体积分数为 ,则SO2的转化率为
,则SO2的转化率为__________ 。
(4)已知Na2SO3能被K2Cr2O7氧化为Na2SO4则24mL 0.05mol∙L﹣1的Na2SO3溶液与20 mL 0.02mol∙L﹣1的K2Cr2O7溶液恰好反应时,Cr元素在还原产物中的化合价为________ 。

(1)图中X的电子式为
(2)下列物质用于Na2S2O3的制备,从氧化还原反应的角度,理论上有可能的是
a. Na2S +S b. Z+S c. Na2SO3+Y d. NaHS+NaHSO3
(3)治理含CO、SO2的烟道气,可以将其在催化剂作用下转化为单质S和无毒的气体。
已知:①CO(g)+
 O2(g)=CO2(g) ΔH=-283 kJ·mol-1
O2(g)=CO2(g) ΔH=-283 kJ·mol-1②S(s)+ O2(g)=SO2(g) ΔH=-296 kJ·mol-1
①则治理烟道气反应的热化学方程式为
②一定条件下,将CO与SO2以体积比为4∶1置于恒容密闭容器中发生上述反应,下列选项能说明反应达到平衡状态的是
a.v (CO) ∶v(SO2) = 2∶1 b.c(CO)∶c(SO2)∶c(CO2) =2∶1∶2
c.气体密度不变 d.CO2和SO2的体积比保持不变
测得上述反应达平衡时,混合气体中CO的体积分数为
 ,则SO2的转化率为
,则SO2的转化率为(4)已知Na2SO3能被K2Cr2O7氧化为Na2SO4则24mL 0.05mol∙L﹣1的Na2SO3溶液与20 mL 0.02mol∙L﹣1的K2Cr2O7溶液恰好反应时,Cr元素在还原产物中的化合价为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】Na2S2O4 (保险粉)是一种强还原剂,锌粉法制备Na2S2O4的原理为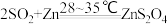 、
、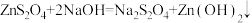 ,制备Na2S2O4的装置(夹持及加热装置已省略)如图所示,回答下列问题:
,制备Na2S2O4的装置(夹持及加热装置已省略)如图所示,回答下列问题:___________ (填名称),导管b的作用是___________ 。
(2)实验开始前,需要向三口烧瓶中充满N2,目的是___________ 。
(3)通入三口烧瓶中的SO2是由铜屑与浓硫酸反应制得的,生成SO2的化学方程式为___________ 。
(4)制备Na2S2O4时,三口烧瓶的加热方式是___________ 。
(5)Zn粉消耗完全后,在搅拌下向三口烧瓶中加入NaOH溶液,充分反应后过滤,向滤液中加入NaCl固体,冷却结晶、过滤、蒸馏水洗涤、酒精洗涤及干燥得产品。加入NaCl固体的作用是___________ ,酒精洗涤的目的是___________ 。
(6)取a g产品溶于适量NaOH溶液,加入亚甲基蓝指示剂,用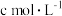 的
的 标准溶液滴定,至终点时消耗
标准溶液滴定,至终点时消耗 标准溶液V mL。
标准溶液V mL。
已知: 被还原为
被还原为 ,
, 被氧化为
被氧化为 。
。
①滴定反应的离子方程式为___________ 。
②产品中Na2S2O4的质量分数为___________ 。(列出计算式)。
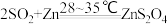 、
、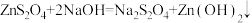 ,制备Na2S2O4的装置(夹持及加热装置已省略)如图所示,回答下列问题:
,制备Na2S2O4的装置(夹持及加热装置已省略)如图所示,回答下列问题: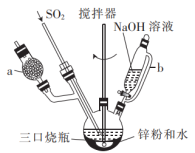
(2)实验开始前,需要向三口烧瓶中充满N2,目的是
(3)通入三口烧瓶中的SO2是由铜屑与浓硫酸反应制得的,生成SO2的化学方程式为
(4)制备Na2S2O4时,三口烧瓶的加热方式是
(5)Zn粉消耗完全后,在搅拌下向三口烧瓶中加入NaOH溶液,充分反应后过滤,向滤液中加入NaCl固体,冷却结晶、过滤、蒸馏水洗涤、酒精洗涤及干燥得产品。加入NaCl固体的作用是
(6)取a g产品溶于适量NaOH溶液,加入亚甲基蓝指示剂,用
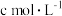 的
的 标准溶液滴定,至终点时消耗
标准溶液滴定,至终点时消耗 标准溶液V mL。
标准溶液V mL。已知:
 被还原为
被还原为 ,
, 被氧化为
被氧化为 。
。①滴定反应的离子方程式为
②产品中Na2S2O4的质量分数为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】六氟锑酸钠(NaSbF6)是一种新开发的锑的精细化工产品,主要用于有机合成、光化学反应、半导体刻蚀等。中南大学的杨天足教授提出了一种在水溶液中由锑白(主要含Sb2O3、Sb2S3和Sb2O5、Fe2O3、CuO等)合成六氟锑酸钠的工艺流程如图所示:

已知:①Sb2O3的性质与Al2O3类似;
②Sb2S3可溶于NaOH溶液;
③NaSbO3·3H2O晶体难溶于水。请回答下列问题:
(1)51Sb在元素周期表中属于_______ 区元素。
(2)“碱浸、还原”时,Sb2O3发生反应的离子方程式为_______ ;若Sb2O5与Na2S2O3反应计量关系为2∶1,则氧化产物为_______ 。
(3)“除杂”时,当溶液中出现蓝色沉淀,立即停止加入CuSO4溶液,测得此时溶液的pH=12,则此时溶液中残留的c(S2-)=_______ mol·L-1[结果保留两位有效数字,常温下,Ksp(CuS)=6.3×10-36,Ksp[Cu(OH)2]=2.1×10-20]。
(4)“转化”时控温约 的原因是
的原因是_______ 。
(5)“氟化”中发生的反应化学方程式为_______ ,此过程不能选择玻璃仪器,是因为_______ 。
(6)氟锑酸化学式为HSbF6,酸性比纯硫酸要强2×1019倍,称为超强酸,其与HF作用生成[H2F]+[SbF6]-,[H2F]+离子的空间构型为_______ 。

已知:①Sb2O3的性质与Al2O3类似;
②Sb2S3可溶于NaOH溶液;
③NaSbO3·3H2O晶体难溶于水。请回答下列问题:
(1)51Sb在元素周期表中属于
(2)“碱浸、还原”时,Sb2O3发生反应的离子方程式为
(3)“除杂”时,当溶液中出现蓝色沉淀,立即停止加入CuSO4溶液,测得此时溶液的pH=12,则此时溶液中残留的c(S2-)=
(4)“转化”时控温约
 的原因是
的原因是(5)“氟化”中发生的反应化学方程式为
(6)氟锑酸化学式为HSbF6,酸性比纯硫酸要强2×1019倍,称为超强酸,其与HF作用生成[H2F]+[SbF6]-,[H2F]+离子的空间构型为
您最近一年使用:0次



