下列实验方案中不能达到相应实验目的的是
A. 探究浓度对化学反应速率的影响 探究浓度对化学反应速率的影响 |
B. 探究催化剂对H2O2分解速率的影响 探究催化剂对H2O2分解速率的影响 |
C.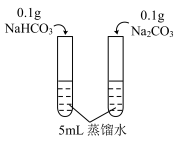 室温下比较NaHCO3和Na2CO3的溶解度 室温下比较NaHCO3和Na2CO3的溶解度 |
D.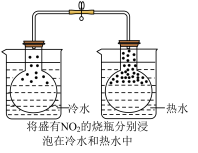 探究温度对化学平衡的影响 探究温度对化学平衡的影响 |
更新时间:2020-01-18 09:55:11
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列情况中反应速率不加快 的是
| A.将在空气中燃着的木条插入盛有纯氧的集气瓶中 |
| B.用煤粉代替煤块燃烧 |
C.增大合成氨反应(N2+3H2 2NH3)体系的压强 2NH3)体系的压强 |
| D.用0.01 mol·L-1的盐酸代替1 mol·L-1的盐酸与铁反应制取氢气 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】碘单质与氢气在一定条件下反应的热化学方程式如下:
①I2(g)+H2(g)⇌2HI(g)△H =-9.48 kJ/mol
②I2(s)+H2(g)⇌2HI(g)△H=+26.48 kJ/mol
下列说法正确的是
①I2(g)+H2(g)⇌2HI(g)△H =-9.48 kJ/mol
②I2(s)+H2(g)⇌2HI(g)△H=+26.48 kJ/mol
下列说法正确的是
| A.该条件下,1 molH2(g)和足量I2(g)充分反应,放出热量9.48 kJ |
| B.该条件下,碘升华的热化学方程式为I2(s)⇌I2(g)△H=+35.96 kJ/mol |
| C.相同条件下,Cl2(g)+H2(g)⇌2HCl(g)的△H>-9.48 kJ/mol |
| D.反应①是放热反应,所以反应①的活化能大于反应②的活化能 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列叙述正确的是
A.恒容密闭容器中进行的反应3A(g) B(g)+C(g),在其它条件不变情况下,再充入一定量的A气体,A的转化率将增大 B(g)+C(g),在其它条件不变情况下,再充入一定量的A气体,A的转化率将增大 |
B.对于可逆反应N2(g)+3H2(g) 2NH3(g),增大氮气浓度可增加活化分子百分数,从而使反应速率增加 2NH3(g),增大氮气浓度可增加活化分子百分数,从而使反应速率增加 |
| C.将AlCl3溶液和NaAlO2溶液分别蒸干后灼烧,所得固体产物均为Al2O3 |
| D.反应NH3(g)+HCl(g)=NH4Cl(s)△H<0在任何条件下均能自发进行 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】为达到相应实验目的,下列实验设计可行的是
| 编号 | 实验目的 | 实验过程 |
| A | 探究浓度对反应速率的影响 | 向 2 支盛有 2mL 0.01mol/L 酸性 KMnO4溶液的试管中分别加入 2mL 0.1mol/L 和 1mL 0.2mol/L的 H2C2O4 溶液,观察溶液褪色所需时间 |
| B | 证明碳酸酸性强于硼酸 | 向饱和碳酸氢钠溶液中滴加少量的硼酸溶液,无气泡产生 |
| C | 证明 Ksp[Fe(OH)3])<Ksp[Mg(OH)2] | 向 盛 有 1mL0.1mol/LMgCl2溶液中滴加1mL0.4mol/LNaOH 溶液,有白色沉淀出现,再滴加 2滴 0.1mol/LFeCl3,静止,有红棕色沉淀出现 |
| D | 除去碱式滴定管内的气泡 | 将尖嘴垂直向下,挤压胶管内玻璃球将气泡排出 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列事实不能 用勒夏特列原理解释的是
A.常温下将 的醋酸溶液稀释10倍,pH<5 的醋酸溶液稀释10倍,pH<5 |
B. 被 被 氧化为 氧化为 的反应,往往需要使用催化剂 的反应,往往需要使用催化剂 |
C.利用 水解制备 水解制备 时,需加入大量水并加热 时,需加入大量水并加热 |
D.向 悬浊液中滴加 悬浊液中滴加 溶液,有红褐色沉淀生成 溶液,有红褐色沉淀生成 |
您最近一年使用:0次
【推荐2】多相催化反应是在催化剂表面通过吸附、解吸过程进行的。如图,我国学者发现T℃时,甲醇(CH3OH)在铜基催化剂上的反应机理如图(该反应为可逆反应):
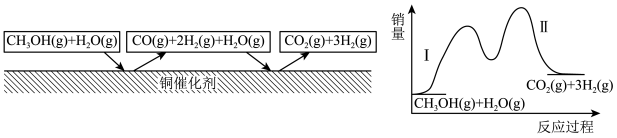
下列有关说法不正确的是

下列有关说法不正确的是
| A.1 mol CH3OH(g)和1 mol H2O(g)的总能量小于1 mol CO2(g)和3 mol H2(g)的总能量 |
B.反应Ⅰ为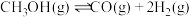 △H>0 △H>0 |
| C.优良的催化剂降低了反应的活化能,并减小△H,节约了能源 |
| D.CH3OH(g)与H2O(g)在高温条件下更有利于正反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】为了说明影响化学反应快慢的因素,甲、乙、丙、丁四位同学分别设计了如下四个实验,你认为结论不正确的是。
| A.将铜片放入稀硫酸中,无现象。若再向所得溶液中加入硝酸银溶液,一段时间后,由于形成原电池,可看到有氢气生成 |
| B.将除去氧化膜的相同大小、相同质量的镁条和铝条与相同浓度盐酸反应,前者速率大于后者 |
| C.两支试管中分别加入根同质量的氯酸钾,其中一支试管中再加入少量二氧化锰,同时加热,产生氧气的快慢不同 |
| D.相同条件下等质量的块状和粉末状大理石与相同浓度盐酸反应时,粉末状的反应速率快 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】探究Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O反应的速率影响因素,设计了以下实验,下列说法正确的是
| 锥形瓶号 | 1 | 2 | 3 | 4 |
| 反应温度/℃ | 20 | 20 | 40 | 40 |
| 0.1 mol/LNa2S2O3溶液/mL | 10 | 10 | 10 | 10 |
| 0.2 mol/LH2SO4溶液/mL | 10 | 5 | 10 | 4 |
| H2O/mL | 0 | x | 0 | 6 |
| 浑浊出现时间/s | 10 | 16 | 5 | 8 |
| 备注 | 第10s反应结束 |
| A.该反应也可以通过单位时间内SO2的体积变化来表示化学反应速率的快慢 |
| B.2号瓶中x为0 |
| C.3号瓶用Na2S2O3来表示反应速率为0.01 mol/(L·s) |
| D.由1号瓶和4号瓶实验结果可得温度越高反应速率越快 |
您最近一年使用:0次

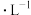 的盐酸与0.65g锌粉反应,若加入适量的下列物质,能加快反应速率但又不影响氢气生成量的是
的盐酸与0.65g锌粉反应,若加入适量的下列物质,能加快反应速率但又不影响氢气生成量的是 溶液
溶液 硫酸
硫酸 溶液
溶液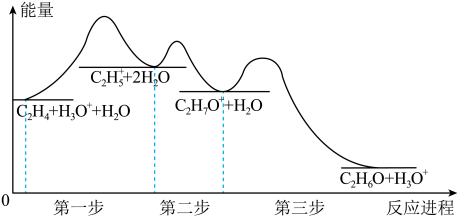
 可增大乙烯的转化率,促进生成更多的乙醇
可增大乙烯的转化率,促进生成更多的乙醇 键的断裂,又有
键的断裂,又有

