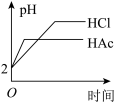
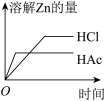
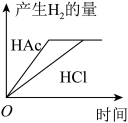
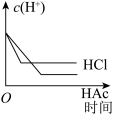
下列事实不能证明H2C2O4(乙二酸)是弱电解质的是( )
| A.草酸能使酸性KMnO4溶液褪色 |
| B.常温下,0.1mol/L的H2C2O4溶液的pH=2 |
| C.浓度均为1mol/L=l的H2C2O4溶液的导电能力比硫酸的导电能力弱 |
| D.常温下,pH=4的H2C2O4溶液稀释100倍,pH约为5 |
更新时间:2020-02-08 09:19:35
|
相似题推荐
【推荐1】食醋是烹饪美食的调味品,其有效成分主要是醋酸( ),下列说法正确的是
),下列说法正确的是
 ),下列说法正确的是
),下列说法正确的是A. 属于离子晶体 属于离子晶体 | B. 含有非极性共价键 含有非极性共价键 |
C. 属于强电解质 属于强电解质 | D. 含有酸基 含有酸基 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列反应的离子方程式正确的是
A.向AgCl悬浊液中滴加氨水,沉淀溶解: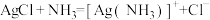 |
B.向 溶液中通入少量 溶液中通入少量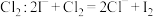 |
C.向 溶液( 溶液(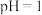 )加入 )加入 溶波: 溶波: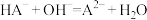 |
D. 溶液中通入少量氯气: 溶液中通入少量氯气: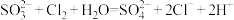 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下,下列说法正确的是( )
| A.pH相等的氨水、醋酸钠溶液中,水的电离程度相同 |
| B.用CH3COOH溶液做导电性实验,灯泡很暗,说明CH3COOH是弱电解质 |
| C.相同物质的量浓度的盐酸与醋酸分别稀释相同倍数,稀释后溶液pH:盐酸<醋酸 |
| D.pH=3的醋酸溶液与pH=11的氢氧化钠溶液等体积混合,混合液呈碱性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】常温下,向浓度均为0.1 mol·L-1、体积均为10mL的两种一元酸(HX、HY)溶液中,分别滴入0.1 mol·L-1NaOH溶液,pH的变化曲线如图所示。下列说法错误的是
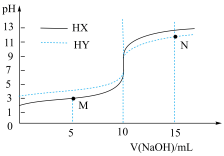

| A.N点:c(Na+)=c(Y-)+c(HY) |
| B.M点:c(X-)>c(Na+) |
| C.滴至pH=7时,消耗NaOH溶液的体积:HX>HY |
| D.滴入10mLNaOH溶液时,溶液中水的电离程度:HX<HY |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】常温下,Ka(HCOOH)=1.77×10-4,Ka(CH3COOH)=1.75×10-5。下列说法不正确 的是
| A.浓度均为0.1mol·L-1的HCOONa和CH3COONa溶液中离子的物质的量浓度之和:前者大于后者 |
| B.用相同浓度的NaOH溶液分别滴定等体积pH均为3的HCOOH和CH3COOH溶液至终点,消耗NaOH溶液的体积:前者小于后者 |
| C.0.2mol·L-1 HCOOH与0.1mol·L-1 NaOH等体积混合后的溶液中:c(HCOO-)+c(OH-)=c(HCOOH)+c(H+) |
| D.0.2mol·L-1 CH3COONa 与 0.1mol·L-1盐酸等体积混合后的溶液中(pH<7):c(CH3COO-)>c(Cl- )>c(CH3COOH)>c(H+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】在25℃的条件下,将体积都为10mL,pH都等于3的醋酸和盐酸,加水稀释到amL和bmL,测得稀释后溶液的pH均为5,则稀释时加入水的体积为( )
| A.a>b=1000mL | B.a=b>1000mL | C.a<b | D.a=b |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列事实能说明H2S是二元酸的是
| A.测0.1mol/L的H2S溶液的pH=3 |
| B.用相同浓度的NaOH进行滴定,消耗的NaOH的体积是H2S溶液体积的2倍 |
| C.NaHS溶液显碱性 |
| D.0.1mol/L的H2S溶液1L与0.2mol Na完全反应,生成标准状况下的H2 2.24L |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列事实能说明亚硝酸是弱电解质的是
| A.用HNO2溶液做导电性实验,灯泡很暗 |
| B.HNO2溶液与Na2CO3溶液混合产生气泡 |
| C.亚硝酸溶液中存在分子,呈酸性 |
| D.向水中加入亚硝酸钠固体,溶液呈碱性 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】硫化氢(H2S)是一种有毒气体,广泛存在于石油化工、冶金等行业的废气中,常用足量纯碱溶液吸收法、热分解法、Fe2(SO4)3溶液氧化脱除法、活性炭吸附氧化法脱除。同时,H2S也是一种重要的化工原料,可以用来制备硫磺、苯硫酚(C6H5SH)、H2S、NaHS还常用于脱除水体中的Cu2+,形成黑色、不溶于稀硫酸的CuS沉淀。室温时,通过下列实验探究NaHS溶液的性质
下列有关说法不正确 的是
| 实验 | 实验操作和现象 |
| 1 | 用pH试纸测量0.1 mol/L NaHS溶液的pH,测得pH约为7.8 |
| 2 | 将浓度均为0.001 mol/L NaHS溶液与CuSO4溶液等体积混合,有黑色沉淀产生 |
| A.0.1 mol/L NaHS溶液中有:c(H2S)>c(S2—) |
| B.0.1 mol/L NaHS溶液中存在:c(H+)+c(H2S)= c(OH—)+2c(S2—) |
| C.实验2发生反应的离子方程式:HS—+ Cu2+ = CuS↓+ H+ |
| D.实验2的上层清液中c(H+)·c(OH—)=1×10—14 |
您最近一年使用:0次

 +2H2O
+2H2O +H2O
+H2O