某兴趣小组在实验室进行如下实验探究活动。
(1)设计如下实验研究2Fe3++2I- 2Fe2++I2的反应。
2Fe2++I2的反应。
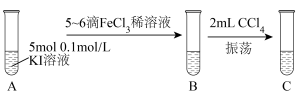
①振荡静置后C中观察到的现象是_______________________ ;为证明该反应存在一定限度,还应补做实验为:取C中分液后的上层溶液,然后______________ (写出实验操作和现象)。
②测定上述KI溶液的浓度,进行以下操作:
I用移液管移取20.00 mL KI溶液至锥形瓶中,加入适量稀硫酸酸化,再加入足量H2O2溶液,充分反应。
II小心加热除去过量的H2O2。
III用淀粉做指示剂,用c mol/L Na2S2O3标准溶液滴定,反应原理为:2Na2S2O3+I2=2NaI+Na2S4O6。
步骤II是否可省略?____________ (答“可以”或“不可以”)
步骤III达到滴定终点的现象是___________________________ 。已知I2浓度很高时,会与淀粉形成稳定的包合物不易解离,为避免引起实验误差,加指示剂的最佳时机是________ 。
(2)探究Mn2+对KMnO4酸性溶液与H2C2O4溶液反应速率的影响。
反应原理(化学方程式)为________ ;
仪器及药品:试管(两支)、0.01 mol/L KMnO4酸性溶液、0.1 mol/L H2C2O4溶液、一粒黄豆大的MnSO4固体;
实验方案:请仿照教材(或同教材)设计一个实验用表格,在行标题或列标题中注明试剂及观察或记录要点。______________
(1)设计如下实验研究2Fe3++2I-
 2Fe2++I2的反应。
2Fe2++I2的反应。
①振荡静置后C中观察到的现象是
②测定上述KI溶液的浓度,进行以下操作:
I用移液管移取20.00 mL KI溶液至锥形瓶中,加入适量稀硫酸酸化,再加入足量H2O2溶液,充分反应。
II小心加热除去过量的H2O2。
III用淀粉做指示剂,用c mol/L Na2S2O3标准溶液滴定,反应原理为:2Na2S2O3+I2=2NaI+Na2S4O6。
步骤II是否可省略?
步骤III达到滴定终点的现象是
(2)探究Mn2+对KMnO4酸性溶液与H2C2O4溶液反应速率的影响。
反应原理(化学方程式)为
仪器及药品:试管(两支)、0.01 mol/L KMnO4酸性溶液、0.1 mol/L H2C2O4溶液、一粒黄豆大的MnSO4固体;
实验方案:请仿照教材(或同教材)设计一个实验用表格,在行标题或列标题中注明试剂及观察或记录要点。
更新时间:2020-02-12 10:16:05
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
真题
名校
【推荐1】用FeCl3酸性溶液脱除H2S后的废液,通过控制电压电解得以再生。某同学使用石墨电极,在不同电压(x)下电解pH=1的0.1mol/LFeCl2溶液,研究废液再生机理。记录如下(a、b、c代表电压值:)
(1)用KSCN溶液检验出Fe3+的现象是_______ 。
(2)I中,Fe2+产生的原因可能是Cl-在阳极放电,生成的Cl2将Fe2+氧化。写出有关反应的方程式_____ 。
(3)由II推测,Fe3+产生的原因还可能是Fe2+在阳极放电,原因是Fe2+具有_____ 性。
(4)II中虽未检测出Cl2,但Cl-在阳极是否放电仍需进一步验证。电解pH=1的NaCl溶液做对照实验,记录如下:
①NaCl溶液的浓度是________ mol/L。
②IV中检测Cl2的实验方法:____________________ 。
③与II对比,得出的结论(写出两点):___________________ 。
| 序号 | 电压/V | 阳极现象 | 检验阳极产物 |
| I | x≥a | 电极附近出现黄色,有气泡产生 | 有Fe3+、有Cl2 |
| II | a>x≥b | 电极附近出现黄色,无气泡产生 | 有Fe3+、无Cl2 |
| III | b>x>0 | 无明显变化 | 无Fe3+、无Cl2 |
(2)I中,Fe2+产生的原因可能是Cl-在阳极放电,生成的Cl2将Fe2+氧化。写出有关反应的方程式
(3)由II推测,Fe3+产生的原因还可能是Fe2+在阳极放电,原因是Fe2+具有
(4)II中虽未检测出Cl2,但Cl-在阳极是否放电仍需进一步验证。电解pH=1的NaCl溶液做对照实验,记录如下:
| 序号 | 电压/V | 阳极现象 | 检验阳极产物 |
| IV | a>x≥c | 无明显变化 | 有Cl2 |
| V | c>x≥b | 无明显变化 | 无Cl2 |
②IV中检测Cl2的实验方法:
③与II对比,得出的结论(写出两点):
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】为分析某盐的成分,做了如图的实验,请回答:
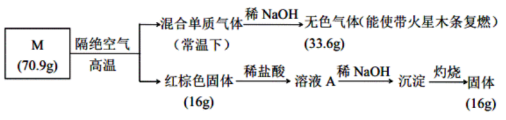
(1)盐M的化学式是:________ 。
(2)盐M隔绝空气分解的化学方程式为________ 。
(3)向溶液A中通入H2S气体的离子方程式:_________ (不考虑空气影响)。

(1)盐M的化学式是:
(2)盐M隔绝空气分解的化学方程式为
(3)向溶液A中通入H2S气体的离子方程式:
您最近一年使用:0次
【推荐3】为验证氧化性Cl2>Fe3+>SO2,某小组用下图所示装置进行实验(夹持仪器和A中加热装置已省略,气密性已检验)。

已知:Na2SO3+H2SO4=SO2↑+Na2SO4+H2O
实验过程:
I.打开弹簧夹K1~K4,通入一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1、K3、K4。
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热。
Ⅲ.当B中溶液变黄时,停止加热,夹紧弹簧夹K2。
Ⅳ.打开活塞b,使约2mL的溶液流入D试管中,检验其中的离子。
Ⅴ.打开弹簧夹K3、活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹K3。
Ⅵ.更新试管D,重复过程Ⅳ,检验B溶液中的离子。
Ⅶ.实验结束后,打开弹簧夹K1~K4,再通入一段时间N2,然后拆卸,洗涤,整理仪器。
(1)A中反应的化学方程式为_______ 。
(2)棉花中浸润的溶液是_______ 。
(3)步骤Ⅲ中溶液变黄的离子方程式是_______ ,能说明氧化性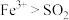 的离子方程式是
的离子方程式是_______ 。
(4)过程Ⅶ的目的是_______ 。
(5)甲、乙、丙三位同学分别完成了上述实验,结论如下表所示。他们的检测结果一定能够证明氧化性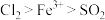 的是
的是_______ (填“甲”、“乙”、“丙”)。
(6)将B中的 溶液换成
溶液换成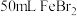 溶液并向其中通入
溶液并向其中通入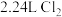 (标准状况下),若溶液中有
(标准状况下),若溶液中有 的
的 被氧化成单质
被氧化成单质 ,则原
,则原 溶液中
溶液中 的物质的量浓度为
的物质的量浓度为_______ 。

已知:Na2SO3+H2SO4=SO2↑+Na2SO4+H2O
实验过程:
I.打开弹簧夹K1~K4,通入一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1、K3、K4。
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热。
Ⅲ.当B中溶液变黄时,停止加热,夹紧弹簧夹K2。
Ⅳ.打开活塞b,使约2mL的溶液流入D试管中,检验其中的离子。
Ⅴ.打开弹簧夹K3、活塞c,加入70%的硫酸,一段时间后夹紧弹簧夹K3。
Ⅵ.更新试管D,重复过程Ⅳ,检验B溶液中的离子。
Ⅶ.实验结束后,打开弹簧夹K1~K4,再通入一段时间N2,然后拆卸,洗涤,整理仪器。
(1)A中反应的化学方程式为
(2)棉花中浸润的溶液是
(3)步骤Ⅲ中溶液变黄的离子方程式是
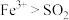 的离子方程式是
的离子方程式是(4)过程Ⅶ的目的是
(5)甲、乙、丙三位同学分别完成了上述实验,结论如下表所示。他们的检测结果一定能够证明氧化性
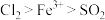 的是
的是| 过程Ⅳ B溶液中含有的离子 | 过程Ⅵ B溶液中含有的离子 | |
| 甲 | 既有 又有 又有 | 有 |
| 乙 | 有 无 无 | 有 |
| 丙 | 有 无 无 | 有 |
(6)将B中的
 溶液换成
溶液换成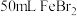 溶液并向其中通入
溶液并向其中通入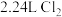 (标准状况下),若溶液中有
(标准状况下),若溶液中有 的
的 被氧化成单质
被氧化成单质 ,则原
,则原 溶液中
溶液中 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】完成下列小题
(1)页岩气不仅能用作燃料,还可用于生产合成气(CO和 )。
)。 与
与 通入聚集太阳能反应器,发生反应
通入聚集太阳能反应器,发生反应
 。
。
已知:Ⅰ. 、
、 、CO的燃烧热(
、CO的燃烧热( )分别为
)分别为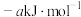 、
、 、
、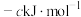 ;
;
Ⅱ.
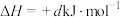 。
。
则
_____  (用含字母a、b、c、d的代数式表示)。
(用含字母a、b、c、d的代数式表示)。
(2)用合成气生成甲醇的反应为
 ,在10L恒容密闭容器中按物质的量之比1:2充入CO和
,在10L恒容密闭容器中按物质的量之比1:2充入CO和 ,200℃时
,200℃时 随时间的变化如表所示:
随时间的变化如表所示:
①0~3min内用 表示的反应速率
表示的反应速率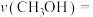
_____ 。
②200℃时,该反应的平衡常数
_____ 。向上述200℃达到平衡的恒容密闭容器中再加入5molCO、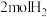 、
、 ,保持温度不变,则反应
,保持温度不变,则反应_____ (填“正向”“逆向”或“不”)进行。
③上述反应如果在绝热恒容的密闭环境下进行,下列各项可作为该反应达到平衡状态的标志的是_____ (填字母)。
A.混合气体密度不再变化
B.容器内的温度保持不变
C.CO和 的物质的量之比保持不变
的物质的量之比保持不变
D.CO的消耗速率与 的生成速率之比为1:1
的生成速率之比为1:1
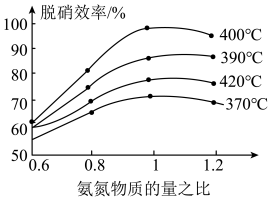
(3)汽车尾气是雾霾形成的原因之一、研究氮氧化物的处理方法可有效减少雾霾的形成,可采用在催化剂作用下氧化还原法脱硝: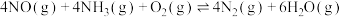
 。根据图示判断提高脱硝效率的最佳条件是
。根据图示判断提高脱硝效率的最佳条件是_____ ;氨氮物质的量之比一定时,在400℃时,脱硝效率最大,其可能的原因是_____ 。
(1)页岩气不仅能用作燃料,还可用于生产合成气(CO和
 )。
)。 与
与 通入聚集太阳能反应器,发生反应
通入聚集太阳能反应器,发生反应
 。
。已知:Ⅰ.
 、
、 、CO的燃烧热(
、CO的燃烧热( )分别为
)分别为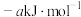 、
、 、
、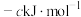 ;
;Ⅱ.

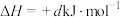 。
。则

 (用含字母a、b、c、d的代数式表示)。
(用含字母a、b、c、d的代数式表示)。(2)用合成气生成甲醇的反应为

 ,在10L恒容密闭容器中按物质的量之比1:2充入CO和
,在10L恒容密闭容器中按物质的量之比1:2充入CO和 ,200℃时
,200℃时 随时间的变化如表所示:
随时间的变化如表所示:| t/min | 0 | 1 | 3 | 5 |
 /mol /mol | 8.0 | 5.4 | 4.0 | 4.0 |
 表示的反应速率
表示的反应速率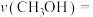
②200℃时,该反应的平衡常数

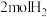 、
、 ,保持温度不变,则反应
,保持温度不变,则反应③上述反应如果在绝热恒容的密闭环境下进行,下列各项可作为该反应达到平衡状态的标志的是
A.混合气体密度不再变化
B.容器内的温度保持不变
C.CO和
 的物质的量之比保持不变
的物质的量之比保持不变D.CO的消耗速率与
 的生成速率之比为1:1
的生成速率之比为1:1(3)汽车尾气是雾霾形成的原因之一、研究氮氧化物的处理方法可有效减少雾霾的形成,可采用在催化剂作用下氧化还原法脱硝:
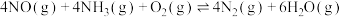
 。根据图示判断提高脱硝效率的最佳条件是
。根据图示判断提高脱硝效率的最佳条件是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐2】当今,世界多国相继规划了碳达峰、碳中和的时间节点,降低空气中二氧化碳含量成为研究热点。因此,研发二氧化碳的利用技术,将二氧化碳转化为能源是缓解环境和能源问题的方案之一、
I.利用二氧化碳催化加氢制甲醇(CH3OH)。
CO2和H2在一定条件下合成甲醇。在2L恒容密闭容器中充入总物质的量为6mol的CO2和H2发生反应: ,改变氢碳比[
,改变氢碳比[ ],在不同温度下反应达到平衡状态,测得的实验数据如下表。
],在不同温度下反应达到平衡状态,测得的实验数据如下表。
(1)下列说法中正确的是___________(填标号);
(2)在700K、氢碳比为3.0的条件下,若5min时反应达到平衡状态,则0~5min内用H2表示的平均反应速率为___________ ;
(3)该反应一般认为通过如下步骤来实现:
①
②
总反应的
___________  ;若反应①为慢反应,下列示意图中能体现上述反应能量变化的是
;若反应①为慢反应,下列示意图中能体现上述反应能量变化的是___________ (填标号)。

II.二氧化碳催化加氢合成乙烯的原理为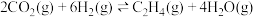 。原料初始组成
。原料初始组成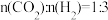 ,体系压强恒定为0.1MPa,不同温度下反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图所示。
,体系压强恒定为0.1MPa,不同温度下反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图所示。

(4)图中曲线a代表四种物质中的_______ (填化学式);
(5)利用A点数据,计算630K时反应的平衡常数Kp=______  (列出计算式即可。以分压表示,分压=总压×物质的量分数)。
(列出计算式即可。以分压表示,分压=总压×物质的量分数)。
III.电解法转化CO2可实现CO2的资源化利用。
(6)电解CO2制 的原理示意图如下所示,反应时阴极电极反应式为
的原理示意图如下所示,反应时阴极电极反应式为___________ 。

I.利用二氧化碳催化加氢制甲醇(CH3OH)。
CO2和H2在一定条件下合成甲醇。在2L恒容密闭容器中充入总物质的量为6mol的CO2和H2发生反应:
 ,改变氢碳比[
,改变氢碳比[ ],在不同温度下反应达到平衡状态,测得的实验数据如下表。
],在不同温度下反应达到平衡状态,测得的实验数据如下表。温度/K CO2转化率/%
| 500 | 600 | 700 | 800 |
| 1.5 | 45 | 33 | 20 | 12 |
| 2.0 | 60 | 43 | 28 | 15 |
| 3.0 | 83 | 62 | 40 | 22 |
| A.v(CH3OH)=v(CO2)时,反应达到平衡 |
| B.增大氢碳比,平衡正向移动,平衡常数增大 |
| C.CO2和H2合成甲醇为放热反应 |
| D.当混合气体密度不变时,达到平衡 |
(3)该反应一般认为通过如下步骤来实现:
①

②

总反应的

 ;若反应①为慢反应,下列示意图中能体现上述反应能量变化的是
;若反应①为慢反应,下列示意图中能体现上述反应能量变化的是
II.二氧化碳催化加氢合成乙烯的原理为
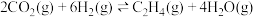 。原料初始组成
。原料初始组成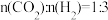 ,体系压强恒定为0.1MPa,不同温度下反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图所示。
,体系压强恒定为0.1MPa,不同温度下反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图所示。
(4)图中曲线a代表四种物质中的
(5)利用A点数据,计算630K时反应的平衡常数Kp=
 (列出计算式即可。以分压表示,分压=总压×物质的量分数)。
(列出计算式即可。以分压表示,分压=总压×物质的量分数)。III.电解法转化CO2可实现CO2的资源化利用。
(6)电解CO2制
 的原理示意图如下所示,反应时阴极电极反应式为
的原理示意图如下所示,反应时阴极电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐3】Cu2O是一种重要的工业原料,广泛川作催化剂。
Ⅰ.制备Cu2O
(1)微乳液—还原法:在100℃的Cu(NO3)2溶液中加入一定体积的NaOH溶液,搅拌均匀,再逐滴加入肼(N2H4)产生红色沉淀,抽滤、洗涤、干燥,得到Cu2O。
已知:N2H4(l)+O2(g)=N2(g)+2H2O(l)△H=-akJ·mol-1
Cu(OH)2(s)=CuO(s)+H2O(l)△H=+bkJ·mol-1
4CuO(s)=2Cu2O(s)+O2(g)△H=+ckJ·mol-1
则由N2H4(l)和Cu(OH)2(s)反应制备Cu2O(s)的热化学方程式为___
(2)电解法:纳米级Cu2O由于具有优良的催化性能而受到关注。
采用阴离子交换膜制备纳米级Cu2O的装置如图所示:
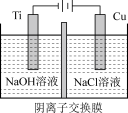
阳极的电极反应式为_____ 。
Ⅱ.纳米级Cu2O催化剂可用于工业上合成甲醇:
CO(g)+2H2(g)⇌CH3OH(g)△H=-90.8kJ·mol-1
(3)能说明反应CO(g)+2H2(g) CH3OH(g)已达平衡状态的是(填字母)。
CH3OH(g)已达平衡状态的是(填字母)。
(4)t℃时,在体积为2L固定体积的密闭容器中加入2.00molH2(g)和1.00molCO(g),起始总压为30kPa,CO的物质的量随时间的变化如表:
根据表中数据回答:
①0~5s内CH3OH的平均速率是_____ ,氢气平衡转化率为_____ 。
②t℃时该反应的压力平衡常数Kp为_____ 。(用平衡分压代替平衡浓度,气体分压=总压×物质的量分数)
③保持其它条件不变,向平衡体系中充入1molCO(g)、2molH2(g)、1molCH3OH(g);此时v正_____ v逆(填“>”“<”或“=”)。
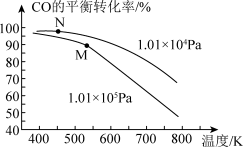
(5)工业实际合成CH3OH生产中,采用如图M点而不是N点对应的反应条件,运用化学反应速率和化学平衡知识,同时考虑生产实际,说明选择该反应条件的理由:_____
Ⅰ.制备Cu2O
(1)微乳液—还原法:在100℃的Cu(NO3)2溶液中加入一定体积的NaOH溶液,搅拌均匀,再逐滴加入肼(N2H4)产生红色沉淀,抽滤、洗涤、干燥,得到Cu2O。
已知:N2H4(l)+O2(g)=N2(g)+2H2O(l)△H=-akJ·mol-1
Cu(OH)2(s)=CuO(s)+H2O(l)△H=+bkJ·mol-1
4CuO(s)=2Cu2O(s)+O2(g)△H=+ckJ·mol-1
则由N2H4(l)和Cu(OH)2(s)反应制备Cu2O(s)的热化学方程式为
(2)电解法:纳米级Cu2O由于具有优良的催化性能而受到关注。
采用阴离子交换膜制备纳米级Cu2O的装置如图所示:

阳极的电极反应式为
Ⅱ.纳米级Cu2O催化剂可用于工业上合成甲醇:
CO(g)+2H2(g)⇌CH3OH(g)△H=-90.8kJ·mol-1
(3)能说明反应CO(g)+2H2(g)
 CH3OH(g)已达平衡状态的是(填字母)。
CH3OH(g)已达平衡状态的是(填字母)。| A.CO的消耗速率等于CH3OH的生成速率 |
| B.一定条件,CO的转化率不再变化 |
| C.在绝热恒容的容器中,反应的平衡常数不再变化 |
| D.CO和H2的浓度比不变 |
时间(s) | 0 | 2 | 5 | 10 | 20 | 40 | 80 |
| 物质的量(mol) | 1.00 | 0.50 | 0.375 | 0.25 | 0.20 | 0.20 | 0.20 |
①0~5s内CH3OH的平均速率是
②t℃时该反应的压力平衡常数Kp为
③保持其它条件不变,向平衡体系中充入1molCO(g)、2molH2(g)、1molCH3OH(g);此时v正
(5)工业实际合成CH3OH生产中,采用如图M点而不是N点对应的反应条件,运用化学反应速率和化学平衡知识,同时考虑生产实际,说明选择该反应条件的理由:

您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐1】硫酸锆[Zr(SO4)2·4H2O],是制取原子能级锆及其它锆化合物的中间原料,并大量用作皮革鞣剂、羊毛处理剂、催化剂等。下面是以锆英砂(主要成分为ZrO2,伴有杂质SiO2)为原料,利用碱熔法再进行酸浸制备硫酸锆的工艺过程。
已知:①Na2ZrO3、ZrOCl2、Zr(SO4)2均易溶于水,难溶于酒精及其他有机溶剂
②ZrOCl2⇌ZrO2++2Cl-;ZrO2++ ⇌ZrOSO4
⇌ZrOSO4
③ZrO2++2H2O⇌ZrO(OH)2+2H+

(1)步骤1中用到的仪器有泥三角、___________ (填“铁”或“瓷”)坩埚、坩埚钳等
(2)下列说法正确的是___________。
(3)如图装置,经过一系列操作完成操作2中的抽滤和洗涤。请选择合适的编号,按正确的操作顺序补充完整:开抽气泵→a→d→b→( )→( )→( )→( )→b→e→关抽气泵,______ 。
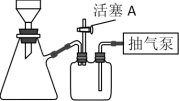
a.转移固液混合物;b.确认抽干;c.加浓盐酸洗涤;d.关闭活塞A;e.打开活塞A;f.加无水乙醇洗涤
(4)ZrOCl2·8H2O洗涤后,在800℃下灼烧可得一种用于制备压电陶瓷的原料ZrO2,写出该灼烧过程的化学方程式___________ 。
(5)实验室可以用络合滴定法测定锆含量。
已知:ZrO2+与二甲酚橙生成红色络合物,ZrO2+能与EDTA发生络合反应(1:1)生成无色络合物,且络合能力更强。

①样品溶解时,需要加入盐酸溶解,原因是:___________ 。
②产品中锆的含量是___________ (用含c、V、m的代数式表达)
③下列有关上述滴定操作的说法正确的是___________ 。

A.滴定管活塞涂凡士林:用手指蘸取少量凡士林涂抹一薄层在活塞a、b(如上图)处的四周,平行插入活塞槽中,然后朝同一个方向转动
B.滴定开始时可以将液体成线状快速流下,接近终点时减慢滴加速度,必要时采用半滴操作
C.读数时应将滴定管从架上取下,捏住管上端无刻度处,使滴定管保持垂直
D.第一次滴定终点时,若测得消耗标准液体积小于5.00mL,则第二次滴定时可稀释待测液后重新滴定来减小误差
已知:①Na2ZrO3、ZrOCl2、Zr(SO4)2均易溶于水,难溶于酒精及其他有机溶剂
②ZrOCl2⇌ZrO2++2Cl-;ZrO2++
 ⇌ZrOSO4
⇌ZrOSO4③ZrO2++2H2O⇌ZrO(OH)2+2H+

(1)步骤1中用到的仪器有泥三角、
(2)下列说法正确的是___________。
| A.副产物1为H2SiO3、副产物2为NaCl、副产物3为HClO |
| B.步骤3加入HCl作用是与Na2ZrO3反应生成ZrOCl2,还能降低ZrOCl2的溶解度 |
| C.操作1为蒸发结晶、趁热过滤;操作2为重结晶 |
| D.制备的Zr(SO4)2·4H2O溶于水溶液呈酸性 |
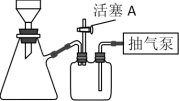
a.转移固液混合物;b.确认抽干;c.加浓盐酸洗涤;d.关闭活塞A;e.打开活塞A;f.加无水乙醇洗涤
(4)ZrOCl2·8H2O洗涤后,在800℃下灼烧可得一种用于制备压电陶瓷的原料ZrO2,写出该灼烧过程的化学方程式
(5)实验室可以用络合滴定法测定锆含量。
已知:ZrO2+与二甲酚橙生成红色络合物,ZrO2+能与EDTA发生络合反应(1:1)生成无色络合物,且络合能力更强。

①样品溶解时,需要加入盐酸溶解,原因是:
②产品中锆的含量是
③下列有关上述滴定操作的说法正确的是

A.滴定管活塞涂凡士林:用手指蘸取少量凡士林涂抹一薄层在活塞a、b(如上图)处的四周,平行插入活塞槽中,然后朝同一个方向转动
B.滴定开始时可以将液体成线状快速流下,接近终点时减慢滴加速度,必要时采用半滴操作
C.读数时应将滴定管从架上取下,捏住管上端无刻度处,使滴定管保持垂直
D.第一次滴定终点时,若测得消耗标准液体积小于5.00mL,则第二次滴定时可稀释待测液后重新滴定来减小误差
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐2】定量分析是化学实验中重要的组成部分。
Ⅰ.中和热的测定:
(1)在实验室中,用50 mL 0.40 mol/L的盐酸与50 mL 0.50mol/L的NaOH溶液反应测定和热。假设此时溶液密度均为1 g/cm3,生成溶液的比容热c = 4.18 J/(g•℃),实验起始温度为T1℃,终止温度为T2℃,请写出中和热的计算式(写出最后结果)△H=__________ kJ/mol。
(2)1L1mol/LH2SO4溶液与2L1mol/LNaOH溶液完全反应,放出114.6 kJ的热量。请写出表示该反应中和热的热化学方程式___________________ 。
Ⅱ.氧化还原滴定实验与中和滴定类似。为测定某H2C2O4溶液的浓度,取该溶液于锥形瓶中,加入适量稀H2SO4后,用浓度为c mol/L KMnO4标准溶液滴定。
(3)滴定原理为:_____________________ (用离子方程式表示)。
(4)滴定时,KMnO4溶液应装在__________ (填“酸式”或“碱式”)滴定管中,达到滴定终点时的颜色变化为_____________ 。
(5)如图表示50mL滴定管中液面的位置,此时滴定管中液面的读数为__________ mL。

(6)为了减小实验误差,该同学一共进行了三次实验,假设每次所取H2C2O4溶液体积均为VmL,三次实验结果记录如下:
从上表可以看出,第一次实验中记录消耗KMnO4溶液的体积明显多于后两次,其原因可能是____________ 。
A.实验结束时俯视刻度线读取滴定终点时KMnO4溶液的体积
B.滴加KMnO4溶液过快,未充分振荡,刚看到溶液变色,立刻停止滴定
C.第一次滴定盛装标准液的滴定管装液前用蒸馏水清洗过,未用标准液润洗,后两次均用标准液润洗
D.第一次滴定用的锥形瓶用待装液润洗过,后两次未润洗
(7)写出计算H2C2O4的物质的量浓度的最简表达式:c=_________ mol/L。
Ⅰ.中和热的测定:
(1)在实验室中,用50 mL 0.40 mol/L的盐酸与50 mL 0.50mol/L的NaOH溶液反应测定和热。假设此时溶液密度均为1 g/cm3,生成溶液的比容热c = 4.18 J/(g•℃),实验起始温度为T1℃,终止温度为T2℃,请写出中和热的计算式(写出最后结果)△H=
(2)1L1mol/LH2SO4溶液与2L1mol/LNaOH溶液完全反应,放出114.6 kJ的热量。请写出表示该反应中和热的热化学方程式
Ⅱ.氧化还原滴定实验与中和滴定类似。为测定某H2C2O4溶液的浓度,取该溶液于锥形瓶中,加入适量稀H2SO4后,用浓度为c mol/L KMnO4标准溶液滴定。
(3)滴定原理为:
(4)滴定时,KMnO4溶液应装在
(5)如图表示50mL滴定管中液面的位置,此时滴定管中液面的读数为

(6)为了减小实验误差,该同学一共进行了三次实验,假设每次所取H2C2O4溶液体积均为VmL,三次实验结果记录如下:
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗KMnO4溶液体积/mL | 26.32 | 24.02 | 23.98 |
A.实验结束时俯视刻度线读取滴定终点时KMnO4溶液的体积
B.滴加KMnO4溶液过快,未充分振荡,刚看到溶液变色,立刻停止滴定
C.第一次滴定盛装标准液的滴定管装液前用蒸馏水清洗过,未用标准液润洗,后两次均用标准液润洗
D.第一次滴定用的锥形瓶用待装液润洗过,后两次未润洗
(7)写出计算H2C2O4的物质的量浓度的最简表达式:c=
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐3】铬及其化合物在催化、金属防腐等方面具有重要应用。
(1)催化剂 可由
可由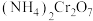 加热分解制备,反应同时生成无污染气体。
加热分解制备,反应同时生成无污染气体。
①完成化学方程式: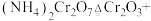 ______
______ 。
。_______ 。
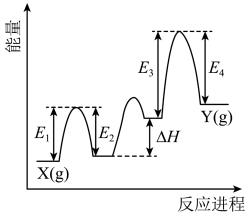
② 催化丙烷脱氢过程中,部分反应历程如图,X(g)→Y(g)过程的焓变为
催化丙烷脱氢过程中,部分反应历程如图,X(g)→Y(g)过程的焓变为_______ (列式表示)。
(2)用重铬酸钾法(一种氧化还原滴定法)可测定产物 中的
中的 含量,请写出酸性条件下K2Cr2O7与
含量,请写出酸性条件下K2Cr2O7与 反应的离子方程式
反应的离子方程式_______ (K2Cr2O7被还原为 )。
)。
(3)若需配制浓度为 的
的 标准溶液250mL,应准确称取K2Cr2O7
标准溶液250mL,应准确称取K2Cr2O7_______ g(保留四位有效数字,已知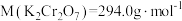 )。配制该标准溶液时,下列仪器一定不会用到的有
)。配制该标准溶液时,下列仪器一定不会用到的有_______ 。
①电子天平 ②烧杯 ③量筒 ④玻璃棒 ⑤250mL容量瓶 ⑥胶头滴管 ⑦托盘天平
(4)若配制K2Cr2O7标准溶液时,俯视刻度线,则测定结果_______ (填“偏大”、“偏小”或“不变”,下同);滴定操作中,若滴定前装有K2Cr2O7标准溶液的滴定管尖嘴部分有气泡,而滴定结束后气泡消失,则滴定结果将_______ 。
(5)K2Cr2O7溶液中存在多个平衡。本题条件下仅需考虑如下平衡:
(i)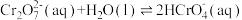

(ii)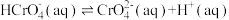
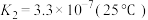
下列有关K2Cr2O7溶液的说法正确的有_______。
(1)催化剂
 可由
可由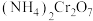 加热分解制备,反应同时生成无污染气体。
加热分解制备,反应同时生成无污染气体。①完成化学方程式:
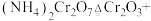 ______
______ 。
。②
 催化丙烷脱氢过程中,部分反应历程如图,X(g)→Y(g)过程的焓变为
催化丙烷脱氢过程中,部分反应历程如图,X(g)→Y(g)过程的焓变为
(2)用重铬酸钾法(一种氧化还原滴定法)可测定产物
 中的
中的 含量,请写出酸性条件下K2Cr2O7与
含量,请写出酸性条件下K2Cr2O7与 反应的离子方程式
反应的离子方程式 )。
)。(3)若需配制浓度为
 的
的 标准溶液250mL,应准确称取K2Cr2O7
标准溶液250mL,应准确称取K2Cr2O7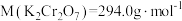 )。配制该标准溶液时,下列仪器一定不会用到的有
)。配制该标准溶液时,下列仪器一定不会用到的有①电子天平 ②烧杯 ③量筒 ④玻璃棒 ⑤250mL容量瓶 ⑥胶头滴管 ⑦托盘天平
(4)若配制K2Cr2O7标准溶液时,俯视刻度线,则测定结果
(5)K2Cr2O7溶液中存在多个平衡。本题条件下仅需考虑如下平衡:
(i)
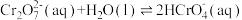

(ii)
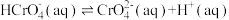
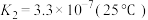
下列有关K2Cr2O7溶液的说法正确的有_______。
| A.加入少量硫酸,溶液的pH不变 |
| B.加入少量水稀释,溶液中离子总数增加 |
| C.加入少NaOH量溶液,反应(ⅰ)的平衡逆向移动 |
D.加入少量K2Cr2O7,固体,平衡时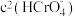 与 与 的比值保持不变 的比值保持不变 |
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐1】某化学学习小组欲探究铁及其化合物的氧化性和还原性。请你协助他们完成实验报告。
(1)实验目的:探究铁及其化合物的氧化性和还原性
(2)实验试剂及仪器:
试剂:氯化亚铁溶液、氯化铁溶液、氯水、KSCN溶液、铁粉、锌片、铜片、稀硫酸
仪器:胶头滴管外,你认为本实验必不可少的一种玻璃仪器是 。
(3)实验记录(在仿照①实验作答,划线部分不必填写)
(4)学习小组的同学将从本实验中获得的知识推广到其他类物质的学习,请判断下列物质既有氧化性又有还原性的是
A、Cl2 B、Na C、Mg2+ D、H2O2
(5)在实验②中,有部分同学在氯化亚铁溶液中滴入KSCN溶液后,就出现了血红色,你认为是什么原因: ;
你将对实验员在配制氯化亚铁溶液时,提出的建议是 。
(6)在配制氯化铁溶液时,由于实验员失误,可能导致溶液中含有少量的Fe2+,为帮助实验员进行检验少量Fe2+的存在,请从下列物质中选择合适的试剂( )
A、KSCN溶液 B、稀盐酸 C、KMnO4 溶液 D、NaOH溶液
(1)实验目的:探究铁及其化合物的氧化性和还原性
(2)实验试剂及仪器:
试剂:氯化亚铁溶液、氯化铁溶液、氯水、KSCN溶液、铁粉、锌片、铜片、稀硫酸
仪器:胶头滴管外,你认为本实验必不可少的一种玻璃仪器是 。
(3)实验记录(在仿照①实验作答,划线部分不必填写)
| 序号 | 实验设计 | 实验观察(主要现象) | 离子方程式 | 解释与结论 |
| ① | 在铁粉中滴 入稀硫酸 | 铁粉溶解,溶液由无 色变成浅绿色,有无 色无味的的气体生成 | Fe +2H+= H2↑+ Fe2+ | Fe具有还原性 |
② | 氯化亚铁溶液中滴入KSCN溶液,再加入氯水 | 滴入KSCN溶液无明 显变化,加入氯水立 即变成血红色 | ||
| ③ | 氯化亚铁溶液加 入锌片 | Fe2++ Zn =" Fe" + Zn 2+ | ||
④ | Fe3+具有氧化性 |
A、Cl2 B、Na C、Mg2+ D、H2O2
(5)在实验②中,有部分同学在氯化亚铁溶液中滴入KSCN溶液后,就出现了血红色,你认为是什么原因: ;
你将对实验员在配制氯化亚铁溶液时,提出的建议是 。
(6)在配制氯化铁溶液时,由于实验员失误,可能导致溶液中含有少量的Fe2+,为帮助实验员进行检验少量Fe2+的存在,请从下列物质中选择合适的试剂( )
A、KSCN溶液 B、稀盐酸 C、KMnO4 溶液 D、NaOH溶液
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐2】某校化学兴趣小组探究SO2与FeCl3溶液的反应,所用装置如图所示:
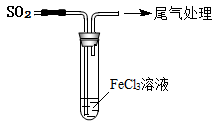
(1)该小组同学预测SO2与FeCl3溶液反应的现象为溶液由棕黄色变成浅绿色,发生反应的离子方程式为_______ 。
(2)按上图所示开始实验:
FeCl3溶液显酸性的原因是(用离子方程式表示)_______ 。
(3)当SO2通入到FeCl3溶液中,同学们观察到的现象是溶液立即由棕黄色变成红棕色。将混合液放置12小时,溶液才变成浅绿色。
【查阅资料】 Fe(HSO3)2+离子为红棕色,它可以将Fe3+还原为Fe2+。生成Fe(HSO3)2+离子的反应为可逆反应。
①请用化学用语表示SO2与FeCl3溶液反应生成红棕色Fe(HSO3)2+离子过程:_______ 。
②写出溶液中Fe(HSO3)2+离子与Fe3+反应的离子方程式:_______ 。
③请应用反应速率和反应限度知识解释产生上述实验现象的原因:_______ 。
(4)为了探究如何缩短红棕色变为浅绿色的时间,该小组同学进行了步骤③的实验。综合上述实验探究过程,可以获得的实验结论:
I.SO2与FeCl3溶液反应生成红棕色中间产物Fe(HSO3)2+离子;
II.红棕色中间产物转变成浅绿色溶液是一个较慢的过程;
III._______ 。

(1)该小组同学预测SO2与FeCl3溶液反应的现象为溶液由棕黄色变成浅绿色,发生反应的离子方程式为
(2)按上图所示开始实验:
| 步骤ⅰ | 配制1 mol·L-1 FeCl3溶液(未用盐酸酸化),测其pH约为1,取少量装入试管中。然后缓缓通入SO2气体。 |
| 步骤ⅱ | 往5mL1mol·L-1 FeCl3溶液中通入SO2气体,溶液立即变为红棕色。微热3 min,溶液颜色变为浅绿色。 |
| 步骤ⅲ | 往5mL重新配制的1mol·L-1 FeCl3溶液(用浓盐酸酸化)中通入SO2气体,溶液立即变为红棕色。几分钟后,发现溶液颜色变成浅绿色。 |
(3)当SO2通入到FeCl3溶液中,同学们观察到的现象是溶液立即由棕黄色变成红棕色。将混合液放置12小时,溶液才变成浅绿色。
【查阅资料】 Fe(HSO3)2+离子为红棕色,它可以将Fe3+还原为Fe2+。生成Fe(HSO3)2+离子的反应为可逆反应。
①请用化学用语表示SO2与FeCl3溶液反应生成红棕色Fe(HSO3)2+离子过程:
②写出溶液中Fe(HSO3)2+离子与Fe3+反应的离子方程式:
③请应用反应速率和反应限度知识解释产生上述实验现象的原因:
(4)为了探究如何缩短红棕色变为浅绿色的时间,该小组同学进行了步骤③的实验。综合上述实验探究过程,可以获得的实验结论:
I.SO2与FeCl3溶液反应生成红棕色中间产物Fe(HSO3)2+离子;
II.红棕色中间产物转变成浅绿色溶液是一个较慢的过程;
III.
您最近一年使用:0次
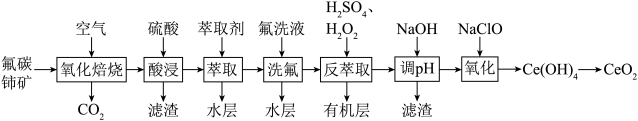
【推荐3】二氧化铈(CeO2)可用作玻璃工业添加剂和有机反应催化剂。以氟碳铈矿(主要含有CeFCO3)为原料制备二氧化铈的一种工艺流程如图所示。
已知:①Ce4+能与F-结合成CeF3+,Al3+也能与F-结合成AlF ;
;
②Ce4+能被萃取剂TBP萃取,而Ce3+不能。
回答下列问题:
(1)“氧化焙烧”生成固体产物CeO2和CeF4,写出该反应的化学方程式___________ 。
(2)TBP是一种有机萃取剂,“萃取”时发生反应:CeF3++TBP CeTBP4++F-,氟洗液中添加Al3+的作用是
CeTBP4++F-,氟洗液中添加Al3+的作用是___________ 。
(3)“反萃取”时加入H2SO4和H2O2的混合液,H2O2的作用为___________ 。
(4)“反萃取”后的水层溶液中c(Ce3+)=1.0mol•L-1,c(Al3+)=0.01mol•L-1。室温下,“调pH”时,先除去Al3+,若忽略过程中溶液的体积变化,则加入NaOH调节溶液pH的范围是___________ ,过滤后,再向滤液中加入NaOH使Ce3+沉淀完全。
已知:①室温下,当溶液中的离子浓度c≤1.0×10-5mol•L-1时,可认为该离子沉淀完全。
②Ksp[Al(OH)3]=1.0×10-32,Ksp[Ce(OH)3]=1.0×10-21
(5)“氧化”时发生反应的离子方程式为___________ 。
(6)用10吨含70%CeFCO3的矿石,按上述工艺生产,制得4.3吨CeO2,则CeO2的产率为___________ (保留3位有效数字,写出计算过程)。

已知:①Ce4+能与F-结合成CeF3+,Al3+也能与F-结合成AlF
 ;
;②Ce4+能被萃取剂TBP萃取,而Ce3+不能。
回答下列问题:
(1)“氧化焙烧”生成固体产物CeO2和CeF4,写出该反应的化学方程式
(2)TBP是一种有机萃取剂,“萃取”时发生反应:CeF3++TBP
 CeTBP4++F-,氟洗液中添加Al3+的作用是
CeTBP4++F-,氟洗液中添加Al3+的作用是(3)“反萃取”时加入H2SO4和H2O2的混合液,H2O2的作用为
(4)“反萃取”后的水层溶液中c(Ce3+)=1.0mol•L-1,c(Al3+)=0.01mol•L-1。室温下,“调pH”时,先除去Al3+,若忽略过程中溶液的体积变化,则加入NaOH调节溶液pH的范围是
已知:①室温下,当溶液中的离子浓度c≤1.0×10-5mol•L-1时,可认为该离子沉淀完全。
②Ksp[Al(OH)3]=1.0×10-32,Ksp[Ce(OH)3]=1.0×10-21
(5)“氧化”时发生反应的离子方程式为
(6)用10吨含70%CeFCO3的矿石,按上述工艺生产,制得4.3吨CeO2,则CeO2的产率为
您最近一年使用:0次



