铜是一种古老而又年轻的金属元素,铜及其化合物在生产生活中有着广泛的应用。
(1)古代留下来的青铜器表面呈绿色,原因是在潮湿的空气中,铜易发生腐蚀生成铜绿,有关反应的化学方程式为______ 。
(2)现代工业主要采用高温冶炼黄铜矿 ,也可表示为
,也可表示为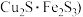 的方法获得铜。火法炼铜首先要焙烧黄铜矿:
的方法获得铜。火法炼铜首先要焙烧黄铜矿: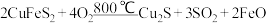 ,每转移0.6mol电子,有
,每转移0.6mol电子,有______ mol硫原子被氧化。写出火法炼铜由 得到Cu的总方程式
得到Cu的总方程式______ 。
(3) 可用于游泳池水的消毒,原因是
可用于游泳池水的消毒,原因是______ 。
(4)向 和
和 的混合溶液中加入CuO粉末会产生新的沉淀,该沉淀的主要成分的化学式为
的混合溶液中加入CuO粉末会产生新的沉淀,该沉淀的主要成分的化学式为______ (已知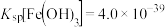 ,
,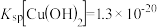 )。
)。
(5)利用Cu和 溶液的反应可制作印刷线路板,为了从含有
溶液的反应可制作印刷线路板,为了从含有 、
、 、
、 的废液中回收Cu,某化学兴趣小组的同学设计了以下两种实验方案:
的废液中回收Cu,某化学兴趣小组的同学设计了以下两种实验方案:
方案1:向废液中加入过量铁粉,充分反应后过滤。在所得滤渣中加入足量盐酸,充分反应后,再过滤即得到铜。方案1中涉及的四种阳离子的氧化性由强到弱的顺序为______ 。
方案2:在废液中加入适量的盐酸调节溶液的pH=1,用铜和石墨作电极进行电解。当观察到阴极上有少量气泡产生时,即停止电解,这时Cu已全部析出,在电极上可直接回收铜。操作比方案1简便,但方案2也有不足之处,主要表现为______ 。
(1)古代留下来的青铜器表面呈绿色,原因是在潮湿的空气中,铜易发生腐蚀生成铜绿,有关反应的化学方程式为
(2)现代工业主要采用高温冶炼黄铜矿
 ,也可表示为
,也可表示为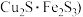 的方法获得铜。火法炼铜首先要焙烧黄铜矿:
的方法获得铜。火法炼铜首先要焙烧黄铜矿: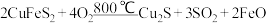 ,每转移0.6mol电子,有
,每转移0.6mol电子,有 得到Cu的总方程式
得到Cu的总方程式(3)
 可用于游泳池水的消毒,原因是
可用于游泳池水的消毒,原因是(4)向
 和
和 的混合溶液中加入CuO粉末会产生新的沉淀,该沉淀的主要成分的化学式为
的混合溶液中加入CuO粉末会产生新的沉淀,该沉淀的主要成分的化学式为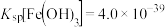 ,
,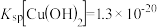 )。
)。(5)利用Cu和
 溶液的反应可制作印刷线路板,为了从含有
溶液的反应可制作印刷线路板,为了从含有 、
、 、
、 的废液中回收Cu,某化学兴趣小组的同学设计了以下两种实验方案:
的废液中回收Cu,某化学兴趣小组的同学设计了以下两种实验方案:方案1:向废液中加入过量铁粉,充分反应后过滤。在所得滤渣中加入足量盐酸,充分反应后,再过滤即得到铜。方案1中涉及的四种阳离子的氧化性由强到弱的顺序为
方案2:在废液中加入适量的盐酸调节溶液的pH=1,用铜和石墨作电极进行电解。当观察到阴极上有少量气泡产生时,即停止电解,这时Cu已全部析出,在电极上可直接回收铜。操作比方案1简便,但方案2也有不足之处,主要表现为
更新时间:2020-02-26 10:04:14
|
相似题推荐
【推荐1】镓(Ga)是一种重要的稀散金属,广泛应用于半导体制造行业。一种从黄磷电尘灰[主要含Ga2O3、ZnO、PbO、Al2O3、MgO、Ca5(PO4)3OH、SiO2]中回收镓并分离特定金属的工艺路线如图所示:
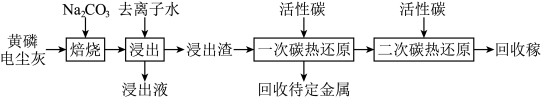
请回答下列问题:
(1)Ga是与Al同主族的第四周期元素,其价电子排布式为______ :
(2)“焙烧”过程中,Ca5(PO4)3OH转化为可溶性的Na3PO4,SiO2与Na2CO3反应生成可溶性钠盐。
①为使焙烧充分,可采取的措施是______ (写一点)。
②写出SiO2与Na2CO3反应的化学方程式__________________ 。
(3)“浸出”时,浸出液中溶质转化为Na2HPO4和NaOH的离子方程式为____________ 。Na2HPO4和NaOH的溶解度曲线如图所示,不考虑其他溶质,将浸出液蒸发浓缩、冷却结晶,先析出的物质是______ (填化学式)。

(4)“碳热还原”时,活性炭将金属氧化物还原为相应的金属单质。反应过程中,相关金属在不同压强下的起始生成温度和沸点如下表所示:
①“一次碳热还原”和“二次碳热还原”是反应温度不同的两步反应。从促进反应发生和实现工序目的的角度出发,“一次碳热还原”时,下列反应条件中最合理的是______ (填标号)。
A.1173K、10Pa B.1173K、 Pa C.1473K、10Pa D.1473K、
Pa C.1473K、10Pa D.1473K、 Pa
Pa
②“二次碳热还原”中,少量副产物Ga2O与产物Ga一起挥发出来。冷凝时(惰性气体作保护气),在产物Ga中检测出少量的Ga2O3,可能的原因是__________________ (用化学方程式表示)。
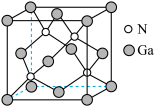
(5)氮化镓是用于高科技领域的半导体材料,其立方晶胞结构如图所示,晶胞参数为a nm。Ga的配位数为______ ,两个氮原子间的最近距离是______ nm。氮化镓的晶胞密度为______ g·cm (列出计算式即可,
(列出计算式即可, 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。

请回答下列问题:
(1)Ga是与Al同主族的第四周期元素,其价电子排布式为
(2)“焙烧”过程中,Ca5(PO4)3OH转化为可溶性的Na3PO4,SiO2与Na2CO3反应生成可溶性钠盐。
①为使焙烧充分,可采取的措施是
②写出SiO2与Na2CO3反应的化学方程式
(3)“浸出”时,浸出液中溶质转化为Na2HPO4和NaOH的离子方程式为

(4)“碳热还原”时,活性炭将金属氧化物还原为相应的金属单质。反应过程中,相关金属在不同压强下的起始生成温度和沸点如下表所示:
| 压强/Pa | 起始生成温度/K | 金属沸点/K | ||||||||
| Zn | Pb | Al | Mg | Ga | Zn | Pb | Al | Mg | Ga | |
| 10 | 784 | 657 | >1473 | >1473 | 918 | 681 | 1110 | 1566 | 783 | 1453 |
 | 1223 | 1038 | >1473 | >1473 | 1284 | 1180 | 2013 | 2600 | 1380 | 2676 |
A.1173K、10Pa B.1173K、
 Pa C.1473K、10Pa D.1473K、
Pa C.1473K、10Pa D.1473K、 Pa
Pa②“二次碳热还原”中,少量副产物Ga2O与产物Ga一起挥发出来。冷凝时(惰性气体作保护气),在产物Ga中检测出少量的Ga2O3,可能的原因是
(5)氮化镓是用于高科技领域的半导体材料,其立方晶胞结构如图所示,晶胞参数为a nm。Ga的配位数为
 (列出计算式即可,
(列出计算式即可, 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】硫酸铁是一种重要的化工原料,用铁矿石(主要成分为 ,还含有少量的
,还含有少量的 、
、 、
、 、有机杂质)制备硫酸铁流程如下:
、有机杂质)制备硫酸铁流程如下:
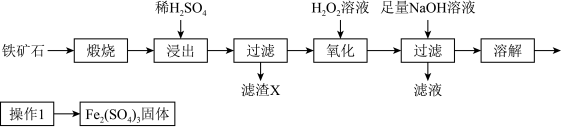
(1)“煅烧”时使用的仪器是_____ 。
(2)请写出“浸出”过程中FeO与 反应
反应 化学方程式
化学方程式_____ ;检验滤液中是否含有Fe3+的试剂可以是_____ 。
(3)滤渣X的成分为_____ 。
(4)“氧化”过程中发生的离子方程式为_____ 。
(5)“操作1”包括_____ 、过滤、洗涤、干燥。
 ,还含有少量的
,还含有少量的 、
、 、
、 、有机杂质)制备硫酸铁流程如下:
、有机杂质)制备硫酸铁流程如下:
(1)“煅烧”时使用的仪器是
(2)请写出“浸出”过程中FeO与
 反应
反应 化学方程式
化学方程式(3)滤渣X的成分为
(4)“氧化”过程中发生的离子方程式为
(5)“操作1”包括
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】氯气常用于自来水的杀菌消毒,实验室常用 和浓盐酸共热制备氯气。
和浓盐酸共热制备氯气。
(1)写出该反应的化学方程式:________ ,其中氧化剂和还原剂的物质的量之比为_____ 。
(2) 固体与浓盐酸在常温下就可以反应制备氯气,反应的化学方程式为
固体与浓盐酸在常温下就可以反应制备氯气,反应的化学方程式为______ (已知酸性条件下 可被还原为
可被还原为 )。
)。
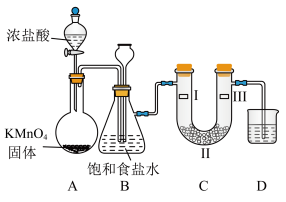
(3) 固体与浓盐酸的反应装置如图所示,同时验证氯气性质(其中夹持装置已省略)。
固体与浓盐酸的反应装置如图所示,同时验证氯气性质(其中夹持装置已省略)。
①从反应条件看, 和
和 的氧化能力不同,氧化能力较强的是
的氧化能力不同,氧化能力较强的是______ 。
②装置B的作用为_________ ;装置C中若发生堵塞,装置B中的实验现象为_______ 。
③装置C的作用是验证氯气是否具有漂白性,则装置C中Ⅰ、Ⅱ、Ⅲ处依次应放入的物质正确的是_______ 。
④D中的液体是___________ (填化学式)
(4)用氯气对自来水消毒易产生致癌物质,二氧化氯是一种更为高效安全的消毒剂。工业上制备 的反应为
的反应为 。
。
①该反应中的还原产物是______ (写化学式),反应中每生成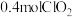 ,转移电子的数目为
,转移电子的数目为______ 。
② 在杀菌消毒的过程中会生成副产物亚氯酸盐(
在杀菌消毒的过程中会生成副产物亚氯酸盐( ),需要将其转化为
),需要将其转化为 除去,下列试剂能实现其转化过程的是
除去,下列试剂能实现其转化过程的是______ (填序号)。
A. B.
B. C.KI D.
C.KI D.
 和浓盐酸共热制备氯气。
和浓盐酸共热制备氯气。(1)写出该反应的化学方程式:
(2)
 固体与浓盐酸在常温下就可以反应制备氯气,反应的化学方程式为
固体与浓盐酸在常温下就可以反应制备氯气,反应的化学方程式为 可被还原为
可被还原为 )。
)。(3)
 固体与浓盐酸的反应装置如图所示,同时验证氯气性质(其中夹持装置已省略)。
固体与浓盐酸的反应装置如图所示,同时验证氯气性质(其中夹持装置已省略)。
①从反应条件看,
 和
和 的氧化能力不同,氧化能力较强的是
的氧化能力不同,氧化能力较强的是②装置B的作用为
③装置C的作用是验证氯气是否具有漂白性,则装置C中Ⅰ、Ⅱ、Ⅲ处依次应放入的物质正确的是
| Ⅰ | Ⅱ | Ⅲ | |
| A | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
| B | 干燥的有色布条 | 无水硫酸铜 | 湿润的有色布条 |
| C | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
| D | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
(4)用氯气对自来水消毒易产生致癌物质,二氧化氯是一种更为高效安全的消毒剂。工业上制备
 的反应为
的反应为 。
。①该反应中的还原产物是
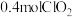 ,转移电子的数目为
,转移电子的数目为②
 在杀菌消毒的过程中会生成副产物亚氯酸盐(
在杀菌消毒的过程中会生成副产物亚氯酸盐( ),需要将其转化为
),需要将其转化为 除去,下列试剂能实现其转化过程的是
除去,下列试剂能实现其转化过程的是A.
 B.
B. C.KI D.
C.KI D.
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】实验表明,将CuSO4溶液与Na2CO3溶液混合有蓝绿色沉淀生成。为了探究该沉淀的化学成分(假设为单一成分,且不含结晶水),某同学设计如下实验。回答下列问题:
(1)蓝绿色沉淀可能为a.___________ ;b.CuCO3;c.碱式碳酸铜【化学式可表示为mCu(OH)2·nCuCO3】。
(2)从悬浊液中获得蓝绿色固体必须用的玻璃仪器有___________ 。
(3)取一定量蓝绿色固体,用如下装置(夹持仪器已省略)进行定性实验。
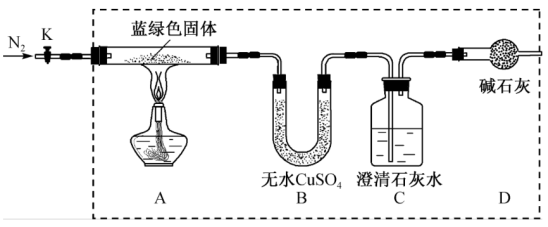
①盛放碱石灰的仪器名称为___________ 。
②检查上述虚线框内装置气密性的实验操作:连接好装置后,关闭K,___________ 。
③若蓝绿色沉淀为CuCO3,则观察到的现象是___________ 。
④实验过程中发现,装置B中无水CuSO4变蓝,装置C中有白色沉淀生成,为测定蓝绿色固体的化学组成,在装置B中盛放足量无水CaCl2,C中盛放足量NaOH溶液再次进行实验。C中盛放NaOH溶液,而不使用澄清石灰水的原因是___________ ;若蓝绿色固体质量为27.1g,实验结束后,装置B的质量增加2.7g,C中溶液增重4.4g,则该蓝绿色固体的化学式为___________ 。
(1)蓝绿色沉淀可能为a.
(2)从悬浊液中获得蓝绿色固体必须用的玻璃仪器有
(3)取一定量蓝绿色固体,用如下装置(夹持仪器已省略)进行定性实验。

①盛放碱石灰的仪器名称为
②检查上述虚线框内装置气密性的实验操作:连接好装置后,关闭K,
③若蓝绿色沉淀为CuCO3,则观察到的现象是
④实验过程中发现,装置B中无水CuSO4变蓝,装置C中有白色沉淀生成,为测定蓝绿色固体的化学组成,在装置B中盛放足量无水CaCl2,C中盛放足量NaOH溶液再次进行实验。C中盛放NaOH溶液,而不使用澄清石灰水的原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】固体化合物 X 由 3 种元素组成。某学习小组进行了如下实验:
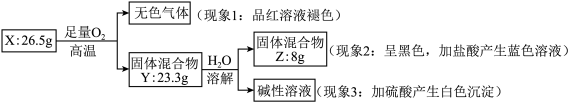
请回答:
(1)由现象 1 得出化合物 X 含有____ 元素(填元素符号),X 的化学式_____ 。
(2)固体混合物 Y 的成分_____ (填化学式)。
(3)实验室常将氨气(NH3)通过红热的黑色固体化合物 Z 制备氮气,该反应的化学方程式是___ ,当有28克氮气生成时转移的电子的物质的量为______ mol。

请回答:
(1)由现象 1 得出化合物 X 含有
(2)固体混合物 Y 的成分
(3)实验室常将氨气(NH3)通过红热的黑色固体化合物 Z 制备氮气,该反应的化学方程式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某化学研究性学习小组探究与铜有关的物质的性质,过程设计如下:
提出猜想:
问题1:在元素周期表中,铜与铝的位置很接近,氢氧化铝具有两性,氢氧化铜有两性吗?
问题2:铁和铜都有变价,一般情况下,Fe2+的稳定性弱于的Fe3+,Cu+的稳定性也弱于Cu2+吗?
问题3:硫酸铜溶液呈蓝色,铜与浓硝酸常温下反应生成的溶液也是蓝色吗?
实验探究:
Ⅰ.解决问题1:
(1)实验需配制100mL0.50mol•L-1CuSO4溶液,必需的玻璃仪器有胶头滴管、烧杯、___ 、___ 。
(2)为达到目的,某同学认为只要进行两次实验即可得出结论。请写出实验②的具体内容。
①向盛有CuSO4溶液的试管中滴加NaOH溶液至过量,观察生成的Cu(OH)2沉淀是否溶解;
②___ 。
Ⅱ.解决问题2的实验和现象如下:
①取一定量制得的氢氧化铜固体,于坩埚中灼烧,当温度达到80~100℃时得到黑色固体粉末;继续加热至1000℃以上,黑色粉末全部变成红色粉末氧化亚铜;
②取适量红色氧化亚铜粉末于洁净试管中,加入过量的稀硫酸,得到蓝色溶液,同时观察到试管底部还有红色固体存在。根据以上实验及现象回答下列问题:
(3)写出氧化亚铜与稀硫酸反应的离子方程式:___ 。
(4)从实验中可得出的结论:当温度在1000℃以上时___ (填Cu2+或Cu+,下同)稳定,在酸性溶液中___ 稳定。
Ⅲ.解决问题3,某同学设计的实验如下:
取一铜片装入试管,加入适量的浓硝酸,观察溶液的颜色变化。
(5)另一同学认为此同学设计的实验有缺陷,原因是___ 。
(6)铜与浓硝酸反应溶液呈绿色,有同学认为这是生成的NO2溶于其中的原因。请设计实验说明此解释是否正确(只需要写出一种方法即可)。___
提出猜想:
问题1:在元素周期表中,铜与铝的位置很接近,氢氧化铝具有两性,氢氧化铜有两性吗?
问题2:铁和铜都有变价,一般情况下,Fe2+的稳定性弱于的Fe3+,Cu+的稳定性也弱于Cu2+吗?
问题3:硫酸铜溶液呈蓝色,铜与浓硝酸常温下反应生成的溶液也是蓝色吗?
实验探究:
Ⅰ.解决问题1:
(1)实验需配制100mL0.50mol•L-1CuSO4溶液,必需的玻璃仪器有胶头滴管、烧杯、
(2)为达到目的,某同学认为只要进行两次实验即可得出结论。请写出实验②的具体内容。
①向盛有CuSO4溶液的试管中滴加NaOH溶液至过量,观察生成的Cu(OH)2沉淀是否溶解;
②
Ⅱ.解决问题2的实验和现象如下:
①取一定量制得的氢氧化铜固体,于坩埚中灼烧,当温度达到80~100℃时得到黑色固体粉末;继续加热至1000℃以上,黑色粉末全部变成红色粉末氧化亚铜;
②取适量红色氧化亚铜粉末于洁净试管中,加入过量的稀硫酸,得到蓝色溶液,同时观察到试管底部还有红色固体存在。根据以上实验及现象回答下列问题:
(3)写出氧化亚铜与稀硫酸反应的离子方程式:
(4)从实验中可得出的结论:当温度在1000℃以上时
Ⅲ.解决问题3,某同学设计的实验如下:
取一铜片装入试管,加入适量的浓硝酸,观察溶液的颜色变化。
(5)另一同学认为此同学设计的实验有缺陷,原因是
(6)铜与浓硝酸反应溶液呈绿色,有同学认为这是生成的NO2溶于其中的原因。请设计实验说明此解释是否正确(只需要写出一种方法即可)。
| 实验步骤 | 实验结论 |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】根据化学平衡理论,请回答下列几个问题:
(1)某温度(t℃)时,水中c(H+)和c(OH-)的关系如图所示,a点水的离子积Kw=____ 。该温度下,pH=12的NaOH溶液与pH=2的H2SO4溶液等体积混合,溶液显____ (填“酸”、“碱”或“中”)性。

(2)向含有酚酞的0.1mol·L-1的氨水中加入少量NH4Cl固体,观察到的现象是____ ,请结合离子方程式分析产生该现象的主要原因是:____ 。
(3)将体积相等的NaOH稀溶液和CH3COOH溶液混合,若溶液呈中性,则溶液中c(Na+)____ c(CH3COO-)(填“>”、“<”或“=”),则混合前c(NaOH)____ c(CH3COOH)(填“>”、“<”或“=”)。
(4)为配制SbCl3溶液,取少量SbCl3固体溶于2~3mL水中,观察到有白色沉淀生成,为避免出现该现象,配制SbCl3溶液的正确方法是____ 。
(5)25℃时,已知Ksp[Cu(OH)2]=2×10-20,要使c(Cu2+)=0.2mol·L-1溶液中的Cu2+沉淀较完全[残留在溶液中的c(Cu2+)降低到2×10-4mol·L-1],则应加入NaOH溶液调节pH为____ 。
(6)用可溶性碳酸盐,可以浸取CaSO4固体,则溶液浸取过程中会发生反应:CaSO4(s)+CO (aq)
(aq) CaCO3(s)+SO
CaCO3(s)+SO (aq)。已知298K时,Ksp(CaCO3)=2.80×10-9,Ksp(CaSO4)=4.90×10-5,则此温度下该反应的平衡常数K为
(aq)。已知298K时,Ksp(CaCO3)=2.80×10-9,Ksp(CaSO4)=4.90×10-5,则此温度下该反应的平衡常数K为____ (计算结果保留三位有效数字)。
(1)某温度(t℃)时,水中c(H+)和c(OH-)的关系如图所示,a点水的离子积Kw=

(2)向含有酚酞的0.1mol·L-1的氨水中加入少量NH4Cl固体,观察到的现象是
(3)将体积相等的NaOH稀溶液和CH3COOH溶液混合,若溶液呈中性,则溶液中c(Na+)
(4)为配制SbCl3溶液,取少量SbCl3固体溶于2~3mL水中,观察到有白色沉淀生成,为避免出现该现象,配制SbCl3溶液的正确方法是
(5)25℃时,已知Ksp[Cu(OH)2]=2×10-20,要使c(Cu2+)=0.2mol·L-1溶液中的Cu2+沉淀较完全[残留在溶液中的c(Cu2+)降低到2×10-4mol·L-1],则应加入NaOH溶液调节pH为
(6)用可溶性碳酸盐,可以浸取CaSO4固体,则溶液浸取过程中会发生反应:CaSO4(s)+CO
 (aq)
(aq) CaCO3(s)+SO
CaCO3(s)+SO (aq)。已知298K时,Ksp(CaCO3)=2.80×10-9,Ksp(CaSO4)=4.90×10-5,则此温度下该反应的平衡常数K为
(aq)。已知298K时,Ksp(CaCO3)=2.80×10-9,Ksp(CaSO4)=4.90×10-5,则此温度下该反应的平衡常数K为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】向某草酸溶液中滴加KOH溶液,溶液中 、
、 、
、 的物质的量浓度分数δ(X)[
的物质的量浓度分数δ(X)[ ]与pH的关系如图所示:
]与pH的关系如图所示:
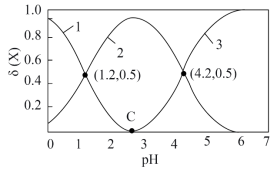
请回答下列问题:
(1)室温下,草酸的一级电离常数 为
为_______ ;
(2)①向草酸溶液中滴加KOH溶液至 的过程中主要反应的离子方程式为
的过程中主要反应的离子方程式为_______ 。
②0.1 moL
 溶液中,
溶液中,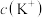
_______ 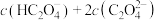 (填“>”、“<”或“=”);
(填“>”、“<”或“=”);
(3)室温下,通过下列实验探究0.0100 mol⋅L
 溶液的性质:
溶液的性质:
实验1:实验测得0.0100 mol⋅L
 溶液的pH为8.6。
溶液的pH为8.6。
实验2:向溶液中滴加等体积、0.0100 mol⋅L HCl溶液。pH由8.6降为4.8。
HCl溶液。pH由8.6降为4.8。
实验3:向溶液中加入等体积0.0200 mol⋅L
 溶液,出现白色沉淀。
溶液,出现白色沉淀。
实验4:向稀硫酸酸化的 ,溶液中滴加
,溶液中滴加 溶液至溶液褪色。
溶液至溶液褪色。
已知室温下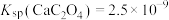 ,下列说法错误的是_______;
,下列说法错误的是_______;
(4)工业上利用硫酸亚铁与草酸反应制备草酸亚铁晶体,其离子方程式为: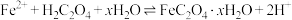 。
。
①制备时需添加氨水以提高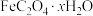 的产率,从化学平衡移动角度解释原因
的产率,从化学平衡移动角度解释原因_______ :
②测定草酸亚铁晶体(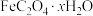 )的x值,实验如下:
)的x值,实验如下:
称取0.5400 g草酸亚铁晶体溶于一定浓度的硫酸中,用酸性 溶液漓定。到达滴定终点时,消耗0.1000 mol·L
溶液漓定。到达滴定终点时,消耗0.1000 mol·L 的酸性
的酸性 溶液18.00 mL。
溶液18.00 mL。
则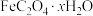 中
中
_______ ( 的摩尔质量是144 g⋅mol
的摩尔质量是144 g⋅mol )。
)。
 、
、 、
、 的物质的量浓度分数δ(X)[
的物质的量浓度分数δ(X)[ ]与pH的关系如图所示:
]与pH的关系如图所示:
请回答下列问题:
(1)室温下,草酸的一级电离常数
 为
为(2)①向草酸溶液中滴加KOH溶液至
 的过程中主要反应的离子方程式为
的过程中主要反应的离子方程式为②0.1 moL

 溶液中,
溶液中,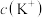
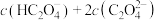 (填“>”、“<”或“=”);
(填“>”、“<”或“=”);(3)室温下,通过下列实验探究0.0100 mol⋅L

 溶液的性质:
溶液的性质:实验1:实验测得0.0100 mol⋅L

 溶液的pH为8.6。
溶液的pH为8.6。实验2:向溶液中滴加等体积、0.0100 mol⋅L
 HCl溶液。pH由8.6降为4.8。
HCl溶液。pH由8.6降为4.8。实验3:向溶液中加入等体积0.0200 mol⋅L

 溶液,出现白色沉淀。
溶液,出现白色沉淀。实验4:向稀硫酸酸化的
 ,溶液中滴加
,溶液中滴加 溶液至溶液褪色。
溶液至溶液褪色。已知室温下
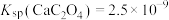 ,下列说法错误的是_______;
,下列说法错误的是_______;A.0.0100 mol⋅L  溶液中满足: 溶液中满足: |
B.实验2滴加盐酸过程中不可能存在: |
C.实验3所得上层清液中: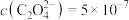 mol⋅L mol⋅L |
D.实验4发生反应的离子方程式为 |
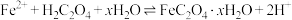 。
。①制备时需添加氨水以提高
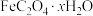 的产率,从化学平衡移动角度解释原因
的产率,从化学平衡移动角度解释原因②测定草酸亚铁晶体(
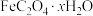 )的x值,实验如下:
)的x值,实验如下:称取0.5400 g草酸亚铁晶体溶于一定浓度的硫酸中,用酸性
 溶液漓定。到达滴定终点时,消耗0.1000 mol·L
溶液漓定。到达滴定终点时,消耗0.1000 mol·L 的酸性
的酸性 溶液18.00 mL。
溶液18.00 mL。则
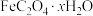 中
中
 的摩尔质量是144 g⋅mol
的摩尔质量是144 g⋅mol )。
)。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】碱式碳酸铜可用作有机催化剂。工业上以辉铜矿(主要成分为 ,含
,含 及少量
及少量 )为原料制备碱式碳酸铜,工业流程如下:
)为原料制备碱式碳酸铜,工业流程如下:
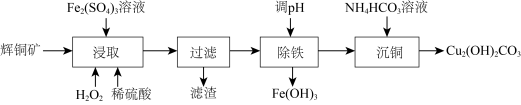
(1)滤渣可能含S、___________ (填化学式)。
(2)①“浸取”时能提高辉铜矿Cu浸取率的措施有___________ (填2条)。
②某小组测得Cu浸取率随 浓度及温度影响的变化曲线如下:
浓度及温度影响的变化曲线如下:

a.由图一可知 适宜的浓度范围为
适宜的浓度范围为___________ ;由图一中的a点分析,浸取时 也起到了氧化辉铜矿的作用,该反应的离子方程式为
也起到了氧化辉铜矿的作用,该反应的离子方程式为___________ 。
b.图二中高于85℃时Cu浸取率下降的原因是___________ 。
(3)“除铁”步骤调pH可加入试剂___________ (填选项字母);
a.氨气 b. c.
c. d.
d.
(4)常温下,“过滤”后的滤液中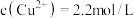 ,则“除铁”步骤调pH应小于
,则“除铁”步骤调pH应小于___________ 。[常温下, ]。
]。
 ,含
,含 及少量
及少量 )为原料制备碱式碳酸铜,工业流程如下:
)为原料制备碱式碳酸铜,工业流程如下:
(1)滤渣可能含S、
(2)①“浸取”时能提高辉铜矿Cu浸取率的措施有
②某小组测得Cu浸取率随
 浓度及温度影响的变化曲线如下:
浓度及温度影响的变化曲线如下:
a.由图一可知
 适宜的浓度范围为
适宜的浓度范围为 也起到了氧化辉铜矿的作用,该反应的离子方程式为
也起到了氧化辉铜矿的作用,该反应的离子方程式为b.图二中高于85℃时Cu浸取率下降的原因是
(3)“除铁”步骤调pH可加入试剂
a.氨气 b.
 c.
c. d.
d.
(4)常温下,“过滤”后的滤液中
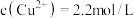 ,则“除铁”步骤调pH应小于
,则“除铁”步骤调pH应小于 ]。
]。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】氮氧化物是评价空气质量的控制标准之一,作为空气污染物的氮氧化物(NOx)常指NO和NO2。
(1)下列关于氮氧化物有关叙述不正确的是:_______ (填序号)
①对人体及动物有毒害作用; ②造成土壤污染;③一氧化氮可结合血红蛋白造成人体缺氧;④是形成酸雨、酸雾的主要原因之一; ⑤增高大气温度; ⑥与碳氢化合物形成光化学烟雾; ⑦参与臭氧层的破坏;⑧一氧化氮分子作为一种传递神经信息的 信使分子 ,在使血管扩张,免疫,增强记忆力
(2)用CH4催化还原NOx可在一定程度上消除氮氧化物的污染。
已知:CH4(g)+4NO(g) 2N2(g)+CO2(g)+2H2O(g)的ΔH=-1160kJ·mol-1
2N2(g)+CO2(g)+2H2O(g)的ΔH=-1160kJ·mol-1
2NO2(g)+N2(g) ⇌4NO(g) ΔH=+293 kJ·mol-1
则该条件下,CH4催化还原NO2消除污染的热化学方程式为_______________ 。
(3)T1℃时,在刚性反应器中以投料比为1:3的NO(g)与O2(g)反应,其中NO2二聚为N2O4的反应可以迅速达到平衡。体系的总压强p随时间t的变化如下表所示[t=∞时,NO(g)完全反应]。
①NO(g)与O2(g)合成的反应速率v=4.2×10-2×p2(NO)×p(O2)(kPa·min-1),t=42 min时,测得体系中p(O2)=22.4 kPa,则此时的v=_________ kPa·min-1(计算结果保留1位小数)。
②若降低反应温度至T2℃,则NO(g)与O2(g)完全反应后体系压强p∞(T2℃)_________ (填“大于”“等于”或“小于”)26.9kPa,原因是___________________________________ 。
③T1℃时,反应N2O4(g) ⇌ 2NO2(g)的平衡常数Kp=___ kPa(Kp为以分压表示的平衡常数,是指平衡时体系中生成气体压强幂之积与反应物气体压强幂之积的比值。计算结果保留3位小数)。
(4)铈元素(Ce)是镧系金属中自然丰度最高的一种,常见有+3、+4两种价态。雾霾中含有大量的污染物NO,可以被含Ce4+的溶液吸收,生成NO2-、NO3-(两者物质的量之比为1:1)。可采用电解法将上述吸收液中的NO2-转化为无毒物质,同时再生Ce4+,其原理如图所示。

①Ce4+从电解槽的_____ (填字母代号)口流出。
②写出阴极的电极反应式:______________ 。
(1)下列关于氮氧化物有关叙述不正确的是:
①对人体及动物有毒害作用; ②造成土壤污染;③一氧化氮可结合血红蛋白造成人体缺氧;④是形成酸雨、酸雾的主要原因之一; ⑤增高大气温度; ⑥与碳氢化合物形成光化学烟雾; ⑦参与臭氧层的破坏;⑧一氧化氮分子作为一种传递神经信息的 信使分子 ,在使血管扩张,免疫,增强记忆力
(2)用CH4催化还原NOx可在一定程度上消除氮氧化物的污染。
已知:CH4(g)+4NO(g)
 2N2(g)+CO2(g)+2H2O(g)的ΔH=-1160kJ·mol-1
2N2(g)+CO2(g)+2H2O(g)的ΔH=-1160kJ·mol-12NO2(g)+N2(g) ⇌4NO(g) ΔH=+293 kJ·mol-1
则该条件下,CH4催化还原NO2消除污染的热化学方程式为
(3)T1℃时,在刚性反应器中以投料比为1:3的NO(g)与O2(g)反应,其中NO2二聚为N2O4的反应可以迅速达到平衡。体系的总压强p随时间t的变化如下表所示[t=∞时,NO(g)完全反应]。
| t/min | 0 | 40 | 80 | 160 | 260 | 700 | ∞ |
| p/kPa | 32.8 | 30.7 | 29.9 | 29.4 | 29.2 | 28.8 | 26.9 |
②若降低反应温度至T2℃,则NO(g)与O2(g)完全反应后体系压强p∞(T2℃)
③T1℃时,反应N2O4(g) ⇌ 2NO2(g)的平衡常数Kp=
(4)铈元素(Ce)是镧系金属中自然丰度最高的一种,常见有+3、+4两种价态。雾霾中含有大量的污染物NO,可以被含Ce4+的溶液吸收,生成NO2-、NO3-(两者物质的量之比为1:1)。可采用电解法将上述吸收液中的NO2-转化为无毒物质,同时再生Ce4+,其原理如图所示。

①Ce4+从电解槽的
②写出阴极的电极反应式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】为迎接江苏省2021年首届中学生实验操作大赛,某校化学研究性学习小组在研究用石墨电极电解氯化铜溶液时,查阅资料得知,CuCl 显黄色,氯化铜溶液显蓝绿色或黄绿色;浓度分别为0.01mol/L、0.05mol/L、0.10mol/L、0.50mol/L的氯化铜溶液中加入NaCl至饱和,对比发现,溶液的颜色由黄绿色向蓝绿色转变。
显黄色,氯化铜溶液显蓝绿色或黄绿色;浓度分别为0.01mol/L、0.05mol/L、0.10mol/L、0.50mol/L的氯化铜溶液中加入NaCl至饱和,对比发现,溶液的颜色由黄绿色向蓝绿色转变。_______ 色,检验该气体可用_______ 。
(2)写出电解的离子方程式_______ 。
(3)实验中,装置的阴极溶液颜色由蓝绿色变为黄绿色,原因是_______ 。
(4)取出阴极的石墨棒,发现表面由浅蓝色固体,试设计实验探究此浅蓝色固体:_______ 。
(5)为什么要设计连接后面的装置_______ 。
 显黄色,氯化铜溶液显蓝绿色或黄绿色;浓度分别为0.01mol/L、0.05mol/L、0.10mol/L、0.50mol/L的氯化铜溶液中加入NaCl至饱和,对比发现,溶液的颜色由黄绿色向蓝绿色转变。
显黄色,氯化铜溶液显蓝绿色或黄绿色;浓度分别为0.01mol/L、0.05mol/L、0.10mol/L、0.50mol/L的氯化铜溶液中加入NaCl至饱和,对比发现,溶液的颜色由黄绿色向蓝绿色转变。
(2)写出电解的离子方程式
(3)实验中,装置的阴极溶液颜色由蓝绿色变为黄绿色,原因是
(4)取出阴极的石墨棒,发现表面由浅蓝色固体,试设计实验探究此浅蓝色固体:
(5)为什么要设计连接后面的装置
您最近一年使用:0次
【推荐3】氨气是生产化肥、硝酸等的重要原料,围绕合成氨,人们进行了一系列研究。
(1)①已知,氨的分解反应:2NH3(g) N2(g)+3H2(g)的活化能 Ea =600 kJ/mol,合成氨有关化学键的键能如下表:
N2(g)+3H2(g)的活化能 Ea =600 kJ/mol,合成氨有关化学键的键能如下表:
则合成氨反应: N2(g)+
N2(g)+ H2
H2 NH3(g)的活化能Ea=
NH3(g)的活化能Ea=___________ 。
②CO对合成氨的催化剂有毒害作用,常用乙酸二氨合铜(I)溶液来吸收原料气中的CO,反应原理为:[Cu(NH3)2CH3COO](1)+CO(g)+NH3(g) [Cu(NH3)3]CH3COO·CO(1) △H<0。吸收CO后的乙酸铜氨溶液经过适当的处理后又可以再生,恢复其吸收CO的能力,则再生过程的适宜条件是
[Cu(NH3)3]CH3COO·CO(1) △H<0。吸收CO后的乙酸铜氨溶液经过适当的处理后又可以再生,恢复其吸收CO的能力,则再生过程的适宜条件是___________ 。
A.高温高压 B.高温低压 C.低温低压 D.低温高压
③体积为1 L的恒温密闭容器中按照甲、乙、丙三种方式投料,发生反应:N2(g)+3H2(g) 2NH3(g),测得甲容器中H2的平衡转化率为50%
2NH3(g),测得甲容器中H2的平衡转化率为50%
平衡常数可用气体分压来表示,即K的表达式中用平衡分压代替平衡浓度,分压=总压×物质的量分数(例如: P(H2)=P总×x(H2)。该反应的平衡常数Kp=___________ (用P总和各气体的物质的量分数来表示)。乙容器中在投料时的正反应速率与逆反应速率的关系为v(正)___________ v(逆) (填“<”、“>” 、“=”)。
(2)NCl3可用来制备ClO2,实验室以NH4Cl、盐酸、NaClO2 (亚氯酸钠)为原料制备ClO2的流程如下:

写出电解过程中阳极的电极反应式:___________ 。
(1)①已知,氨的分解反应:2NH3(g)
 N2(g)+3H2(g)的活化能 Ea =600 kJ/mol,合成氨有关化学键的键能如下表:
N2(g)+3H2(g)的活化能 Ea =600 kJ/mol,合成氨有关化学键的键能如下表:| 化学键 | H-H | N≡N | N-H |
| E/ kJ· mol-1 | 436 | 946 | 391 |
则合成氨反应:
 N2(g)+
N2(g)+ H2
H2 NH3(g)的活化能Ea=
NH3(g)的活化能Ea=②CO对合成氨的催化剂有毒害作用,常用乙酸二氨合铜(I)溶液来吸收原料气中的CO,反应原理为:[Cu(NH3)2CH3COO](1)+CO(g)+NH3(g)
 [Cu(NH3)3]CH3COO·CO(1) △H<0。吸收CO后的乙酸铜氨溶液经过适当的处理后又可以再生,恢复其吸收CO的能力,则再生过程的适宜条件是
[Cu(NH3)3]CH3COO·CO(1) △H<0。吸收CO后的乙酸铜氨溶液经过适当的处理后又可以再生,恢复其吸收CO的能力,则再生过程的适宜条件是A.高温高压 B.高温低压 C.低温低压 D.低温高压
③体积为1 L的恒温密闭容器中按照甲、乙、丙三种方式投料,发生反应:N2(g)+3H2(g)
 2NH3(g),测得甲容器中H2的平衡转化率为50%
2NH3(g),测得甲容器中H2的平衡转化率为50%| mol | N2 | H2 | NH3 |
| 甲 | 1 | 3 | 0 |
| 乙 | 0.5 | 1 | 1 |
| 丙 | 0 | 0 | 4 |
平衡常数可用气体分压来表示,即K的表达式中用平衡分压代替平衡浓度,分压=总压×物质的量分数(例如: P(H2)=P总×x(H2)。该反应的平衡常数Kp=
(2)NCl3可用来制备ClO2,实验室以NH4Cl、盐酸、NaClO2 (亚氯酸钠)为原料制备ClO2的流程如下:

写出电解过程中阳极的电极反应式:
您最近一年使用:0次



