三位化学家因研究锂电池做出开创性贡献而获得2019年诺贝尔化学奖。磷酸亚铁锂(LiFePO4)可用作锂离子电池正极材料,具有热稳定性好、循环性能优良、安全性高等特点;成为目前广泛使用的锂电池。
(1)铁元素在元素周期表中的位置__ ;LiFePO4中Fe2+基态电子排布式是__ 。
(2)P的电负性___ O的电负性(填写“大于”“小于”或“等于”);PO43-的空间构型是__ ,中心原子的杂化方式是___ 。
(3)Li+与H-具有相同的电子构型,r(Li+)小于r(H-),原因是__ 。
(4)FeCl3中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在的FeCl3的结构式为__ ,其中Fe的配位数为__ 。
(5)有一种蓝色晶体[可表示为:KFex(CN)6,相对分子质量为Mr],经研究发现,其晶胞的 如图所示(K+未画出)。
如图所示(K+未画出)。
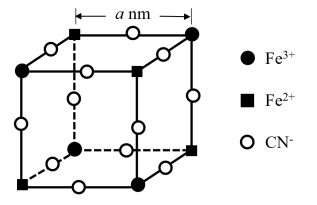
①晶体中与每个Fe3+距离最近且等距离的CN-有__ 个。
②该晶体的化学式为__ 。
③若晶胞中每个Fe3+和Fe2+距离用anm表示,则晶体的密度表达式是__ g/cm3。
(1)铁元素在元素周期表中的位置
(2)P的电负性
(3)Li+与H-具有相同的电子构型,r(Li+)小于r(H-),原因是
(4)FeCl3中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在的FeCl3的结构式为
(5)有一种蓝色晶体[可表示为:KFex(CN)6,相对分子质量为Mr],经研究发现,其晶胞的
 如图所示(K+未画出)。
如图所示(K+未画出)。
①晶体中与每个Fe3+距离最近且等距离的CN-有
②该晶体的化学式为
③若晶胞中每个Fe3+和Fe2+距离用anm表示,则晶体的密度表达式是
更新时间:2020-02-26 16:18:52
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】近日,济南大学原长洲教授制备了一种高性能的钾离子电池负极材料(Bi-MOF),反应可简单表示为Bi(NO3)3·5H2O+BTC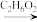 Bi–MOF。回答下列问题:
Bi–MOF。回答下列问题:
(1)铋(Bi)位于元素周期表中第6周期VA族,基态Bi原子的价层电子排布式为___________ 。Bi(NO3)3中阴离子的立体构型为___________ 。基态O原子核外成对电子数与未成对电子数之比为___________ 。
(2)BTC分子中组成元素C、N、O的电负性由大到小排序为___________ 。
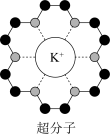
(3)冠醚是皇冠状的分子,可用不同大小的空穴适配不同大小的碱金属离子。18-冠-6(18指C、O原子总数为18,6指氧原子数)与钾离子形成的超分子结构如图所示。
①冠醚分子中C原子的杂化类型为___________ 。
②下列叙述正确的是___________ (填字母)。
A.含该超分子的物质属于分子晶体
B.冠醚可用于分离不同的碱金属离子
C.中心碱金属离子的配位数固定不变
D.冠醚与碱金属离子之间形成离子键
(4)铋的相关晶胞如图所示。___________ 。
②已知乙晶胞底边长为acm,高为bcm,NA为阿伏加德罗常数的值。该晶体密度___________ g·cm-3(只列计算式)。
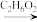 Bi–MOF。回答下列问题:
Bi–MOF。回答下列问题:(1)铋(Bi)位于元素周期表中第6周期VA族,基态Bi原子的价层电子排布式为
(2)BTC分子中组成元素C、N、O的电负性由大到小排序为
(3)冠醚是皇冠状的分子,可用不同大小的空穴适配不同大小的碱金属离子。18-冠-6(18指C、O原子总数为18,6指氧原子数)与钾离子形成的超分子结构如图所示。
①冠醚分子中C原子的杂化类型为
②下列叙述正确的是
A.含该超分子的物质属于分子晶体
B.冠醚可用于分离不同的碱金属离子
C.中心碱金属离子的配位数固定不变
D.冠醚与碱金属离子之间形成离子键
(4)铋的相关晶胞如图所示。
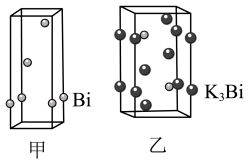
②已知乙晶胞底边长为acm,高为bcm,NA为阿伏加德罗常数的值。该晶体密度
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】[化学——选修3:物质结构与性质]
具有自主知识产权、中国制造的C919,是一款与波音737MAX同等体量的民用飞机。制造C919需要大量的合金材料,其中包括钢,钢是现代社会的物质基础,钢中除含有铁外还含有碳和少量不可避免的硅、锰、磷、硫等元素。请回答下列有关问题:
(1)基态Mn原子的价电子排布式为___________ 。
(2)NO3-的立体构型名称为___________ ,其中心原子的杂化方式为___________ 。
(3)C、O、Si三种元素第一电离能由大到小的顺序是___________ 。
(4)写出和CN-互为等电子体的一种离子的电子式___________ 。
(5)铵盐大多易分解,NH4F和NH4Br两种盐中较易分解的是___________ (填化学式);理由是___________ 。
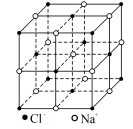
(6)氧化亚铁晶胞与NaCl的相似,NaCl的晶胞如图所示。由于晶体缺陷,某氧化亚铁晶体的实际组成为Fe0.9O,其中包含有Fe2+和Fe3+,晶胞边长为apm,该晶体的密度为ρg·cm-3,则a=___________ (列出计算式即可,用NA表示阿伏伽德罗常数的值)。
具有自主知识产权、中国制造的C919,是一款与波音737MAX同等体量的民用飞机。制造C919需要大量的合金材料,其中包括钢,钢是现代社会的物质基础,钢中除含有铁外还含有碳和少量不可避免的硅、锰、磷、硫等元素。请回答下列有关问题:
(1)基态Mn原子的价电子排布式为
(2)NO3-的立体构型名称为
(3)C、O、Si三种元素第一电离能由大到小的顺序是
(4)写出和CN-互为等电子体的一种离子的电子式
(5)铵盐大多易分解,NH4F和NH4Br两种盐中较易分解的是
(6)氧化亚铁晶胞与NaCl的相似,NaCl的晶胞如图所示。由于晶体缺陷,某氧化亚铁晶体的实际组成为Fe0.9O,其中包含有Fe2+和Fe3+,晶胞边长为apm,该晶体的密度为ρg·cm-3,则a=

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】物质结构决定物质的性质,物质的性质反映物质结构。
(1)BCl3、NCl3发生水解反应化学方程式如下:
BCl3+ 3 H2O = B(OH)3 + 3 HCl
NCl3+ 3 H2O = NH3 +3 HClO
分析上述反应,判断B、N、Cl三种元素的电负性由大到小的顺序是_________ 。上述反应所含的微粒中,呈三角锥形的是_____________ (填化学式)。
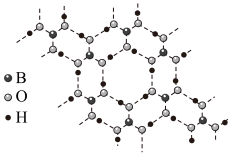
(2)BN是一种新型无机非金属材料,熔点很高、硬度很大,晶胞结构如图所示。BN晶体中存在的作用力有____(填字母编号)。

(3)B(OH)3晶体结构如图所示。晶体中B原子的轨道杂化方式是________ ;B(OH)3可能具有的性质是________ (填字母编号)。
A.熔化状态下能导电 B.熔点很高
C.能形成[B(OH)4]— D.硬度很大
(4)还原铁粉可作为合成氨的触媒。基态Fe原子的核外有________ 个未成对电子。从原子结构的角度分析,二价铁易被氧化为三价铁的原因是________ 。
(1)BCl3、NCl3发生水解反应化学方程式如下:
BCl3+ 3 H2O = B(OH)3 + 3 HCl
NCl3+ 3 H2O = NH3 +3 HClO
分析上述反应,判断B、N、Cl三种元素的电负性由大到小的顺序是
(2)BN是一种新型无机非金属材料,熔点很高、硬度很大,晶胞结构如图所示。BN晶体中存在的作用力有____(填字母编号)。

| A.σ键 | B.π键 | C.配位键 | D.分子间作用力 |

A.熔化状态下能导电 B.熔点很高
C.能形成[B(OH)4]— D.硬度很大
(4)还原铁粉可作为合成氨的触媒。基态Fe原子的核外有
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】含氮化合物在生活中应用十分广泛。神舟飞船外壳使用了氮化硅新型陶瓷结构材料,该材料硬度大、耐磨损。可用石英与焦炭在1400~1450℃的氮气气氛下合成氮化硅,同时生成一种与氮气结构相似的气态分子。
(1)写出上述反应的化学方程式____________________________________ 。反应原料中涉及的元素电负性由大到小的排列顺序为________________________________ 。
(2)基态氮原子中的原子轨道形状有_______________ 种。
(3)某同学画出了硅原子基态的核外电子排布图如下图,该电子排布违背了______ 原理。

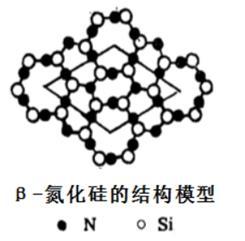
(4)氮化硅有多种型体,其中β-氮化硅层状结构模型如图,以图中所示的平行四边形为基本重复单元无限伸展,则该基本单元中含氮原子______ 个,硅原子______ 个。
(5)含氮的有机化合物氨基乙酸H2NCH2COOH中的碳原子杂化方式有____________ ,σ与π键的个数比为_______________ 。
(6)氨分子是一种常见的配体。Cu2+离子在水溶液中以[Cu(H2O)4]2+形式存在,向含Cu2+离子的溶液中加入足量氨水,可生成更稳定的[Cu(NH3)4]2+离子,其原因是_____ 。某配合物的化学式为CoCl3·4NH3,内界为正八面体构型配离子。0.1 mol该化合物溶于水中,加入过量AgNO3,有14.35g白色沉淀生成。则它的中心离子价电子排布式为____________ ,内界可能的结构有__________ 种。
(1)写出上述反应的化学方程式
(2)基态氮原子中的原子轨道形状有
(3)某同学画出了硅原子基态的核外电子排布图如下图,该电子排布违背了


(4)氮化硅有多种型体,其中β-氮化硅层状结构模型如图,以图中所示的平行四边形为基本重复单元无限伸展,则该基本单元中含氮原子
(5)含氮的有机化合物氨基乙酸H2NCH2COOH中的碳原子杂化方式有
(6)氨分子是一种常见的配体。Cu2+离子在水溶液中以[Cu(H2O)4]2+形式存在,向含Cu2+离子的溶液中加入足量氨水,可生成更稳定的[Cu(NH3)4]2+离子,其原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】黄铜矿(主要成分为CuFeS2)是一种天然矿石。中国在商代就掌握了利用黄铜矿冶炼铜的技术。医药上,黄铜矿有促进骨折愈合的作用。请回答下列问题:
(1)基态Cu+比Cu2+稳定的原因是___________ 。
(2) 的空间结构为
的空间结构为___________ 。
(3)某阳离子的结构如图所示,加热时该离子先失去的配位体是___________ (填化学式),原因是___________ 。

(4)四方晶系的CuFeS2晶胞结构如图所示。
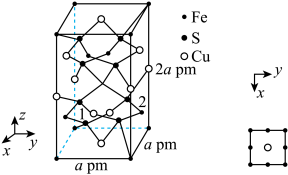
①晶胞中S原子的杂化方式为___________ 。
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标,例如图中原子1的分数坐标为( ,
, ,
, ),则原子2的分数坐标为
),则原子2的分数坐标为___________ 。
(1)基态Cu+比Cu2+稳定的原因是
(2)
 的空间结构为
的空间结构为(3)某阳离子的结构如图所示,加热时该离子先失去的配位体是

(4)四方晶系的CuFeS2晶胞结构如图所示。

①晶胞中S原子的杂化方式为
②以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标,例如图中原子1的分数坐标为(
 ,
, ,
, ),则原子2的分数坐标为
),则原子2的分数坐标为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】揖选做题铱本题包括A、B两小题,请选定其中一小题,并在相应的答题区域内作答。若多做,则按A小题评分。
A.[物质结构与性质]
一项科学研究成果表明,铜锰氧化物(CuMn2O4)能在常温下催化氧化空气中的一氧化碳和甲醛(HCHO)。
(1)向一定物质的量浓度的Cu(NO3)2和Mn(NO3)2溶液中加入Na2CO3溶液,所得沉淀经高温灼烧,可制得CuMn2O4。
①Mn2+基态的电子排布式可表示为______________________ 。
②NO3-的空间构型是_____________________ (用文字描述)。
(2)在铜锰氧化物的催化下,CO被氧化为CO2,HCHO被氧化为CO2和H2O。
①根据等电子体原理,CO分子的结构式为_____________________ 。
②H2O分子中O原子轨道的杂化类型为_____________________ 。
③1 mol CO2中含有的σ键数目为_____________________ 。
(3)向CuSO4溶液中加入过量NaOH溶液可生成[Cu (OH)4]2-。不考虑空间构型,[Cu(OH)4]2-的结构可用示意图表示为_____________________ 。
A.[物质结构与性质]
一项科学研究成果表明,铜锰氧化物(CuMn2O4)能在常温下催化氧化空气中的一氧化碳和甲醛(HCHO)。
(1)向一定物质的量浓度的Cu(NO3)2和Mn(NO3)2溶液中加入Na2CO3溶液,所得沉淀经高温灼烧,可制得CuMn2O4。
①Mn2+基态的电子排布式可表示为
②NO3-的空间构型是
(2)在铜锰氧化物的催化下,CO被氧化为CO2,HCHO被氧化为CO2和H2O。
①根据等电子体原理,CO分子的结构式为
②H2O分子中O原子轨道的杂化类型为
③1 mol CO2中含有的σ键数目为
(3)向CuSO4溶液中加入过量NaOH溶液可生成[Cu (OH)4]2-。不考虑空间构型,[Cu(OH)4]2-的结构可用示意图表示为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】铁是日常生活中最常见的金属,铁制品的使用在人类历史发展中起到了重要作用。回答下列问题:
(1)磺基水杨酸离子与 可以生成系列配合物
可以生成系列配合物 。加入
。加入 调节溶液的
调节溶液的 ,生成
,生成 的红褐色配合物
的红褐色配合物 。
。

①硫元素位于元素周期表中___________ 区,基态硫原子电子排布式为___________ ,磺基水杨酸分子中所含元素电负性由大到小的顺序为___________ 。
②依据原子轨道重叠的方式,判断 中的
中的 键属于
键属于___________ 键,该键是氢原子的 轨道和氧原子的
轨道和氧原子的___________ 轨道重叠形成的, 的VSEPR构型为
的VSEPR构型为___________ 。
③羧酸根( )中羧基
)中羧基 和两个
和两个 之间形成大
之间形成大 键,负电荷是平均分布在这个离域体系上。配合物
键,负电荷是平均分布在这个离域体系上。配合物 中含有两个六元环,在形成配合物
中含有两个六元环,在形成配合物 时,能提供电子对形成配位键的原子是
时,能提供电子对形成配位键的原子是___________ (填标号)。
(2)下表是 逐级失去电子的电离能,
逐级失去电子的电离能, 明显大于
明显大于 ,从原子结构角度解释其原因为
,从原子结构角度解释其原因为___________ 。
(3)已知 晶体的晶胞结构为
晶体的晶胞结构为 型(如图所示),晶胞边长为
型(如图所示),晶胞边长为 ,
, 表示阿伏加德罗常数的值。该晶体中铁离子占据空隙的几何形状(即与铁离子距离最近且等距离的
表示阿伏加德罗常数的值。该晶体中铁离子占据空隙的几何形状(即与铁离子距离最近且等距离的 围成的空间形状)是
围成的空间形状)是___________ ,晶体密度为___________  。
。

(1)磺基水杨酸离子与
 可以生成系列配合物
可以生成系列配合物 。加入
。加入 调节溶液的
调节溶液的 ,生成
,生成 的红褐色配合物
的红褐色配合物 。
。
①硫元素位于元素周期表中
②依据原子轨道重叠的方式,判断
 中的
中的 键属于
键属于 轨道和氧原子的
轨道和氧原子的 的VSEPR构型为
的VSEPR构型为③羧酸根(
 )中羧基
)中羧基 和两个
和两个 之间形成大
之间形成大 键,负电荷是平均分布在这个离域体系上。配合物
键,负电荷是平均分布在这个离域体系上。配合物 中含有两个六元环,在形成配合物
中含有两个六元环,在形成配合物 时,能提供电子对形成配位键的原子是
时,能提供电子对形成配位键的原子是(2)下表是
 逐级失去电子的电离能,
逐级失去电子的电离能, 明显大于
明显大于 ,从原子结构角度解释其原因为
,从原子结构角度解释其原因为电离能( ) ) |  |  |  |  |
 | 762.5 | 1561.9 | 2957 | 5290 |
(3)已知
 晶体的晶胞结构为
晶体的晶胞结构为 型(如图所示),晶胞边长为
型(如图所示),晶胞边长为 ,
, 表示阿伏加德罗常数的值。该晶体中铁离子占据空隙的几何形状(即与铁离子距离最近且等距离的
表示阿伏加德罗常数的值。该晶体中铁离子占据空隙的几何形状(即与铁离子距离最近且等距离的 围成的空间形状)是
围成的空间形状)是 。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】铜及其化合物在科学研究和工农业生产中有许多用途。回答下列问题:
(1)[Cu(NH3)2]SO4溶液可以吸收合成氨中对催化剂有毒害的CO气体,反应的化学方程式为:[Cu(NH3)2]SO4+CO+NH3⇌[Cu(NH3)3CO]SO4
①基态Cu+的价层电子排布图为_______ 。
② 的空间结构为
的空间结构为_______ 。
③N、O和S的第一电离能由大到小的顺序是_______ (用元素符号表示)。
④[Cu(NH3)3CO]SO4晶体中存在的化学键类型有_______ (填字母)。
A.离子键 B.极性共价键 C.非极性共价键 D.氢键 E.配位键 F.π键
(2)Cu—Mn—Al合金为磁性形状记忆合金材料之一,其晶胞结构如图所示:
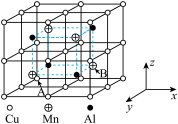
①该合金的化学式为_______ 。
②若A原子的坐标参数为(0,0,0),则B原子的坐标参数为_______ 。
③已知该合金晶体的密度为ρ g·cm-3,则最近的两个Cu原子间的距离为_______ nm(阿伏加德罗常数的值用NA表示)。
(1)[Cu(NH3)2]SO4溶液可以吸收合成氨中对催化剂有毒害的CO气体,反应的化学方程式为:[Cu(NH3)2]SO4+CO+NH3⇌[Cu(NH3)3CO]SO4
①基态Cu+的价层电子排布图为
②
 的空间结构为
的空间结构为③N、O和S的第一电离能由大到小的顺序是
④[Cu(NH3)3CO]SO4晶体中存在的化学键类型有
A.离子键 B.极性共价键 C.非极性共价键 D.氢键 E.配位键 F.π键
(2)Cu—Mn—Al合金为磁性形状记忆合金材料之一,其晶胞结构如图所示:

①该合金的化学式为
②若A原子的坐标参数为(0,0,0),则B原子的坐标参数为
③已知该合金晶体的密度为ρ g·cm-3,则最近的两个Cu原子间的距离为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题
(1)写出CO 的VSEPR模型名称
的VSEPR模型名称___________ ;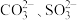 的中心原子上的孤电子对数分别是
的中心原子上的孤电子对数分别是___________ 、___________ 。
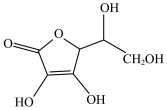
(2)抗坏血酸的分子结构如图所示,分子中碳原子的轨道杂化类型为___________ ;1mol该分子中π键数为___________ 。
(3)富马酸亚铁(FeC4H2O4)是一种补铁剂。富马酸分子的结构模型如图所示,富马酸分子中 键与
键与 键的数目比为
键的数目比为___________ 。

(4)已知,可用异氰酸苯酯与2—氯—4—氨基吡啶反应生成氯吡苯脲:

反应过程中,每生成 氯吡苯脲,断裂
氯吡苯脲,断裂___________  键,断裂
键,断裂___________ 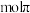 键;已知该2—氯—4—氨基分子中六元环结构与苯环相似,也存在大π键,可表示为
键;已知该2—氯—4—氨基分子中六元环结构与苯环相似,也存在大π键,可表示为___________ (写成π 的形式)
的形式)
(5)N2H 的电子式为
的电子式为___________ ,CH3NH 中N原子的
中N原子的___________ 杂化轨道与H的1s轨道形成σ键;CH3NH 中H-N-H键角比NH3中H-N-H键角
中H-N-H键角比NH3中H-N-H键角___________ (填“大”或“小”),理由是___________ 。
(1)写出CO
 的VSEPR模型名称
的VSEPR模型名称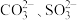 的中心原子上的孤电子对数分别是
的中心原子上的孤电子对数分别是(2)抗坏血酸的分子结构如图所示,分子中碳原子的轨道杂化类型为

(3)富马酸亚铁(FeC4H2O4)是一种补铁剂。富马酸分子的结构模型如图所示,富马酸分子中
 键与
键与 键的数目比为
键的数目比为
(4)已知,可用异氰酸苯酯与2—氯—4—氨基吡啶反应生成氯吡苯脲:

反应过程中,每生成
 氯吡苯脲,断裂
氯吡苯脲,断裂 键,断裂
键,断裂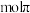 键;已知该2—氯—4—氨基分子中六元环结构与苯环相似,也存在大π键,可表示为
键;已知该2—氯—4—氨基分子中六元环结构与苯环相似,也存在大π键,可表示为 的形式)
的形式)(5)N2H
 的电子式为
的电子式为 中N原子的
中N原子的 中H-N-H键角比NH3中H-N-H键角
中H-N-H键角比NH3中H-N-H键角
您最近一年使用:0次
【推荐1】我国具有丰富的铜矿资源,请回答下列有关铜及其化合物的问题:
(1)请写出基态Cu原子的价电子排布式_________ 。焰火中的绿色是铜的焰色,基态铜原子在灼烧时价电子发生了_________ 而变为激发态。
(2)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电离能Il(Zn)______ Il(Cu)(填“大于”或“小于”),原因是___________ 。
(3)新型农药松脂酸铜具有低残留的特点,下图是松脂酸铜的结构简式:
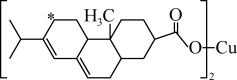
请分析1个松脂酸铜中π键的个数___________ 加“*”碳原子的杂化方式为_____________ 。
(4)硫酸铜溶于氨水形成 4深蓝色溶液。
4深蓝色溶液。
① 中阴离子的立体构型是
中阴离子的立体构型是_______ 。
②在 中
中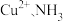 之间形成的化学键称为
之间形成的化学键称为_____ ,提供孤电子对的成键原子是_______________________ 。
③氨的沸点_________________ (填“高于”或“低于”)膦;
(5)黄铜合金可以表示为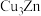 ,为面心立方晶胞,晶体密度为8.5
,为面心立方晶胞,晶体密度为8.5 ,求晶胞的边长
,求晶胞的边长___________ (只写计算式,不求结果)
(1)请写出基态Cu原子的价电子排布式
(2)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电离能Il(Zn)
(3)新型农药松脂酸铜具有低残留的特点,下图是松脂酸铜的结构简式:

请分析1个松脂酸铜中π键的个数
(4)硫酸铜溶于氨水形成
 4深蓝色溶液。
4深蓝色溶液。 ①
 中阴离子的立体构型是
中阴离子的立体构型是②在
 中
中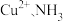 之间形成的化学键称为
之间形成的化学键称为③氨的沸点
(5)黄铜合金可以表示为
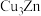 ,为面心立方晶胞,晶体密度为8.5
,为面心立方晶胞,晶体密度为8.5 ,求晶胞的边长
,求晶胞的边长
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】2019年诺贝尔化学奖授予约翰·B·古迪纳夫、M·斯坦利·威廷汉、吉野彰等三位科学家,以表彰他们在锂电池研究作出的卓越贡献。常用的锂电池一般用镍钴锰酸锂Li(NiCoMn)O2或磷酸铁锂(LiFePO4)等为正极材料。请回答下列问题:
(1)Ni在元素周期表的位置是_______ 区(填分区),基态Fe原子价电子的空间运动状态有_______ 种。
(2)1 mol配合物[Co(NH3)4Cl2]Cl含σ键数目为_______ NA。
(3)磷元素可以形成多种含氧酸H3PO4、H3PO2、H3PO3、HPO3,这四种酸中酸性最强的是_______ ,HPO3中心原子的杂化方式是_______ ,写出与 互为等电子体的离子
互为等电子体的离子_______ (写离子符号,任写两个)。
(4)硫化锂Li2S的纳米晶体是开发先进锂电池的关键材料,硫化锂的晶体为反萤石结构,其晶胞结构如图。若a处微粒的坐标是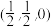 ,则b处微粒的坐标是
,则b处微粒的坐标是_______ ;S2-的配位数是_______ ;若硫化锂晶体的密度为ρ g·cm-3,则Li+与S2-的最短距离是_______ nm。(用含ρ、NA的计算式表示)。

(1)Ni在元素周期表的位置是
(2)1 mol配合物[Co(NH3)4Cl2]Cl含σ键数目为
(3)磷元素可以形成多种含氧酸H3PO4、H3PO2、H3PO3、HPO3,这四种酸中酸性最强的是
 互为等电子体的离子
互为等电子体的离子(4)硫化锂Li2S的纳米晶体是开发先进锂电池的关键材料,硫化锂的晶体为反萤石结构,其晶胞结构如图。若a处微粒的坐标是
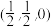 ,则b处微粒的坐标是
,则b处微粒的坐标是
您最近一年使用:0次
【推荐3】用含钴废料(主要成分为Co2O3,含少量Fe2O3、A12O3、CaO、MgO、碳及有机物等)制备草酸钴晶体(CoC2O4·2H2O)的工艺流程如图所示:
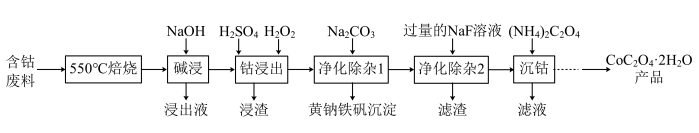
已知:ⅰ.金属钴与铁具有相似的化学性质
ⅱ.黄钠铁矾的化学式为Na2Fe6(SO4)4(OH)12
ⅲ.Ksp(MgF2)=6.25×10-9,Ksp(CaF2)=2.25×10-11
回答下列问题:
(1)550℃焙烧的目的是___________ 。
(2)“钴浸出”过程中,主要反应的离子方程式是___________ 。
(3)“净化除杂1”为生成黄钠铁矾沉淀,需加入Na2CO3溶液调节pH为2.5~3.0,控制pH在此范围的原因是___________ 。
(4)常温下,在“净化除杂2”中加入NaF溶液可除去Ca2+、Mg2+,当两者沉淀完全时,F-的浓度至少为___________ mol∙L-1(离子浓度小于1.0×10-5mol∙L-1即为该离子沉淀完全)。
(5)草酸钴晶体在空气中受热可得到Co3O4,该反应的化学方程式为___________ 。
(6)一种掺钴催化剂的晶胞如图所示,则该晶体沿z轴的投影图为___________ (填序号),设阿伏加德罗常数的值为NA,晶胞的密度为ρ ,则晶胞参数为
,则晶胞参数为___________ nm(用含ρ、NA的代数式表示)。


已知:ⅰ.金属钴与铁具有相似的化学性质
ⅱ.黄钠铁矾的化学式为Na2Fe6(SO4)4(OH)12
ⅲ.Ksp(MgF2)=6.25×10-9,Ksp(CaF2)=2.25×10-11
回答下列问题:
(1)550℃焙烧的目的是
(2)“钴浸出”过程中,主要反应的离子方程式是
(3)“净化除杂1”为生成黄钠铁矾沉淀,需加入Na2CO3溶液调节pH为2.5~3.0,控制pH在此范围的原因是
(4)常温下,在“净化除杂2”中加入NaF溶液可除去Ca2+、Mg2+,当两者沉淀完全时,F-的浓度至少为
(5)草酸钴晶体在空气中受热可得到Co3O4,该反应的化学方程式为
(6)一种掺钴催化剂的晶胞如图所示,则该晶体沿z轴的投影图为
 ,则晶胞参数为
,则晶胞参数为
您最近一年使用:0次



