在某H2SO4和Fe2(SO4)3的混合溶液中,测得H+的物质的量浓度为0.40mol/L,而SO42-的物质的量浓度为0.65mol/L,则混合液中Fe3+的物质的量浓度(mol/L)为
| A.0.10 | B.0.20 | C.0.30 | D.0.40 |
更新时间:2020/02/27 17:53:49
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】常温下,向一定浓度 溶液中加入
溶液中加入 固体,保持溶液体积和温度不变,测得
固体,保持溶液体积和温度不变,测得 与
与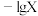 [X为
[X为 、
、 、
、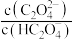 ]的变化关系如图所示。
]的变化关系如图所示。不正确 的是
 溶液中加入
溶液中加入 固体,保持溶液体积和温度不变,测得
固体,保持溶液体积和温度不变,测得 与
与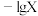 [X为
[X为 、
、 、
、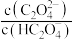 ]的变化关系如图所示。
]的变化关系如图所示。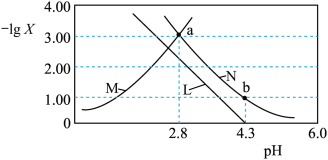
A.曲线M表示 随 随 的变化 的变化 |
| B.从a点至b点,水的电离程度逐渐减小 |
C.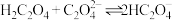 的化学平衡常数为 的化学平衡常数为 |
D.a点溶液中: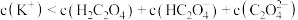 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】下表是25℃时某些盐的溶度积常数和弱酸的电离平衡常数。下列说法正确的是
| 化学式 | CH3COOH | H2CO3 | AgCl | Ag2CrO4 |
| Ka或Ksp | Ka=1.75×10-5 | Ka1=4.5×10-7 Ka2=4.7×10-11 | Ksp=1.8×10-10 | Ksp=2.0×10-12 |
A.常温下,相同浓度的①CH3COONH4、②NH4HCO3、③NH4HSO4溶液中,c(NH )由大到小的顺序是①>②>③ )由大到小的顺序是①>②>③ |
| B.向饱和氯水中滴加NaOH溶液至溶液刚好呈中性时,c(Na+)=2c(ClO-)+c(HClO) |
| C.AgCl在盐酸中的Ksp大于其在水中的Ksp |
D.向浓度均为1×10-3mol·L-1的KCl和K2CrO4的混合溶液中滴加1×10-3mol·L-1的AgNO3溶液, 先形成沉淀 先形成沉淀 |
您最近一年使用:0次



