根据下列图示所得出的结论正确的是( )
A.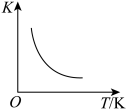 ,反应 ,反应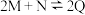 的平衡常数与温度的关系,说明该反应的 的平衡常数与温度的关系,说明该反应的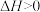 |
B.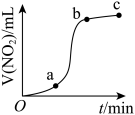 , , 与过量浓硝酸反应生成的 与过量浓硝酸反应生成的 气体体积随时间的变化关系,说明该反应在b→c时间段内反应速率最快 气体体积随时间的变化关系,说明该反应在b→c时间段内反应速率最快 |
C.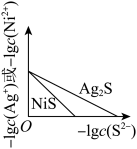 ,常温下 ,常温下 和 和 的沉淀溶解平衡曲线,若 的沉淀溶解平衡曲线,若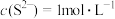 时,两者的 时,两者的 相等 相等 |
D.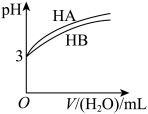 ,常温下 ,常温下 的 的 和 和 溶液分别加水稀释时 溶液分别加水稀释时 的变化曲线,说明两者的电离平衡常数 的变化曲线,说明两者的电离平衡常数 |
更新时间:2020-03-26 10:17:38
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】对于可逆反应A(s) +3B(g) 2C(g)△H>0,下列图像中符合真实变化的是
2C(g)△H>0,下列图像中符合真实变化的是
 2C(g)△H>0,下列图像中符合真实变化的是
2C(g)△H>0,下列图像中符合真实变化的是A. | B.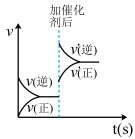 |
C. | D. |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】根据下列图示所得出的结论正确的是
A.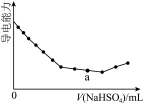 是Ba(OH)2溶液中滴加NaHSO4溶液之后,溶液的导电能力随滴入NaHSO4溶液体积变化的曲线,说明a点对应的溶液呈碱性 是Ba(OH)2溶液中滴加NaHSO4溶液之后,溶液的导电能力随滴入NaHSO4溶液体积变化的曲线,说明a点对应的溶液呈碱性 |
B. 表示某放热反应分别在有、无催化剂的情况下,反应过程中的能量变化 表示某放热反应分别在有、无催化剂的情况下,反应过程中的能量变化 |
C. 是I2+I-⇌I3-中I3-的平衡浓度随温度变化的曲线,说明平衡常数K(T1)<K(T2) 是I2+I-⇌I3-中I3-的平衡浓度随温度变化的曲线,说明平衡常数K(T1)<K(T2) |
D.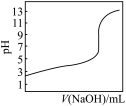 是室温下用0.1 mol·L-1 NaOH溶液滴定0.1 mol·L-1某酸HX的滴定曲线,说明可用甲基橙判断该反应的终点 是室温下用0.1 mol·L-1 NaOH溶液滴定0.1 mol·L-1某酸HX的滴定曲线,说明可用甲基橙判断该反应的终点 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】判断下列相关说法正确的是
A.密闭容器中反应aA(g)+bY(g) cZ(g)达到平衡,T0时改变某一条件变化如图 cZ(g)达到平衡,T0时改变某一条件变化如图 ,则改变的条件只能是加入催化剂 ,则改变的条件只能是加入催化剂 |
B.反应L(s)+aG(g) bR(g)达到平衡时,外界条件对平衡影响关系如图 bR(g)达到平衡时,外界条件对平衡影响关系如图 ,则正反应为放热反应,且a>b ,则正反应为放热反应,且a>b |
C.其它条件相同时,物质的量和温度关系如图所示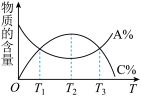 ,则反应aA+bB ,则反应aA+bB cC的正反应为放热反应 cC的正反应为放热反应 |
D.反应速率和反应条件变化关系如图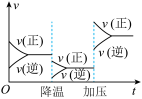 ,则反应A+2B ,则反应A+2B 2C+3D的正反应为放热反应,且A、B、C、D均为气体 2C+3D的正反应为放热反应,且A、B、C、D均为气体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】对于气相反应,某组分(B)的平衡压强(PB)代替物质的量浓度(c B)也可表示平衡常数(记作Kp).已知反应4NH3(g)+5O2(g)⇌4NO(g)+6H2O(g)在T℃的平衡常数Kp=a,则下列说法正确的是
| A.Kp=[4(NH3)P5(O2)]P4(NO)P6(H2O) |
| B.升高温度,若Kp增大,则该反应为吸热反应 |
| C.该反应达到平衡状态后,增大压强,平衡向左移动,Kp减小 |
| D.2NH3(g)+5/2O2(g)⇌2NO(g)+3H2O(g) 的平衡常数Kp=0.5a |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】温度为T1时,在三个容积均为1L的恒容密闭容器中仅发生反应:2NO2(g) 2NO(g)+O2(g)(正反应吸热)。实验测得:v正=v(NO2)消耗=k正c2(NO2),v逆=v(NO)消耗=2v(O2)消耗=k逆c2(NO)·c(O2),k正、k逆为速率常数,受温度影响。
2NO(g)+O2(g)(正反应吸热)。实验测得:v正=v(NO2)消耗=k正c2(NO2),v逆=v(NO)消耗=2v(O2)消耗=k逆c2(NO)·c(O2),k正、k逆为速率常数,受温度影响。
下列说法不正确的是
 2NO(g)+O2(g)(正反应吸热)。实验测得:v正=v(NO2)消耗=k正c2(NO2),v逆=v(NO)消耗=2v(O2)消耗=k逆c2(NO)·c(O2),k正、k逆为速率常数,受温度影响。
2NO(g)+O2(g)(正反应吸热)。实验测得:v正=v(NO2)消耗=k正c2(NO2),v逆=v(NO)消耗=2v(O2)消耗=k逆c2(NO)·c(O2),k正、k逆为速率常数,受温度影响。容器 编号 | 物质的起始浓度(mol·L-1) | 物质的平衡浓度(mol·L-1) | ||
c(NO2) | c(NO) | c(O2) | c(O2) | |
I | 0.6 | 0 | 0 | 0.2 |
II | 0.3 | 0.5 | 0.2 | |
III | 0 | 0.5 | 0.35 | |
| A.达平衡时,容器I与容器II中的总压强之比为4:5 |
| B.达平衡时,容器II中c(O2)/c(NO2)比容器I中的小 |
| C.达平衡时,容器III中NO的体积分数小于50% |
| D.当温度改变为T2时,若k正=k逆,则T2>T1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】相同温度下,在体积相等的三个恒容密闭容器中发生可逆反应:N2(g) + 3H2(g)  2NH3(g)△H=-92.4 kJ/mol。实验测得起始、平衡时的有关数据如下表:
2NH3(g)△H=-92.4 kJ/mol。实验测得起始、平衡时的有关数据如下表:
下列叙述正确的是
 2NH3(g)△H=-92.4 kJ/mol。实验测得起始、平衡时的有关数据如下表:
2NH3(g)△H=-92.4 kJ/mol。实验测得起始、平衡时的有关数据如下表:| 容器编号 | 起始时各物质物质的量/mol | 平衡时反应中的能量变化 | ||
| N2 | H2 | NH3 | ||
| ① | 1 | 3 | 0 | 放出热量a kJ |
| ② | 2 | 3 | 0 | 放出热量b kJ |
| ③ | 2 | 6 | 0 | 放出热量c kJ |
| A.放出热量关系:a < b <92.4 |
| B.三个容器内反应的平衡常数:③>①>② |
| C.达平衡时氨气的体积分数:①>③ |
| D.N2的转化率:②>①>③ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列叙述正确的是
| A.25℃时,NH4Cl溶液的KW大于100℃时NaCl溶液的KW |
| B.在蒸馏水中滴加浓H2SO4,KW不变 |
| C.CaCO3难溶于水,属于弱电解质 |
| D.pH=4的番茄汁中c(H+)是pH=6的牛奶中c(H+)的100倍 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】在25℃,草酸(HOOCCOOH)电离常数:Ka1=5.9×10-2,,Ka2=6.4×10-5。下列说法正确的是
| A.0.1mol•L-1HOOCCOOH溶液的pH<1 |
B.将Na2C2O4溶液加水稀释时, 将增大 将增大 |
C.0.1mol•L-1NaHC2O4溶液中:c(HC2O )>c(H2C2O4)>c(C2O )>c(H2C2O4)>c(C2O ) ) |
| D.向草酸溶液加入Na2CO3粉末,有CO2放出,说明草酸为弱酸 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】根据下列实验操作和现象所得到的结论不正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向浓度均为0.1 mol·L-1的NaCl和NaI混合溶液中滴加少量AgNO3溶液,先出现黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| B | 向苯酚浊液中加入Na2CO3溶液,溶液变澄清 | 酸性:苯酚>HCO |
| C | 用pH试纸测得:CH3COONa溶液的pH约为9,NaNO2溶液的pH约为8 | HNO2电离出H+的能力比CH3COOH的强 |
| D | 向NaAlO2溶液中滴加NaHCO3溶液,产生白色沉淀 | Al 结合H+的能力比C 结合H+的能力比C 强 强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】室温下,用0.01mol·L-1CuSO4溶液浸泡NiS固体,一段时间后过滤,向滤液中加入氨水,产生蓝色沉淀。已知Ksp(NiS)=1.0×10−21,Ksp(CuS)=1.5×10−36,Ksp(PbS)=9×10−29。下列有关说法正确的是
| A.过滤后所得溶液中存在:c(Ni2+)·c(S2−)<Ksp(NiS) |
| B.滤液中加入氨水产生蓝色沉淀的离子方程式:Cu2++2OH−=Cu(OH)2↓ |
C.欲使反应NiS + Cu2+ Ni2+ + CuS向右进行,则需满足 Ni2+ + CuS向右进行,则需满足 > > ×1015 ×1015 |
| D.用0.01 mol·L-1CuSO4溶液浸泡PbS固体,不能得到CuS固体 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列实验操作、现象及得出的结论均正确的是
| 选项 | 实验操作 | 实验现象 | 实验结论 |
| A | Cu片与足量浓硫酸加热反应,冷却后,再将冷水缓慢加入盛有反应混合物的烧杯中 | 溶液变蓝 | 证明反应生成了Cu2+ |
| B | 取少量某溶液于试管中,加入NaOH浓溶液并加热,用湿润的蓝色石蕊试纸检验产生的气体 | 蓝色石蕊试纸变红 | 溶液中含有NH4+ |
| C | 向20.00mL浓度均为0.01mol/L的Na2SO4和Na2S 的混合溶液中滴加几滴等浓度的AgNO3溶液 | 只产生黑色沉淀Ag2S | Ksp(Ag2S)<Ksp(Ag2SO4) |
| D | 室温下,用pH试纸分别测定浓度均为0.1mol/L的Na2SO3和Na2CO3两种溶液的pH | pH: Na2CO3>Na2SO3 | 非金属性:S>C |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

 的电离常数
的电离常数 增大的是
增大的是

