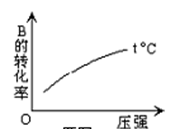
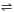在密闭容器中进行反应:2A(g)+B(g) 3C(g)+Q(Q>0)。下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是( )
3C(g)+Q(Q>0)。下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是( )
 3C(g)+Q(Q>0)。下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是( )
3C(g)+Q(Q>0)。下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是( )A.图I表示温度对化学平衡的影响,且甲的温度较高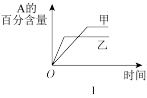 |
B.图Ⅱ表示t0时刻缩小容器体积对反应速率的影响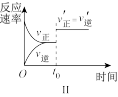 |
C.图Ⅲ表示t0时刻增大B浓度对反应速率的影响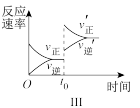 |
D.图Ⅳ中a、b、c三点中只有b点已经达到化学平衡状态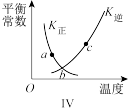 |
2013·上海黄浦·一模 查看更多[2]
更新时间:2020-03-30 15:07:02
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】学习“化学平衡移动原理”后,联系生产、生活,下列说法错误的是
| A.热的纯碱溶液比冷的纯碱溶液洗涤油污效果更好 |
| B.合成氨反应,为提高氨的产率,应采取高温高压的措施 |
| C.啤酒瓶开启后,马上泛起大量泡沫 |
| D.将一氧化碳中毒者放入高压氧舱,增大氧气浓度,利用平衡移动原理缓解病情 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】室温下,向3 mL0.1 mol/L稀盐酸中加入1 mL0.1mol/L氯化钴溶液发生反应: ,平衡时溶液呈浅紫色。下列说法不正确的是
,平衡时溶液呈浅紫色。下列说法不正确的是
 ,平衡时溶液呈浅紫色。下列说法不正确的是
,平衡时溶液呈浅紫色。下列说法不正确的是| A.加热,溶液会逐渐变成蓝色 |
| B.向溶液中加AgNO3,如果生成白色沉淀.说明该反应存在限度 |
| C.加入少量水,平衡会逆向移动 |
| D.加入NaCl固体,平衡右移,但平衡常数不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】一定条件下存在反应:CO(g)+H2O(g) CO2(g)+H2(g),其正反应放热。现有三个相同的2L恒容绝热(与外界没有热量交换)密闭容器I、II、III,在I中充入1molCO和1molH2O,在II中充入1molCO2和1mol H2,在III中充入2molCO和2molH2O,700℃条件下开始反应。达到平衡时,下列说法正确的是
CO2(g)+H2(g),其正反应放热。现有三个相同的2L恒容绝热(与外界没有热量交换)密闭容器I、II、III,在I中充入1molCO和1molH2O,在II中充入1molCO2和1mol H2,在III中充入2molCO和2molH2O,700℃条件下开始反应。达到平衡时,下列说法正确的是
 CO2(g)+H2(g),其正反应放热。现有三个相同的2L恒容绝热(与外界没有热量交换)密闭容器I、II、III,在I中充入1molCO和1molH2O,在II中充入1molCO2和1mol H2,在III中充入2molCO和2molH2O,700℃条件下开始反应。达到平衡时,下列说法正确的是
CO2(g)+H2(g),其正反应放热。现有三个相同的2L恒容绝热(与外界没有热量交换)密闭容器I、II、III,在I中充入1molCO和1molH2O,在II中充入1molCO2和1mol H2,在III中充入2molCO和2molH2O,700℃条件下开始反应。达到平衡时,下列说法正确的是| A.容器I、II中正反应速率相同 |
| B.容器I、III中反应的平衡常数相同 |
| C.容器I中CO的物质的量比容器II中的多 |
| D.容器I中CO的转化率与容器II中CO2的转化率之和等于1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
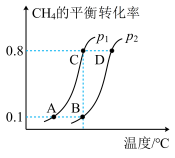
【推荐2】将2molCH4(g)和5molH2O(g)通入一密闭容器中,发生反应:CH4(g)+H2O(g) CO(g)+3H2(g)。CH4(g)的平衡转化率与温度、压强的关系如图所示,下列有关平衡常数的判断正确的是
CO(g)+3H2(g)。CH4(g)的平衡转化率与温度、压强的关系如图所示,下列有关平衡常数的判断正确的是
 CO(g)+3H2(g)。CH4(g)的平衡转化率与温度、压强的关系如图所示,下列有关平衡常数的判断正确的是
CO(g)+3H2(g)。CH4(g)的平衡转化率与温度、压强的关系如图所示,下列有关平衡常数的判断正确的是
| A.KA>KB=KC>KD |
| B.KA<KB= KC<KD |
| C.KA=KB>KC=KD |
| D.KA=KB<KC=KD |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】某可逆反应为2X(g) 3Y(g)+Z(g),混合气体中X的物质的量分数与温度关系如图所示:下列推断正确的是
3Y(g)+Z(g),混合气体中X的物质的量分数与温度关系如图所示:下列推断正确的是
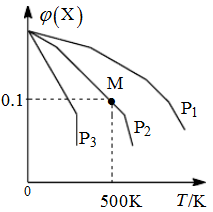
 3Y(g)+Z(g),混合气体中X的物质的量分数与温度关系如图所示:下列推断正确的是
3Y(g)+Z(g),混合气体中X的物质的量分数与温度关系如图所示:下列推断正确的是
| A.升高温度,该反应平衡常数K减小 |
| B.压强大小有P3>P2>P1 |
| C.平衡后加入高效催化剂使Mr(混合气体的平均相对分子质量)增大 |
D.在该条件下M点X平衡转化率为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】某化学研究小组探究外界条件(压强、温度)对化学反应 平衡的影响图象如图所示,下列判断正确的是( )
平衡的影响图象如图所示,下列判断正确的是( )
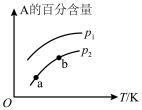
 平衡的影响图象如图所示,下列判断正确的是( )
平衡的影响图象如图所示,下列判断正确的是( )
| A.由图可知,该反应的正反应为吸热反应 |
B.由图可知,若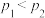 ,则该反应中 ,则该反应中 |
C.图中,点a和点b的反应速率大小为 |
| D.当反应达到平衡时,只加入催化剂,A的百分含量将发生变化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】T ℃时,A、B、C三种气体在反应过程中浓度变化如图(Ⅰ)所示;若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如图(Ⅱ)所示,则下列结论正确的是
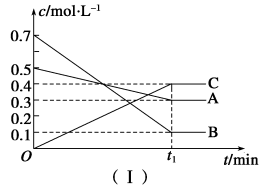



| A.在(t1+10) min时,保持其他条件不变,增大压强,平衡向逆反应方向移动 |
| B.其他条件不变,升高温度时,正、逆反应速率增大,且A的转化率增大 |
| C.T ℃时,在相同容器中,若由0.4 mol·L-1A、0.4 mol·L-1B、0.2 mol·L-1C反应,达到平衡后,C的浓度也为0.4 mol·L-1 |
| D.(t1+10) min时,保持压强不变,通入稀有气体,平衡不移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】在某容积为1L的密闭容器中,A、B、C、D四种气体物质发生可逆反应,其物质的量n(mol)随时间t(min)的变化曲线加图所示。下列说法不正确的是
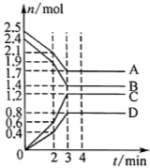

A.该反应的化学方程式为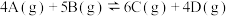 |
B.反应在3min时, |
| C.其他条件不变,4min时体系的压强不再发生变化 |
| D.增加气体D的浓度,B的反应速率随之降低 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】向1L的密闭容器中加入1molX、0.3molZ和一定量的Y三种气体。一定条件下发生反应,各物质的浓度随时间的变化如图甲所示。图乙为t2时刻后改变反应条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件。下列说法不正确的是( )
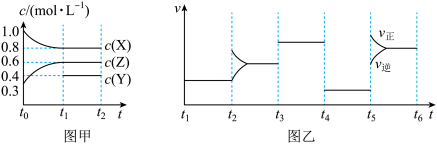

| A.t4时改变的条件为增大容器容积以减小压强 |
| B.该反应的化学方程式为2X(g)+Y(g)⇌3Z(g) ΔH>0 |
| C.若t0 =0,t1=10s,则t0~t1阶段的平均反应速率为υ(Y)=0.03mol·L-1·s-1 |
| D.反应物X的转化率t6点比t4点高 |
您最近一年使用:0次

 SO3(g)+NO(g) △H<0下列有关说法正确的是
SO3(g)+NO(g) △H<0下列有关说法正确的是
 ,在其他条件不变时,改变下列条件能使反应物中活化分子百分数、化学反应速率和化学平衡常数都变化的是
,在其他条件不变时,改变下列条件能使反应物中活化分子百分数、化学反应速率和化学平衡常数都变化的是