现向含6molKI的硫酸溶液中逐滴加入KBrO3溶液,整个过程中含碘物质的物质的量与所加入KBrO3的物质的量的关系如图所示。请回答下列问题:

(1)b点时,KI反应完全,则消耗的氧化剂与还原剂物质的量之比为__ ,还原产物是__ 。
(2)已知b→c过程中,仅有一种元素发生化合价变化,写出并配平该反应的离子方程式__ 。
(3)①已知反应:2BrO3-+I2=2IO3-+Br2;有同学由此得出氧化性:I2>Br2的结论,你认为是否正确,并说明理由:__ 。
②n(KBrO3)=4时,对应含碘物质的化学式为__ 。
(4)含amolKI的硫酸溶液所能消耗n(KBrO3)的最大值为__ 。

(1)b点时,KI反应完全,则消耗的氧化剂与还原剂物质的量之比为
(2)已知b→c过程中,仅有一种元素发生化合价变化,写出并配平该反应的离子方程式
(3)①已知反应:2BrO3-+I2=2IO3-+Br2;有同学由此得出氧化性:I2>Br2的结论,你认为是否正确,并说明理由:
②n(KBrO3)=4时,对应含碘物质的化学式为
(4)含amolKI的硫酸溶液所能消耗n(KBrO3)的最大值为
2011·上海虹口·一模 查看更多[1]
(已下线)上海虹口区2011届高三一模化学试题
更新时间:2020-03-31 16:34:40
|
相似题推荐
计算题
|
较难
(0.4)
解题方法
【推荐1】将含有铜的印刷线路板浸入200 mL氯化铁浓溶液中,有19.2 g铜被腐蚀掉。取出印刷线路板,向溶液中加入16.8 g铁粉,经充分反应,溶液中还存在9.6 g不溶物(设溶液体积不变)。回答下列问题:
(1)写出铜与氯化铁溶液反应的离子方程式_______ 。
(2)充分反应后,溶液中存在的9.6 g不溶物的成分为_______ 。
(3)充分反应后溶液中一定不存在的金属离子为_______ 。
(4)Fe2+、Fe3+、Cu2+的氧化性由强到弱的顺序为_______ ,最后所得溶液中Fe2+的物质的量浓度为_______ mol·L-1。
(1)写出铜与氯化铁溶液反应的离子方程式
(2)充分反应后,溶液中存在的9.6 g不溶物的成分为
(3)充分反应后溶液中一定不存在的金属离子为
(4)Fe2+、Fe3+、Cu2+的氧化性由强到弱的顺序为
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
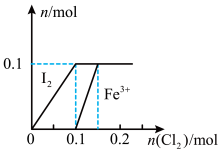
【推荐2】已知5Cl2+I2+6H2O=10HCl+2HIO3,HIO3不与Cl2继续反应。向200 mLFeI2溶液中缓慢通入Cl2,其中I2、Fe3+的物质的量随n(Cl2)的变化如图所示,请回答下列问题:______ 。
(2)当n(Cl2)=0.12 mol时,溶液中的离子主要为______ ,从开始通入Cl2到n(Cl2)=0.12 mol时的总反应的离子方程式为______ 。
(3)在图中画出IO 的物质的量随n(Cl2)的变化曲线
的物质的量随n(Cl2)的变化曲线______ 。
(4)当溶液中n(Cl-):n(IO )=8:1时,通入的氯气在标准状况下的体积为
)=8:1时,通入的氯气在标准状况下的体积为______ 。
(2)当n(Cl2)=0.12 mol时,溶液中的离子主要为
(3)在图中画出IO
 的物质的量随n(Cl2)的变化曲线
的物质的量随n(Cl2)的变化曲线(4)当溶液中n(Cl-):n(IO
 )=8:1时,通入的氯气在标准状况下的体积为
)=8:1时,通入的氯气在标准状况下的体积为
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐1】已知 NH3和 Cl2在常温下可快速反应生成氮气:2 NH3 + 3Cl2 → N2 + 6HCl。当 Cl2和 NH3 比例不同时,产物有差异。
(1)若利用该反应处理含有氨气和氯气的尾气,用于制备盐酸,则 Cl2 和 NH3 的最佳比例为____________ 。该反应可用于检验化工生产中氯气是否泄漏。如氯气有少量泄漏,用氨气检验时有明显现象,此过程中发生反应的Cl2和NH3的体积比范围为___________ 。
(2)体积为1.12 L,质量为3.335 g的Cl2和N2的混合气体通过浓氨水后,体积变为0.672 L(其中Cl2体积分数为50%)(气体体积均为标准状况下测定)。则原混合气体中N2的体积为_____________ mL。
(3)根据第(2)题数据,计算被氧化的NH3的质量。下面是两位学生从不同角度解题时所列的第一步算式,请判断他们所列未知数X分别表示什么量,并填写在表格内:(单位没列出)
(4)有Cl2和N2的混合气体,其中N2的体积分数为x,将1L该混合气体与1L氨气混合,讨论x取不同范围的数值时,所得气体体积y与x的关系式(所有气体体积均在相同状况下测定)。______________
(1)若利用该反应处理含有氨气和氯气的尾气,用于制备盐酸,则 Cl2 和 NH3 的最佳比例为
(2)体积为1.12 L,质量为3.335 g的Cl2和N2的混合气体通过浓氨水后,体积变为0.672 L(其中Cl2体积分数为50%)(气体体积均为标准状况下测定)。则原混合气体中N2的体积为
(3)根据第(2)题数据,计算被氧化的NH3的质量。下面是两位学生从不同角度解题时所列的第一步算式,请判断他们所列未知数X分别表示什么量,并填写在表格内:(单位没列出)
| 学生编号 | 所列第一步算式 | 未知数X表示的意义 |
| 甲 | 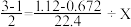 | |
| 乙 |  | |
(4)有Cl2和N2的混合气体,其中N2的体积分数为x,将1L该混合气体与1L氨气混合,讨论x取不同范围的数值时,所得气体体积y与x的关系式(所有气体体积均在相同状况下测定)。
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐2】现有一定量的镁铝合金与100 mL稀硝酸充分反应,在反应过程中无气体放出。在反应结束后的溶液中,逐滴加入1.00mol/LNaOH溶液,加入NaOH溶液的体积与产生沉淀的物质的量的关系如图所示:
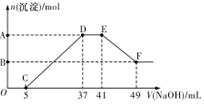
(1)合金中的铝与稀硝酸发生反应的化学方程式为________ 。
(2)纵坐标上A点数值是________ ,B点数值是________ 。
(3)原HNO3溶液中溶质的物质的量浓度为________ 。

(1)合金中的铝与稀硝酸发生反应的化学方程式为
(2)纵坐标上A点数值是
(3)原HNO3溶液中溶质的物质的量浓度为
您最近一年使用:0次
计算题
|
较难
(0.4)
解题方法
【推荐3】次硫酸钠甲醛(xNaHSO2•yHCHO•zH2O)俗称吊白块,在印染、医药以及原子能工业中有广泛应用。它的组成可通过下列实验测定:①准确称取1.5400g样品,完全溶于水配成100mL溶液。②取25.00mL所配溶液经AHMT分光光度法测得甲醛物质的量浓度为0.10mol×L-1。③另取25.00mL所配溶液,加入过量碘完全反应后,加入BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重得到白色固体0.5825g。次硫酸氢钠和碘反应的方程式如下:xNaHSO2•yHCHO•zH2O+I2→NaHSO4+HI+HCHO+H2O(未配平)
(1)生成0.5825g白色固体时,需要消耗碘的质量为_____ 。
(2)若向吊白块溶液中加入氢氧化钠,甲醛会发生自身氧化还原反应,生成两种含氧有机物,写出该反应的离子方程式_____ 。
(3)通过计算确定次硫酸氢钠甲醛的组成______ (写出计算过程)。
(1)生成0.5825g白色固体时,需要消耗碘的质量为
(2)若向吊白块溶液中加入氢氧化钠,甲醛会发生自身氧化还原反应,生成两种含氧有机物,写出该反应的离子方程式
(3)通过计算确定次硫酸氢钠甲醛的组成
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐1】Cu、Cu2O和CuO组成的混合物,加入100mL0.6 mol·L-1HNO3溶液恰好使混合物完全溶解,完全生成硝酸铜、一氧化氮和水。现共收集到224mLNO气体(标准状况)。求:
(1)相同物质的量的Cu、Cu2O和CuO,消耗该浓度硝酸最多的是哪一种物质,写出其与该硝酸反应的离子方程式。________ ,_______________________________ 。
(2)如原混合物中含单质铜0.01moL,则其中Cu2O、CuO的物质的量分别为多少________ ,__________ ?
(3)求混合物中CuO的物质的量可能接近的最大值__________ 。
(1)相同物质的量的Cu、Cu2O和CuO,消耗该浓度硝酸最多的是哪一种物质,写出其与该硝酸反应的离子方程式。
(2)如原混合物中含单质铜0.01moL,则其中Cu2O、CuO的物质的量分别为多少
(3)求混合物中CuO的物质的量可能接近的最大值
您最近一年使用:0次
【推荐2】已知 和
和 在常温下可快速反应生成氮气:
在常温下可快速反应生成氮气: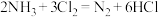 。当
。当 和
和 比例不同时,产物有差异。请回答:
比例不同时,产物有差异。请回答:
 若利用该反应处理含有氨气和氯气的尾气,用于制备盐酸,则
若利用该反应处理含有氨气和氯气的尾气,用于制备盐酸,则 和
和 的最佳体积比为
的最佳体积比为___________ 。
 体积为
体积为 的
的 和
和 的混合气体通过浓氨水后,体积变为
的混合气体通过浓氨水后,体积变为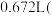 其中
其中 体积分数为
体积分数为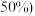 ,则原混合气体中
,则原混合气体中 的体积为
的体积为_____________ 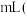 气体体积均为标准状况下测定
气体体积均为标准状况下测定 。
。
 有
有 和
和 的混合气体,其中
的混合气体,其中 的体积分数为x,将
的体积分数为x,将 该混合气体与1L氨气混合,讨论当x取不同范围的数值时,所得气体体积y与x的关系式
该混合气体与1L氨气混合,讨论当x取不同范围的数值时,所得气体体积y与x的关系式 气体体积均在相同状况下测定
气体体积均在相同状况下测定 。
。
 和
和 在常温下可快速反应生成氮气:
在常温下可快速反应生成氮气: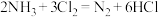 。当
。当 和
和 比例不同时,产物有差异。请回答:
比例不同时,产物有差异。请回答: 若利用该反应处理含有氨气和氯气的尾气,用于制备盐酸,则
若利用该反应处理含有氨气和氯气的尾气,用于制备盐酸,则 和
和 的最佳体积比为
的最佳体积比为 体积为
体积为 的
的 和
和 的混合气体通过浓氨水后,体积变为
的混合气体通过浓氨水后,体积变为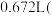 其中
其中 体积分数为
体积分数为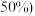 ,则原混合气体中
,则原混合气体中 的体积为
的体积为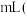 气体体积均为标准状况下测定
气体体积均为标准状况下测定 。
。 有
有 和
和 的混合气体,其中
的混合气体,其中 的体积分数为x,将
的体积分数为x,将 该混合气体与1L氨气混合,讨论当x取不同范围的数值时,所得气体体积y与x的关系式
该混合气体与1L氨气混合,讨论当x取不同范围的数值时,所得气体体积y与x的关系式 气体体积均在相同状况下测定
气体体积均在相同状况下测定 。
。| x的取值范围 | y与x的关系式 |
  |  |
 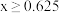 |  |
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
解题方法
【推荐3】填写下列空白:
(1)工业上湿法制备高铁酸钾( )的反应体系中有六种微粒:
)的反应体系中有六种微粒: 、
、 、
、 、
、 、
、 、
、 。写出并配平该反应的离子方程式
。写出并配平该反应的离子方程式___________ ;若反应过程中转移了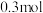 电子,则还原产物的物质的量为
电子,则还原产物的物质的量为___________  。
。
(2)一定条件下,下列物质可以通过化合反应制得的有(写序号)___________ 。
①小苏打 ②硫酸铝 ③氯化亚铁 ④磁性氧化铁 ⑤铜绿(碱式碳酸铜) ⑥氢氧化铁
(3)向一定量的 的混合物中加入
的混合物中加入 的盐酸,恰好使混合物完全溶解,放出
的盐酸,恰好使混合物完全溶解,放出 (标准状况)的气体,在所得溶液中加入
(标准状况)的气体,在所得溶液中加入 溶液无血红色出现。若用足量的
溶液无血红色出现。若用足量的 在高温下还原相同质量的此混合物,能得到铁的质量是
在高温下还原相同质量的此混合物,能得到铁的质量是___________ g。
(4)将 铁粉与含有
铁粉与含有 的
的 溶液完全反应,铁粉全部溶解,并得到
溶液完全反应,铁粉全部溶解,并得到 铜,则参加反应的
铜,则参加反应的 与
与 的物质的量之比为
的物质的量之比为___________ 。
(5)等质量的铝分别与 浓度均为
浓度均为 的盐酸和氢氧化钠溶液反应,生成气体体积比为
的盐酸和氢氧化钠溶液反应,生成气体体积比为 ,铝与氢氧化钠溶液反应的离子方程式:
,铝与氢氧化钠溶液反应的离子方程式:___________ ;铝的质量为___________ g。
(6)将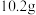 镁铝合金置于
镁铝合金置于 的盐酸中充分反应,无金属剩余,向反应后的溶液中加入
的盐酸中充分反应,无金属剩余,向反应后的溶液中加入 烧碱溶液,沉淀达到最大值,加入的烧碱的物质的量浓度为
烧碱溶液,沉淀达到最大值,加入的烧碱的物质的量浓度为___________  。
。
(1)工业上湿法制备高铁酸钾(
 )的反应体系中有六种微粒:
)的反应体系中有六种微粒: 、
、 、
、 、
、 、
、 、
、 。写出并配平该反应的离子方程式
。写出并配平该反应的离子方程式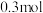 电子,则还原产物的物质的量为
电子,则还原产物的物质的量为 。
。(2)一定条件下,下列物质可以通过化合反应制得的有(写序号)
①小苏打 ②硫酸铝 ③氯化亚铁 ④磁性氧化铁 ⑤铜绿(碱式碳酸铜) ⑥氢氧化铁
(3)向一定量的
 的混合物中加入
的混合物中加入 的盐酸,恰好使混合物完全溶解,放出
的盐酸,恰好使混合物完全溶解,放出 (标准状况)的气体,在所得溶液中加入
(标准状况)的气体,在所得溶液中加入 溶液无血红色出现。若用足量的
溶液无血红色出现。若用足量的 在高温下还原相同质量的此混合物,能得到铁的质量是
在高温下还原相同质量的此混合物,能得到铁的质量是(4)将
 铁粉与含有
铁粉与含有 的
的 溶液完全反应,铁粉全部溶解,并得到
溶液完全反应,铁粉全部溶解,并得到 铜,则参加反应的
铜,则参加反应的 与
与 的物质的量之比为
的物质的量之比为(5)等质量的铝分别与
 浓度均为
浓度均为 的盐酸和氢氧化钠溶液反应,生成气体体积比为
的盐酸和氢氧化钠溶液反应,生成气体体积比为 ,铝与氢氧化钠溶液反应的离子方程式:
,铝与氢氧化钠溶液反应的离子方程式:(6)将
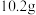 镁铝合金置于
镁铝合金置于 的盐酸中充分反应,无金属剩余,向反应后的溶液中加入
的盐酸中充分反应,无金属剩余,向反应后的溶液中加入 烧碱溶液,沉淀达到最大值,加入的烧碱的物质的量浓度为
烧碱溶液,沉淀达到最大值,加入的烧碱的物质的量浓度为 。
。
您最近一年使用:0次



