解题方法
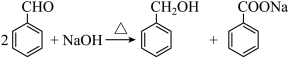
1 . 苯甲醇与苯甲酸是重要的化工原料,可通过苯甲醛在氢氧化钠水溶液中的歧化反应制得,某研究小组在实验室制备苯甲醇与苯甲酸,并测定苯甲酸的纯度。
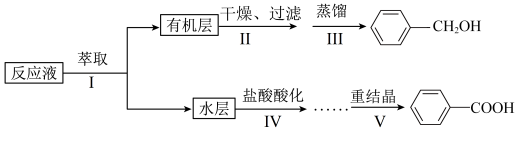
I.制备反应原理及反应结束后对反应液的处理步骤如下:
已知:苯甲醛在空气中极易被氧化,生成白色苯甲酸。
请根据以上信息,回答下列问题(下图夹持仪器已省略):_______ 。
(2)关于制备、提纯过程下列说法正确的是_______ 。
A.步骤I:可用乙醚作为萃取剂
B.步骤Ⅱ:可用无水MgSO4作干燥剂
C.步骤V:具体操作为热水溶解、加入活性炭脱色、冷却结晶
D.步骤V:产品宜用冷水洗涤
E.步骤V:产品可用酒精灯、沸水浴加热烘干
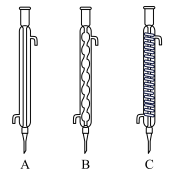
(3)该小组拟用如图装置进行步骤Ⅲ,装置a应选用,_______ (从上图A、B、C中选填,写仪器名称),蒸馏时宜选用减压蒸馏,优点是_______ (任写一点)。_______ 。
Ⅱ.苯甲酸的纯度测定:
(5)为精确测定产品纯度,拟用以下实验方案:称取mg样品,溶于过量的,V1mL浓度为0.1mol/L的氢氧化钾溶液中,滴加几滴酚酞溶液,摇匀,用0.1mol/L盐酸滴定,达到滴定终点,记录耗酸体积。做3组平行实验,所消耗盐酸的平均体积为V2mL。
①滴定终点现象是_______ 。
②产品的纯度是_______ %。
③若用甲基橙作指示剂,则测定结果_______ (填“偏大”、“偏小”或“无影响”)。
I.制备反应原理及反应结束后对反应液的处理步骤如下:
| 名称 | 相对分子质量 | 熔点℃ | 沸点℃ | 溶解性 | 其他 |
| 苯甲醇 | 108 | -15.3 | 205.7 | 在水中溶解度较小,易溶于乙醚、乙醇 | 加热时易分子间脱水成醚 |
| 苯甲酸 | 122 | 122.4(100℃左右开始升华) | 248 | 微溶于冷水,易溶于乙醇、热水 | 毒性较小 |
请根据以上信息,回答下列问题(下图夹持仪器已省略):
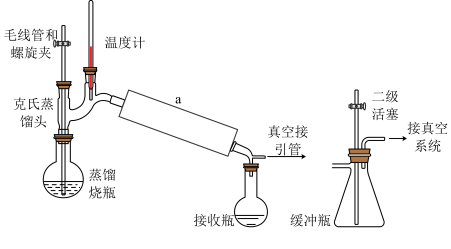
(2)关于制备、提纯过程下列说法正确的是
A.步骤I:可用乙醚作为萃取剂
B.步骤Ⅱ:可用无水MgSO4作干燥剂
C.步骤V:具体操作为热水溶解、加入活性炭脱色、冷却结晶
D.步骤V:产品宜用冷水洗涤
E.步骤V:产品可用酒精灯、沸水浴加热烘干
(3)该小组拟用如图装置进行步骤Ⅲ,装置a应选用,
Ⅱ.苯甲酸的纯度测定:
(5)为精确测定产品纯度,拟用以下实验方案:称取mg样品,溶于过量的,V1mL浓度为0.1mol/L的氢氧化钾溶液中,滴加几滴酚酞溶液,摇匀,用0.1mol/L盐酸滴定,达到滴定终点,记录耗酸体积。做3组平行实验,所消耗盐酸的平均体积为V2mL。
①滴定终点现象是
②产品的纯度是
③若用甲基橙作指示剂,则测定结果
您最近半年使用:0次
解题方法
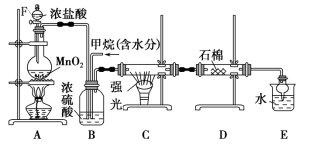
2 . 利用甲烷与氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实。某化学兴趣小组在实验室中模拟上述过程,其设计的模拟装置如图所示:_______ 。
(2)装置B一般有三种功能:①控制气体流速;②均匀混合气体;③_______ 。控制氯气流速的实验操作是_______ 。
(3)请写出C装置中由CH4生成CH2Cl2的总化学方程式:_______ 。
(4)其它烷烃也可与氯气发生取代反应,写出含有四个碳原子的烷烃的一种结构简式:_____ 。
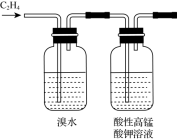
(5)国际上以乙烯的产量来衡量一个国家石油化工的生产水平,乙烯是通过对石油进行_______ (填“分馏”、“裂化”、“裂解”)加工炼制得到。如图所示,乙烯可使溴水褪色,其发生反应的化学方程式是_______ ,乙烯可使酸性高锰酸钾溶液褪色,其发生反应的类型是_______ 。
(2)装置B一般有三种功能:①控制气体流速;②均匀混合气体;③
(3)请写出C装置中由CH4生成CH2Cl2的总化学方程式:
(4)其它烷烃也可与氯气发生取代反应,写出含有四个碳原子的烷烃的一种结构简式:
(5)国际上以乙烯的产量来衡量一个国家石油化工的生产水平,乙烯是通过对石油进行
您最近半年使用:0次
3 . 邻苯二甲酸二丁酯(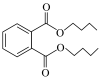 )为无色粘稠液体,可用作增塑剂,对多种树脂具有很强溶解力,通过邻苯二甲酸酐(
)为无色粘稠液体,可用作增塑剂,对多种树脂具有很强溶解力,通过邻苯二甲酸酐(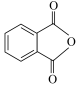 )和正丁醇制备邻苯二甲酸二丁酯的反应如下(其中第一步反应会完全进行):
)和正丁醇制备邻苯二甲酸二丁酯的反应如下(其中第一步反应会完全进行):
第二步:
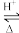
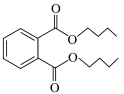 +H2O。
+H2O。
| 物质 | 相对分子质量 | 沸点/℃ | 溶解性 | 其他性质 |
| 正丁醇 | 74 | 117.6 | 易溶于有机溶剂,在水中溶解度不大 | 密度小于水 |
| 邻苯二甲酸单丁酯 | 222 | 363.5 | 易溶于有机溶剂,难溶于水 | |
| 邻苯二甲酸二丁酯 | 278 | 337 | 易溶于有机溶剂,不溶于水 | 着火点202℃ |
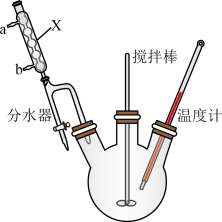
①向三颈烧瓶内加入
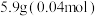 邻苯二甲酸酐,
邻苯二甲酸酐, 正丁醇,几粒沸石和
正丁醇,几粒沸石和 浓硫酸;另在分水器中加入正丁醇至与分水器支管口齐平,后加热三颈烧瓶至微沸。
浓硫酸;另在分水器中加入正丁醇至与分水器支管口齐平,后加热三颈烧瓶至微沸。②待三颈烧瓶内邻苯二甲酸䣲完全溶解后,继续升温,并持续搅拌反应2小时,保温至反应结束。
③冷却至室温,将反应混合物倒出;依次用
 溶液、饱和食盐水洗涤得到粗产品。
溶液、饱和食盐水洗涤得到粗产品。④粗产品用无水硫酸镁处理→取处理后的液体→圆底烧瓶→减压蒸馏,经过处理得到产品
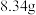 。
。回答下列问题:
(1)仪器X的名称为
(2)分水器使用前需要进行的操作为
(3)制备的第一步是制备邻苯二甲酸单丁酯,涉及反应的化学方程式为
(4)实验中用
 溶液洗涤的目的为
溶液洗涤的目的为(5)本实验中,邻苯二甲酸二丁酯的产率为
您最近半年使用:0次
名校
解题方法
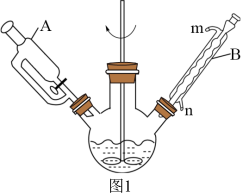
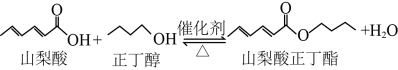
4 . 山梨酸酯具有解毒作用,可以减轻肝脏负担,促进肝细胞修复,保护肝脏健康。实验室用如图1所示装置(夹持、加热装置省略),依据下面的原理制备山梨酸正丁酯。
实验步骤:
①在三颈烧瓶中加入16.8g山梨酸、7.4g正丁醇、少量催化剂和几粒沸石,水浴加热三颈烧瓶,使反应体系保持微沸。
②回流4小时后停止加热和搅拌,反应液冷却至室温。
③滤去催化剂和沸石,将滤液倒入200mL水中,加入50mL乙醚,倒入分液漏斗中,分液。
④分离出的有机层先用ρ=10mg/L的NaHCO3溶液洗涤至中性,再用水洗涤分液,收集有机层。
⑤在有机层中加入少量无水MgSO4,静置片刻,过滤。
⑥将滤液进行蒸馏,除去杂质得到纯净的山梨酸正丁酯6.0g。
回答下列问题:
(1)仪器A的名称是___________ ;冷却水由___________ (填“m”或“n”)口通入。
(2)洗涤、分液过程中,加入ρ=10mg/L的NaHCO3溶液的目的是___________ 。
(3)在实验步骤④中加入少量无水MgSO₄的目的是___________ 。
(4)在实验步骤⑥中进行蒸馏,蒸馏至120℃除去的杂质是___________ 。
(5)本实验中,山梨酸正丁酯的产率是___________ (精确至0.1%)。
(6)为了提高反应正向进行的程度,实验室常使用如图2所示装置(夹持、加热装置已略去)代替图1装置制备山梨酸正丁酯以提高产物的产率,请结合环己烷的物理性质,解释在该装置中环己烷的主要作用___________ 。
| 物质 | 相对分子质量 | 密度/(g·cm-3) | 沸点/℃ | 水溶性 |
| 山梨酸 | 112 | 1.204 | 228 | 易溶 |
| 正丁醇 | 74 | 0.8089 | 117 | 溶 |
| 山梨酸正丁酯 | 168 | 0.926 | 195 | 难溶 |
| 乙醚 | 74 | 0.714 | 34.6 | 难溶 |
| 环己烷 | 84 | 0.779 | 80.7 | 难溶 |
①在三颈烧瓶中加入16.8g山梨酸、7.4g正丁醇、少量催化剂和几粒沸石,水浴加热三颈烧瓶,使反应体系保持微沸。
②回流4小时后停止加热和搅拌,反应液冷却至室温。
③滤去催化剂和沸石,将滤液倒入200mL水中,加入50mL乙醚,倒入分液漏斗中,分液。
④分离出的有机层先用ρ=10mg/L的NaHCO3溶液洗涤至中性,再用水洗涤分液,收集有机层。
⑤在有机层中加入少量无水MgSO4,静置片刻,过滤。
⑥将滤液进行蒸馏,除去杂质得到纯净的山梨酸正丁酯6.0g。
回答下列问题:
(1)仪器A的名称是
(2)洗涤、分液过程中,加入ρ=10mg/L的NaHCO3溶液的目的是
(3)在实验步骤④中加入少量无水MgSO₄的目的是
(4)在实验步骤⑥中进行蒸馏,蒸馏至120℃除去的杂质是
(5)本实验中,山梨酸正丁酯的产率是
(6)为了提高反应正向进行的程度,实验室常使用如图2所示装置(夹持、加热装置已略去)代替图1装置制备山梨酸正丁酯以提高产物的产率,请结合环己烷的物理性质,解释在该装置中环己烷的主要作用

您最近半年使用:0次
名校
解题方法
5 . 常见的一硝基甲苯有对硝基甲苯和邻硝基甲苯两种,均可用于合成各种染料,某探究小组利用下列反应和装置制备一硝基甲苯。
实验步骤:
①按体积比1:3配制浓硫酸与浓硝酸混合物40mL;
②在三颈瓶中加入15mL(13g)甲苯,按图所示装好药品和其他仪器;
③向三颈瓶中加入混酸,并不断搅拌(磁力搅拌器已略去);
④控制温度约为50℃,反应大约10min,三颈瓶底有大量淡黄色油状液体出现;
⑤分离出一硝基甲苯的总质量13.60g。
请回答下列问题:
(1)反应中的加热方式是______________ 。
(2)使用仪器A前必须进行的操作是________________ ,仪器B的作用是_____________ 。
(3)若实验后在三颈瓶中收集到的产物较少,可能的原因是______________________ 。
(4)分离反应后产物的方案如下:______________ 。
(5)一硝基甲苯的产率为___________ (保留两位有效数字)。产率=(实际产量/理论产量)×100%


密度/ | 沸点/℃ | 溶解性 | |
甲苯 | 0.866 | 110.6 | 不溶于水,易溶于硝基甲苯 |
对硝基甲苯 | 1.286 | 237.7 | 不溶于水,易溶于液态烃 |
邻硝基甲苯 | 1.162 | 222 | 不溶于水,易溶于液态烃 |
①按体积比1:3配制浓硫酸与浓硝酸混合物40mL;
②在三颈瓶中加入15mL(13g)甲苯,按图所示装好药品和其他仪器;
③向三颈瓶中加入混酸,并不断搅拌(磁力搅拌器已略去);
④控制温度约为50℃,反应大约10min,三颈瓶底有大量淡黄色油状液体出现;
⑤分离出一硝基甲苯的总质量13.60g。
请回答下列问题:
(1)反应中的加热方式是
(2)使用仪器A前必须进行的操作是
(3)若实验后在三颈瓶中收集到的产物较少,可能的原因是
(4)分离反应后产物的方案如下:

(5)一硝基甲苯的产率为
您最近半年使用:0次
名校
解题方法
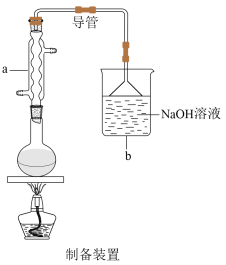
6 . 某实验小组设计如图所示实验装置来制取乙炔,并粗略测定电石(含有N、P、S等元素)中碳化钙的质量分数。回答下列问题:_________ 。
(2)仪器b中发生反应的化学方程式为_________ ,实验过程中为了减缓水与电石的反应速率,可采取的措施是_________ (写一条即可)。
(3)将生成的气体通入酸性KMnO4溶液中,观察到酸性KMnO4溶液褪色。
①_______ (填“能”或“不能”)说明生成的气体全部为乙炔,原因是______ 。
②实验小组发现该实验不能用启普发生器来制取乙炔,理由是______ (写一条即可)。
(4)为了安全,点燃乙炔前应_______ ,乙炔燃烧时的现象是____________ 。
(5)取mg电石样品,使其与水完全反应,实验结束后测得排入量筒中水的体积为VmL,则电石中碳化钙的质量分数为______ (用含V和m的代数式表示,忽略导管中残留的水和气体中含有的水蒸气,所有气体均已换算成标准状况下)。
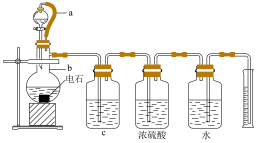
(2)仪器b中发生反应的化学方程式为
(3)将生成的气体通入酸性KMnO4溶液中,观察到酸性KMnO4溶液褪色。
①
②实验小组发现该实验不能用启普发生器来制取乙炔,理由是
(4)为了安全,点燃乙炔前应
(5)取mg电石样品,使其与水完全反应,实验结束后测得排入量筒中水的体积为VmL,则电石中碳化钙的质量分数为
您最近半年使用:0次
解题方法
7 . 柱色谱法包含两个相,一个是固定相,一个是流动相。当两相相对运动时,反复多次地利用混合物中所含各组分分配平衡性质的差异,最后达到彼此分离的目的。茉莉醛(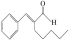 )是一种合成香料、制备苯莉醛的工艺流程如图所示。下列说法正确的是
)是一种合成香料、制备苯莉醛的工艺流程如图所示。下列说法正确的是
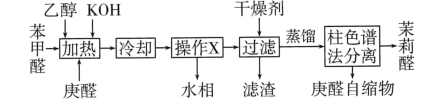
| A.乙醇的主要作用是助溶剂 |
| B.操作X为过滤 |
| C.可将最后两步“蒸馏”和“柱色谱法分离” 替换为“真空减压蒸馏” |
| D.可采用与浓硫酸共热的方法来除去产品中少量的庚醛自缩物 |
您最近半年使用:0次
解题方法
8 . 抗血栓药物氯吡格雷的重要中间体之一“2―噻吩乙醇”( )的制备步骤如下:
)的制备步骤如下: ,静置,过滤 ⑤进行________,分离出四氢呋喃、噻吩和液体X等杂质 ⑥得到ng产品。
,静置,过滤 ⑤进行________,分离出四氢呋喃、噻吩和液体X等杂质 ⑥得到ng产品。
按要求回答下列问题:
(1)步骤ⅰ中液体X可以选择_______ 。
a.水 b.甲苯 c.乙醇 d.苯酚
(2)写出步骤ⅰ制2-噻吩钠的化学方程式为_______ 。
(3)步骤ⅱ,加入溶液的方式为________ (填“缓慢加入”或“一次性加入”)。
(4)写出步骤ⅲ中用盐酸调节pH的化学方程式:________ 。加入无水 的作用为
的作用为___________ 。
(5)步骤ⅲ中⑤的操作的名称为_______ ;写出选择此分离提纯方法的理由是_______ 。
(6)产品“2―噻吩乙醇”( )的产率为
)的产率为_______ (用含m、n的代数式表示)。
(7)某次平行实验所得产品质量比ng低些,写出其中一种可能的原因:_______ 。
 )的制备步骤如下:
)的制备步骤如下: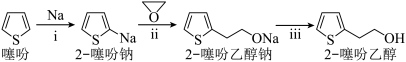
ⅱ.制噻吩乙醇钠:降温至−10℃,加入稍过量的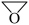 的四氢呋喃溶液,反应30min(四氢呋喃
的四氢呋喃溶液,反应30min(四氢呋喃 是有机溶剂,沸点66℃,可防止因反应放热而导致温度过高而引发副反应)。
是有机溶剂,沸点66℃,可防止因反应放热而导致温度过高而引发副反应)。
 ,静置,过滤 ⑤进行________,分离出四氢呋喃、噻吩和液体X等杂质 ⑥得到ng产品。
,静置,过滤 ⑤进行________,分离出四氢呋喃、噻吩和液体X等杂质 ⑥得到ng产品。按要求回答下列问题:
(1)步骤ⅰ中液体X可以选择
a.水 b.甲苯 c.乙醇 d.苯酚
(2)写出步骤ⅰ制2-噻吩钠的化学方程式为
(3)步骤ⅱ,加入溶液的方式为
(4)写出步骤ⅲ中用盐酸调节pH的化学方程式:
 的作用为
的作用为(5)步骤ⅲ中⑤的操作的名称为
(6)产品“2―噻吩乙醇”(
 )的产率为
)的产率为(7)某次平行实验所得产品质量比ng低些,写出其中一种可能的原因:
您最近半年使用:0次
解题方法
9 . 实验室可以在 用浓硝酸在硝酸汞催化下氧化乙炔
用浓硝酸在硝酸汞催化下氧化乙炔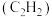 气体来制备草酸,主要装置如图所示。
气体来制备草酸,主要装置如图所示。错误 的是
 用浓硝酸在硝酸汞催化下氧化乙炔
用浓硝酸在硝酸汞催化下氧化乙炔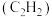 气体来制备草酸,主要装置如图所示。
气体来制备草酸,主要装置如图所示。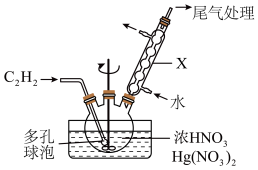
| A.多孔球泡可增加气体与溶液的接触面积 |
B.用电石制得的 中含有的 中含有的 杂质,应用 杂质,应用 溶液除去 溶液除去 |
| C.增大硝酸的质量分数,草酸的产率可能会下降 |
D.实验中会产生氮氧化物等污染性气体,可用 溶液吸收 溶液吸收 |
您最近半年使用:0次
名校
解题方法
10 . 1-溴丁烷可用于合成麻醉药盐酸丁卡因,也用于生产染料和香料,是稀有元素萃取的溶剂及有机合成的中间体,其制备如图(夹持装置略): (浓)
(浓)
ⅱ.
ⅲ. (浓)
(浓)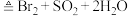
请回答下列问题:
(1)在反应时,若选用较浓的硫酸作为反应物,得到的产品会呈黄色,为除去颜色,最好选择下列的_______ (填标号)溶液来洗涤产品。
A.四氯化碳 B.硫酸钠 C.氢氧化钠 D.亚硫酸钠
产品选择上述溶液洗涤后,还需要用蒸馏水洗涤一次,洗涤液与产品分离的操作是_______ (填操作名称)。
(2)分离得到的有机层依次用适量的水、饱和 溶液、水洗涤、用无水
溶液、水洗涤、用无水 干燥,蒸馏,得到最终产品。若投入正丁醇
干燥,蒸馏,得到最终产品。若投入正丁醇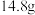 ,得到产物
,得到产物 ,则1-溴丁烷的产率为
,则1-溴丁烷的产率为______ %(保留一位小数)。
(3)探究小组为研究1-溴丁烷的水解反应和消去反应,设计如下探究实验:_______ 。
②实验ⅲ的有机化学反应方程式是_______ 。
③为深入研究1-溴丁烷与 溶液是否能发生消去反应,小组设计如图装置探究(加热和夹持装置略去):
溶液是否能发生消去反应,小组设计如图装置探究(加热和夹持装置略去):
Ⅰ.甲同学认为不能依据酸性高锰酸钾溶液褪色,判断A中发生消去反应,理由是_______ 。
Ⅱ.乙同学对实验进行了改进,依据实验现象可判断是否发生消去反应,改进的方案是_______ 。
 (浓)
(浓)
ⅱ.

ⅲ.
 (浓)
(浓)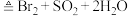
请回答下列问题:
(1)在反应时,若选用较浓的硫酸作为反应物,得到的产品会呈黄色,为除去颜色,最好选择下列的
A.四氯化碳 B.硫酸钠 C.氢氧化钠 D.亚硫酸钠
产品选择上述溶液洗涤后,还需要用蒸馏水洗涤一次,洗涤液与产品分离的操作是
(2)分离得到的有机层依次用适量的水、饱和
 溶液、水洗涤、用无水
溶液、水洗涤、用无水 干燥,蒸馏,得到最终产品。若投入正丁醇
干燥,蒸馏,得到最终产品。若投入正丁醇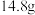 ,得到产物
,得到产物 ,则1-溴丁烷的产率为
,则1-溴丁烷的产率为(3)探究小组为研究1-溴丁烷的水解反应和消去反应,设计如下探究实验:
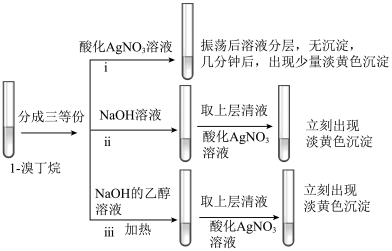
②实验ⅲ的有机化学反应方程式是
③为深入研究1-溴丁烷与
 溶液是否能发生消去反应,小组设计如图装置探究(加热和夹持装置略去):
溶液是否能发生消去反应,小组设计如图装置探究(加热和夹持装置略去):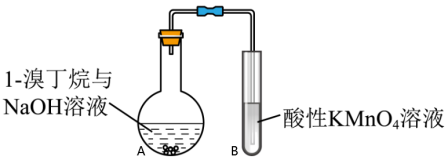
Ⅰ.甲同学认为不能依据酸性高锰酸钾溶液褪色,判断A中发生消去反应,理由是
Ⅱ.乙同学对实验进行了改进,依据实验现象可判断是否发生消去反应,改进的方案是
您最近半年使用:0次
2024-05-04更新
|
369次组卷
|
3卷引用:山东省青岛第五十八中学2023-2024学年高二下学期4月月考化学试卷




