名校
解题方法
1 . 下列装置能达到相应实验目的的是
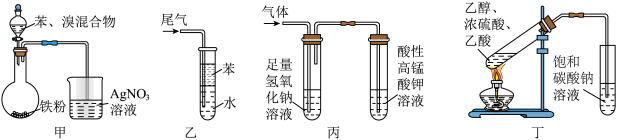

A.利用甲装置可制备溴苯并验证有 生成 生成 | B.利用乙装置可吸收 并防倒吸 并防倒吸 |
C.利用丙装置可检验含有 杂质的乙烯 杂质的乙烯 | D.利用丁装置可制备并收集乙酸乙酯 |
您最近一年使用:0次
名校
解题方法
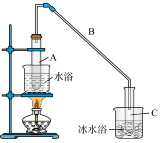
2 . 某化学小组采用类似制乙酸乙酯的装置(如图),以环己醇制备环己烯。
已知: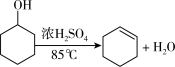
(1)制备粗品
将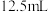 环己醇加入试管A中,再加入
环己醇加入试管A中,再加入 浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①A中碎瓷片的作用是___________ ,导管B的作用是___________ 。
②试管C置于冰水浴中的目的是___________ 。
(2)制备精品
环己烯粗品中含有环己醇和少量有机酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在___________ 层(填“上”或下),分液后用___________ (填编号)洗涤,再进行蒸馏。
a. 溶液 b.稀
溶液 b.稀 c.饱和
c.饱和 溶液
溶液
(3)欲除去环己烯中的环己醇杂质,以下试剂合理的是___________ 。
a.水 b.浓硫酸 c.酸性高锰酸钾溶液 d.溴水

已知:

密度( ) ) | 熔点(℃) | 沸点(℃) | 溶解性 | |
| 环己醇 | 0.96 | 25 | 161 | 能溶于水 |
| 环己烯 | 0.81 | 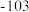 | 83 | 难溶于水 |
将
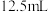 环己醇加入试管A中,再加入
环己醇加入试管A中,再加入 浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。①A中碎瓷片的作用是
②试管C置于冰水浴中的目的是
(2)制备精品
环己烯粗品中含有环己醇和少量有机酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在
a.
 溶液 b.稀
溶液 b.稀 c.饱和
c.饱和 溶液
溶液(3)欲除去环己烯中的环己醇杂质,以下试剂合理的是
a.水 b.浓硫酸 c.酸性高锰酸钾溶液 d.溴水
您最近一年使用:0次
名校
解题方法
3 . 苯甲酸可用作食品防腐剂。实验室可通过甲苯氧化制苯甲酸,其反应原理简示如下:

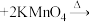
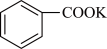


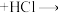


实验步骤:
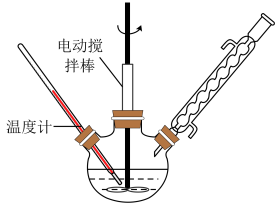
①在装有温度计、冷凝管和搅拌器的三颈烧瓶中加入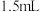 甲苯、
甲苯、 水和
水和 (约
(约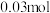 )高锰酸钾,慢慢开启搅拌器,并加热回流反应。
)高锰酸钾,慢慢开启搅拌器,并加热回流反应。
②停止加热,继续搅拌,冷却片刻后,从冷凝管上口慢慢加入适量饱和亚硫酸氢钠溶液,并将反应混合物趁热过滤,用少量热水洗涤滤渣。合并滤液和洗涤液,于冰水浴中冷却,然后用浓盐酸酸化至苯甲酸析出完全。将析出的苯甲酸过滤,用少量冷水洗涤,放在沸水浴上干燥。称量,粗产品为 。
。
③纯度测定:称取经过提纯后的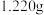 产品,配成
产品,配成 甲醇溶液,取
甲醇溶液,取 溶液与
溶液与 溶液反应,消耗
溶液反应,消耗 的物质的量为
的物质的量为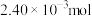 。
。
回答下列问题:
(1)步骤①中当看到__________ 现象即可判断反应已完成,可以停止加热。
(2)步骤②中加入适量饱和亚硫酸氢钠溶液的作用是__________ 。
(3)测定粗产品的熔点,发现其在115℃开始熔化,达到130℃时仍有少量不熔,该同学推测粗产品是苯甲酸与 的混合物,设计了如下方案进行提纯和检验,实验结果表明推测正确。按要求填写下列表格:
的混合物,设计了如下方案进行提纯和检验,实验结果表明推测正确。按要求填写下列表格:
(4)若要得到纯度更高的苯甲酸可通过__________ 的方法对粗产品提纯。在该操作中,不需要用到的仪器是__________ 。
A. B.
B. C.
C. D.
D.
(5)步骤③纯度测定,根据有关数据计算粗产品中苯甲酸质量分数为__________ 。

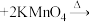



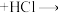


名称 |
| 熔点/℃ | 沸点/℃ | 密度 | 溶解性 |
甲苯 | 92 |
| 110.6 | 0.867 | 不溶于水,易溶于乙醇 |
苯甲酸 | 122 | 122.4(100℃左右开始升华) | 248 | 微溶于冷水,易溶于乙醇,热水 |
①在装有温度计、冷凝管和搅拌器的三颈烧瓶中加入
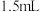 甲苯、
甲苯、 水和
水和 (约
(约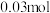 )高锰酸钾,慢慢开启搅拌器,并加热回流反应。
)高锰酸钾,慢慢开启搅拌器,并加热回流反应。②停止加热,继续搅拌,冷却片刻后,从冷凝管上口慢慢加入适量饱和亚硫酸氢钠溶液,并将反应混合物趁热过滤,用少量热水洗涤滤渣。合并滤液和洗涤液,于冰水浴中冷却,然后用浓盐酸酸化至苯甲酸析出完全。将析出的苯甲酸过滤,用少量冷水洗涤,放在沸水浴上干燥。称量,粗产品为
 。
。③纯度测定:称取经过提纯后的
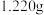 产品,配成
产品,配成 甲醇溶液,取
甲醇溶液,取 溶液与
溶液与 溶液反应,消耗
溶液反应,消耗 的物质的量为
的物质的量为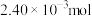 。
。
回答下列问题:
(1)步骤①中当看到
(2)步骤②中加入适量饱和亚硫酸氢钠溶液的作用是
(3)测定粗产品的熔点,发现其在115℃开始熔化,达到130℃时仍有少量不熔,该同学推测粗产品是苯甲酸与
 的混合物,设计了如下方案进行提纯和检验,实验结果表明推测正确。按要求填写下列表格:
的混合物,设计了如下方案进行提纯和检验,实验结果表明推测正确。按要求填写下列表格:序号 | 实验方案 | 实验现象 | 结论 |
① | 将粗产品加入水中,加热溶解, | 得到白色晶体和无色溶液 | — |
② | 取少量滤液于试管中,滴入适量的硝酸酸化的 溶液 溶液 | 生成白色沉淀 | 滤液含 |
③ | 干燥白色晶体, | 白色晶体是苯甲酸 |
A.
 B.
B. C.
C. D.
D.
(5)步骤③纯度测定,根据有关数据计算粗产品中苯甲酸质量分数为
您最近一年使用:0次
解题方法
4 . 一硝基甲苯是一种重要的工业原料,某化学学习小组设计如图所示装置(夹持及搅拌装置已略去)制备一硝基甲苯,实验步骤如下:
①配制浓硫酸和浓硝酸的混合物(混酸,足量);
②在三颈烧瓶中加入15mL甲苯(密度为0.866g•cm-3);
③装好其他试剂,并组装好仪器;
④向三颈烧瓶中加入混酸,并不断搅拌;
⑤控制温度,反应大约10min至三颈烧瓶底部有大量液体(淡黄色油状)出现;
⑥分离出一硝基甲苯,经提纯最终得到一硝基甲苯12.5g。
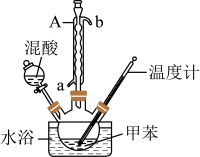
根据上述实验,回答下列问题:
(1)仪器A的名称是______ ,作用是______ 。
(2)本实验的关键是控制温度在30℃左右,如果温度过高,可能会产生_____ (填一种物质的名称)等副产物。写出甲苯与混酸反应生成2,4,6-三硝基甲苯的化学方程式:______ 。
分离产品的方案如图:
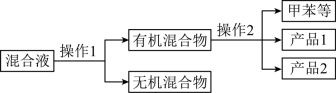
(3)操作1一定需要用到的玻璃仪器是______ ,操作2的名称是______ 。
(4)经测定产品2的核磁共振氢谱中有3组峰,则产品2的结构简式为______ 。
(5)本实验中一硝基甲苯的产率为______ (结果保留三位有效数字)。
①配制浓硫酸和浓硝酸的混合物(混酸,足量);
②在三颈烧瓶中加入15mL甲苯(密度为0.866g•cm-3);
③装好其他试剂,并组装好仪器;
④向三颈烧瓶中加入混酸,并不断搅拌;
⑤控制温度,反应大约10min至三颈烧瓶底部有大量液体(淡黄色油状)出现;
⑥分离出一硝基甲苯,经提纯最终得到一硝基甲苯12.5g。

根据上述实验,回答下列问题:
(1)仪器A的名称是
(2)本实验的关键是控制温度在30℃左右,如果温度过高,可能会产生
分离产品的方案如图:

(3)操作1一定需要用到的玻璃仪器是
(4)经测定产品2的核磁共振氢谱中有3组峰,则产品2的结构简式为
(5)本实验中一硝基甲苯的产率为
您最近一年使用:0次
2023-04-22更新
|
147次组卷
|
6卷引用:重庆市名校联盟2021-2022学年高二下学期5月大联考化学试题
名校
5 . 用下列装置进行相应的实验,能达到实验目的的是
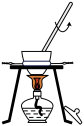 | 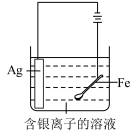 |  |  |
| A.灼烧碎海带 | B.电镀银 | C.氧化还原反应滴定 | D.制备乙酸乙酯 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-04-22更新
|
488次组卷
|
3卷引用:福建省莆田市2023届高中毕业班下学期3月第二次教学质量检测化学试题
解题方法
6 . 实验室制备丙炔酸甲酯(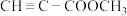 ,沸点为103〜105°C)的流程如下,下列说法错误的是
,沸点为103〜105°C)的流程如下,下列说法错误的是

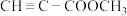 ,沸点为103〜105°C)的流程如下,下列说法错误的是
,沸点为103〜105°C)的流程如下,下列说法错误的是
| A.“蒸馏”时不能用水浴加热 |
| B.“操作1”名称为干燥 |
| C.“洗涤2”中5%Na2CO3溶液的作用是除去丙快酸等酸性物质 |
| D.“反应”前加入试剂的顺序为浓硫酸、丙炔酸、甲醇 |
您最近一年使用:0次
名校
解题方法
7 . 氨基甲磺酸(H2NCH2SO3H)具有抗癌和抗病毒活性,在生产生活领域应用广泛。某兴趣小组在实验室模拟工业上用氨气、甲醛和亚硫酸氢钠反应制备氨基甲磺酸的反应,装置及步骤如下。
查阅资料:①甲醛为无色、有特殊刺激性气味的气体,具有还原性。
②氨基甲磺酸为白色结晶或粉末.微溶于水、甲醇和乙醚,溶于碱液。
③制备过程涉及的反应HCHO+NaHSO3→HOCH2SO3Na;
HOCH2SO3Na+NH3→H2NCH2SO3Na+H2O;
2H2NCH2SO3Na+H2SO4→2H2NCH2SO3H+Na2SO4。
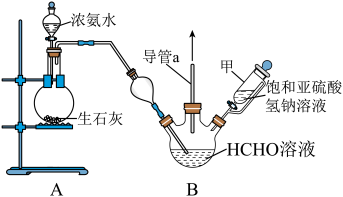
步骤Ⅰ:准确量取含66.0g甲醛的水溶液,加入三颈烧瓶中;
步骤Ⅱ:控制温度10℃左右,缓慢加入饱和亚硫酸氢钠溶液至过量,缓慢升温到50℃左右继续反应;
步骤Ⅲ:待反应完成后,通入过量氨气,充分反应;
步骤Ⅳ:反应完成后,缓慢加入足量的硫酸溶液,降温结晶,过滤并用冰水洗涤,得干燥固体177.6g。
回答下列问题:
(1)仪器甲的名称为_____ ;步骤Ⅱ中控制温度50℃左右的加热方式最好是_____ 。
(2)实验室用氯化铵和氢氧化钙反应制取氨气的化学方程式为_____ 。装置A能够制取少量氨气,请结合化学用语简述原理:_____ 。
(3)步骤Ⅳ中,用冰水洗涤的目的是_____ 。
(4)装置B中,导管a的作用是______ 。
(5)本实验中的产品产率为______ (保留三位有效数字)。
查阅资料:①甲醛为无色、有特殊刺激性气味的气体,具有还原性。
②氨基甲磺酸为白色结晶或粉末.微溶于水、甲醇和乙醚,溶于碱液。
③制备过程涉及的反应HCHO+NaHSO3→HOCH2SO3Na;
HOCH2SO3Na+NH3→H2NCH2SO3Na+H2O;
2H2NCH2SO3Na+H2SO4→2H2NCH2SO3H+Na2SO4。

步骤Ⅰ:准确量取含66.0g甲醛的水溶液,加入三颈烧瓶中;
步骤Ⅱ:控制温度10℃左右,缓慢加入饱和亚硫酸氢钠溶液至过量,缓慢升温到50℃左右继续反应;
步骤Ⅲ:待反应完成后,通入过量氨气,充分反应;
步骤Ⅳ:反应完成后,缓慢加入足量的硫酸溶液,降温结晶,过滤并用冰水洗涤,得干燥固体177.6g。
回答下列问题:
(1)仪器甲的名称为
(2)实验室用氯化铵和氢氧化钙反应制取氨气的化学方程式为
(3)步骤Ⅳ中,用冰水洗涤的目的是
(4)装置B中,导管a的作用是
(5)本实验中的产品产率为
您最近一年使用:0次
名校
解题方法
8 . 1,2-二氯乙烷是制备杀菌剂和植物生长调节剂的中间体,已知其沸点为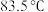 ,熔点为
,熔点为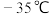 。下图为实验室中制备1,2-二氯乙烷的装置,无水乙醇的密度约为
。下图为实验室中制备1,2-二氯乙烷的装置,无水乙醇的密度约为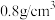 ,其中加热和夹持装置已略去。
,其中加热和夹持装置已略去。
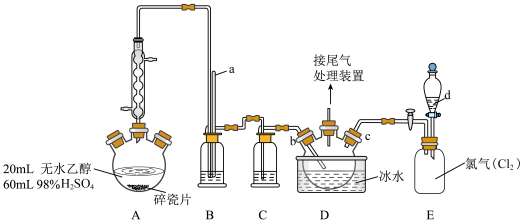
(1)装置A中还缺少的一种必要仪器是_______ ,使用冷凝管的目的是_______ 。
(2)装置A中发生主要反应的化学方程式为_______ 。
(3)装置B中玻璃管a的作用是_______ 。
(4)装置B中应加入的最佳试剂为_______(填字母序号)。
(5)D中b、c两个导气管进入仪器的长度不同,其目的是_______ 。
(6)实验结束后收集得到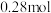 1,2—二氯乙烷,则乙醇的利用率为
1,2—二氯乙烷,则乙醇的利用率为_______ %。
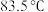 ,熔点为
,熔点为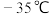 。下图为实验室中制备1,2-二氯乙烷的装置,无水乙醇的密度约为
。下图为实验室中制备1,2-二氯乙烷的装置,无水乙醇的密度约为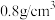 ,其中加热和夹持装置已略去。
,其中加热和夹持装置已略去。
(1)装置A中还缺少的一种必要仪器是
(2)装置A中发生主要反应的化学方程式为
(3)装置B中玻璃管a的作用是
(4)装置B中应加入的最佳试剂为_______(填字母序号)。
| A.浓硫酸 | B.饱和 溶液 溶液 |
C.酸性 溶液 溶液 | D. 溶液 溶液 |
(6)实验结束后收集得到
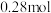 1,2—二氯乙烷,则乙醇的利用率为
1,2—二氯乙烷,则乙醇的利用率为
您最近一年使用:0次
2023-04-21更新
|
486次组卷
|
3卷引用:山东省济宁市2022-2023学年高二下学期4月期中考试化学试题
解题方法
9 . 在无水三氯化铝的催化作用下,利用乙醇制备乙烯的反应温度是120℃。某兴趣小组据此设计如下图所示实验,合成无水 并完成乙烯的制备及收集。
并完成乙烯的制备及收集。
Ⅰ.无水 的制备
的制备
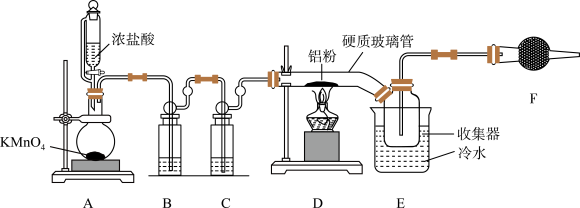
(1)装置A中发生的化学方程式为___________ 。
(2)硬质玻璃管直接接入收集器的优点是___________ 。
(3)装置F中的药品名称是___________ 。
Ⅱ.乙烯的制备及收集
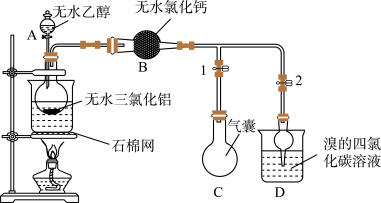
实验过程:检验装置气密性后,在圆底烧瓶中加入5g无水三氯化铝和10mL无水乙醇,点燃酒精灯加热。
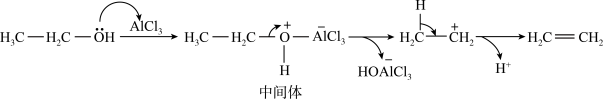
(4)该催化机理如下图所示,写出此反应历程中生成 的反应方程式
的反应方程式___________ 。
(5)实验装置中还缺少的仪器是___________ 。加入药品后,开始实验前,应先打开止水夹___________ (填“1”、“2”或“1和2”),反应进行一段时间后,出现现象___________ ,再关闭相应止水夹。
(6)B中无水氯化钙的作用是___________ 。
(7)与教材中用乙醇和浓硫酸制备乙烯相比,用三氯化铝做催化剂制备乙烯的优点有___________ (任写两点)。
 并完成乙烯的制备及收集。
并完成乙烯的制备及收集。Ⅰ.无水
 的制备
的制备
(1)装置A中发生的化学方程式为
(2)硬质玻璃管直接接入收集器的优点是
(3)装置F中的药品名称是
Ⅱ.乙烯的制备及收集

实验过程:检验装置气密性后,在圆底烧瓶中加入5g无水三氯化铝和10mL无水乙醇,点燃酒精灯加热。
(4)该催化机理如下图所示,写出此反应历程中生成
 的反应方程式
的反应方程式
(5)实验装置中还缺少的仪器是
(6)B中无水氯化钙的作用是
(7)与教材中用乙醇和浓硫酸制备乙烯相比,用三氯化铝做催化剂制备乙烯的优点有
您最近一年使用:0次
10 . 实验室可用酒精、浓硫酸作试剂来制取乙烯,但实验表明,还有许多副反应发生,如反应中会生成 、
、 、水蒸气等无机物,某研究性学习小组欲用如图所示的装置制备纯净的乙烯并探究乙烯与单质溴能否反应及反应类型,回答下列问题:
、水蒸气等无机物,某研究性学习小组欲用如图所示的装置制备纯净的乙烯并探究乙烯与单质溴能否反应及反应类型,回答下列问题:

(1)写出制备乙烯反应的化学方程式:___________ ,实验中,加热F装置时必须使液体温度___________ 。
(2)写出浓硫酸与酒精直接反应生成上述无机副产物的化学方程式:___________ 。
(3)为实现上述实验目的,装置的连接顺序为F→___________ →D,(各装置限用一次)
(4)当C中观察到___________ 时,表明单质溴能与乙烯反应;当D中___________ 时,表明C中发生的是取代反应;若D没有出现前面所描述的现象时,表明C中发生的是___________ 反应。
 、
、 、水蒸气等无机物,某研究性学习小组欲用如图所示的装置制备纯净的乙烯并探究乙烯与单质溴能否反应及反应类型,回答下列问题:
、水蒸气等无机物,某研究性学习小组欲用如图所示的装置制备纯净的乙烯并探究乙烯与单质溴能否反应及反应类型,回答下列问题:
(1)写出制备乙烯反应的化学方程式:
(2)写出浓硫酸与酒精直接反应生成上述无机副产物的化学方程式:
(3)为实现上述实验目的,装置的连接顺序为F→
(4)当C中观察到
您最近一年使用:0次