2023高二下·北京·期中
名校
1 . 下列实验能达到实验目的的是
A.制取乙烯 | B.检验1-溴丁烷的消去产物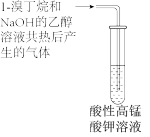 |
C.检验乙炔具有还原性 | D.鉴别甲苯与己烷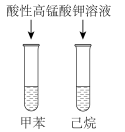 |
您最近一年使用:0次
2 . 青蒿素(分子结构: )是高效的抗疟药,为无色针状晶体,易溶于有机溶剂,难溶于水,熔点为156~157℃,温度超过60℃完全失去药效(已知:乙醚沸点为35℃)。
)是高效的抗疟药,为无色针状晶体,易溶于有机溶剂,难溶于水,熔点为156~157℃,温度超过60℃完全失去药效(已知:乙醚沸点为35℃)。
Ⅰ.从青蒿中提取青蒿素的一种工艺如图:

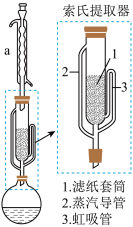
索氏提取装置如图所示。实验时烧瓶中溶剂受热蒸发,蒸汽沿蒸汽导管2上升至装置a,冷凝后滴入滤纸套筒1中,与青蒿粉末接触,进行萃取。萃取液液面达到虹吸管3顶端时,经虹吸管3返回烧瓶,从而实现对青蒿粉末的连续萃取。回答下列问题:
(1)实验前要对青蒿进行粉碎,其目的是___________ 。
(2)装置a的名称为___________ 。
(3)索氏提取装置提取的青蒿素位于___________ (填“圆底烧瓶”或“索氏提取器”)中;与常规的萃取相比,索氏提取的优点是___________ 。
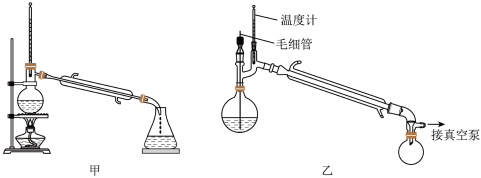
(4)提取液蒸馏过程中选用下列哪种装置更好___________ (填“甲”或“乙”),原因是___________ 。
Ⅱ.测定产品中青蒿素的纯度:
取青蒿素样品8.0 g配制成250 mL溶液,取25.00 mL加入锥形瓶中,再加入足量的KI溶液和几滴淀粉溶液,用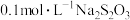 标准液滴定。
标准液滴定。
已知:①青蒿素分子中含有过氧键,与碘化钠反应生成碘单质;
② ;
;
③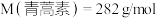 。
。
(5)滴定终点的颜色变化为___________ 。
(6)三次滴定数据记录如表:
则青蒿素的纯度为___________ 。
 )是高效的抗疟药,为无色针状晶体,易溶于有机溶剂,难溶于水,熔点为156~157℃,温度超过60℃完全失去药效(已知:乙醚沸点为35℃)。
)是高效的抗疟药,为无色针状晶体,易溶于有机溶剂,难溶于水,熔点为156~157℃,温度超过60℃完全失去药效(已知:乙醚沸点为35℃)。Ⅰ.从青蒿中提取青蒿素的一种工艺如图:

索氏提取装置如图所示。实验时烧瓶中溶剂受热蒸发,蒸汽沿蒸汽导管2上升至装置a,冷凝后滴入滤纸套筒1中,与青蒿粉末接触,进行萃取。萃取液液面达到虹吸管3顶端时,经虹吸管3返回烧瓶,从而实现对青蒿粉末的连续萃取。回答下列问题:

(1)实验前要对青蒿进行粉碎,其目的是
(2)装置a的名称为
(3)索氏提取装置提取的青蒿素位于
(4)提取液蒸馏过程中选用下列哪种装置更好

Ⅱ.测定产品中青蒿素的纯度:
取青蒿素样品8.0 g配制成250 mL溶液,取25.00 mL加入锥形瓶中,再加入足量的KI溶液和几滴淀粉溶液,用
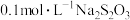 标准液滴定。
标准液滴定。已知:①青蒿素分子中含有过氧键,与碘化钠反应生成碘单质;
②
 ;
;③
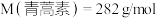 。
。(5)滴定终点的颜色变化为
(6)三次滴定数据记录如表:
| 滴定次数 | 待测液体(mL) | 标准液读数(mL) | |
| 滴定前读数 | 滴定后读数 | ||
| 第一次 | 25.00 | 1.50 | 41.52 |
| 第二次 | 25.00 | 3.00 | 42.98 |
| 第三次 | 25.00 | 4.50 | 41.60 |
您最近一年使用:0次
名校
解题方法
3 . 溴乙烷是一种重要的有机化工原料,其沸点为38.4℃,制备溴乙烷的一种方法是乙醇与氢溴酸反应。
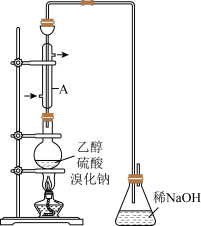
实际通常是用溴化钠固体与一定浓度的硫酸以及乙醇起反应。某课外化学兴趣小组欲在实验室制备溴乙烷(装置如图),实验操作步骤如下:
①检查装置的气密性;
②在圆底烧瓶中加入95%乙醇、80%硫酸,然后加入研细的溴化钠粉末和几小块碎瓷片;
③小心加热,使其充分反应。回答下列问题:
(1)装置A的作用是_______ ,加入碎瓷片的作用是_______ 。
(2)反应结束后,得到的粗产品呈棕黄色。为了除去粗产品中的棕黄色杂质,可选用_______ (填试剂名称)除杂,并进行_______ 操作(填实验操作名称)。
(3)要进一步制得纯净的溴乙烷,可继续用蒸馏水进行洗涤、分液,然后再加入无水 ,最后进行
,最后进行_______ 操作(填实验操作名称)。
(4)为了检验溴乙烷中含有溴元素,_______ (填“能”或“不能”)直接向溴乙烷中滴加硝酸银溶液来检验,其原因是_______ 。通常采用的方法是取少量溴乙烷,然后_______ (按实验的操作顺序选填下列序号)。
①加热 ②加入 溶液 ③加入稀
溶液 ③加入稀 酸化 ④加入NaOH溶液
酸化 ④加入NaOH溶液

实际通常是用溴化钠固体与一定浓度的硫酸以及乙醇起反应。某课外化学兴趣小组欲在实验室制备溴乙烷(装置如图),实验操作步骤如下:
①检查装置的气密性;
②在圆底烧瓶中加入95%乙醇、80%硫酸,然后加入研细的溴化钠粉末和几小块碎瓷片;
③小心加热,使其充分反应。回答下列问题:
(1)装置A的作用是
(2)反应结束后,得到的粗产品呈棕黄色。为了除去粗产品中的棕黄色杂质,可选用
(3)要进一步制得纯净的溴乙烷,可继续用蒸馏水进行洗涤、分液,然后再加入无水
 ,最后进行
,最后进行(4)为了检验溴乙烷中含有溴元素,
①加热 ②加入
 溶液 ③加入稀
溶液 ③加入稀 酸化 ④加入NaOH溶液
酸化 ④加入NaOH溶液
您最近一年使用:0次
4 . α-呋喃丙烯酸是一种重要的有机酸,其实验室制备原理如下:
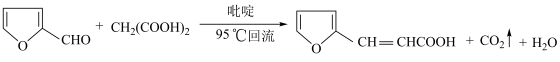
制备α-呋喃丙烯酸的步骤如下:向三颈烧瓶中依次加入丙二酸、糠醛和吡啶,在95℃下回流2小时,停止反应;将混合物倒入冷的3 盐酸中析出淡黄色沉淀,将其置于冰水中1小时,过滤,用水洗涤2-3次,得到粗产品。实验装置如图所示。
盐酸中析出淡黄色沉淀,将其置于冰水中1小时,过滤,用水洗涤2-3次,得到粗产品。实验装置如图所示。
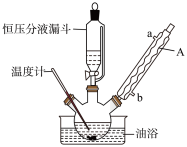
下列说法正确的是

制备α-呋喃丙烯酸的步骤如下:向三颈烧瓶中依次加入丙二酸、糠醛和吡啶,在95℃下回流2小时,停止反应;将混合物倒入冷的3
 盐酸中析出淡黄色沉淀,将其置于冰水中1小时,过滤,用水洗涤2-3次,得到粗产品。实验装置如图所示。
盐酸中析出淡黄色沉淀,将其置于冰水中1小时,过滤,用水洗涤2-3次,得到粗产品。实验装置如图所示。
下列说法正确的是
| A.仪器A的a口为进水口 |
| B.不产生气泡时表明三颈烧瓶中反应已完成 |
| C.冷的盐酸和冰水的主要作用是提高晶体纯度 |
| D.过滤后洗涤时,向漏斗中注满蒸馏水并不断搅拌 |
您最近一年使用:0次
2023-04-24更新
|
64次组卷
|
11卷引用:安徽省河南省皖豫名校联盟体2022届高三下学期第三次考试理综化学试题
安徽省河南省皖豫名校联盟体2022届高三下学期第三次考试理综化学试题(已下线)卷06 小题仿真卷-【小题小卷】冲刺2022年高考化学小题限时集训(全国卷专用)江西省南昌市八一中学2022届高三下学期第三次模拟考试理科综合化学试题河南省南阳一中2022-2023学年高三上学期第一次阶段性考试化学试题(已下线)微专题46 常见有机物的制备实验-备战2023年高考化学一轮复习考点微专题(已下线)河南省湘豫名校联考2022-2023学年高三上学期12月期末摸底考试变式汇编(9-16)(已下线)湖北省七市(州)2023届高三3月联合统一调研测试化学试题变式题(选择题11-15)山西省晋城市第一中学校2022-2023学年高二下学期4月月考化学试题(已下线)T8-化学实验基础(已下线)T9-实验方案的设计与评价云南省宣威市第六中学2023-2024学年高二上学期11月月考化学试题
名校
解题方法
5 . 实验室用如图所示装置来制备乙炔,并验证乙炔的某些化学性质,制备的乙炔气体中往往含有少量的H2S气体,请按下列要求填空:
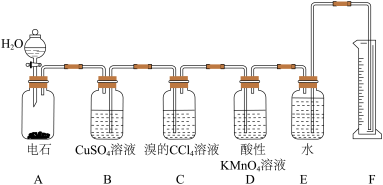
(1)实验室制乙炔的化学方程式是_______ ;为了得到较为平稳的乙炔气流,装置A的分液漏斗中常用_______ 来代替水。
(2)装置C中观察到的现象是_______ ,反应的化学方程式是_______ 。
(3)装置D中观察到的现象是_______ ,该反应的类型_______ 。

(1)实验室制乙炔的化学方程式是
(2)装置C中观察到的现象是
(3)装置D中观察到的现象是
您最近一年使用:0次
解题方法
6 . 苯的硝化反应的实验装置如图所示,苯与浓硝酸、浓硫酸的混合物在50~60℃时生成硝基苯,当温度升高至100~110℃时,生成二硝基苯。下列说法正确的是
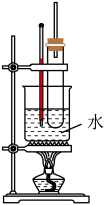
| A.添加试剂的先后顺序为浓硫酸、苯、浓硝酸 |
| B.长玻璃导管的作用为冷凝回流 |
| C.图示装置的生成物主要为二硝基苯 |
| D.硝化反应属于加成反应 |
您最近一年使用:0次
2023-04-24更新
|
239次组卷
|
3卷引用:重庆市2022-2023学年高二下学期期中考试化学试题
名校
解题方法
7 . 实验室将乙酸、1-丁醇、浓硫酸混合物加热到120℃左右制取乙酸丁酯,实验装置有以下甲,乙两种装置可供选用。
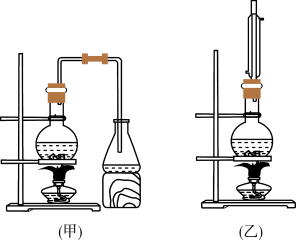
制备乙酸丁酯所涉及的有关物质的物理性质见表。
(1)浓硫酸的作用是______ ;若用同位素18O示踪法确定反应产物水分子中氧原子的提供者,写出能表示18O位置的化学方程式______ 。
(2)该实验生成物中除了乙酸丁酯外,写出两种还可能生成的有机副产物 (写结构简式)______ 。
(3)制取乙酸丁酯的装置应选用______ (填“甲”或“乙”)。不选另一种装置的理由是_____ 。
(4)实验中加入稍过量的乙酸,目的是_____ ,为达成该目的,还可以采用的方法是_____ 。
制备乙酸丁酯所得的混合物中分离、提纯乙酸丁酯时,需要经过多步操作。
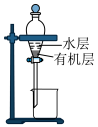
(5)反应结束并冷却后,先将水层和有机层分离,其操作名称是______ ,必须的玻璃仪器有______ 。
(6)为进一步除去有机层中的乙酸,可加入的试剂是______ 。
(7)在一系列的操作中,必须的装置是______ 。

制备乙酸丁酯所涉及的有关物质的物理性质见表。
| 乙酸 | 1-丁醇 | 乙酸丁酯 | |
| 熔点(℃) | 16.6 | -89.5 | -73.5 |
| 沸点(℃) | 117.9 | 117 | 126.3 |
| 密度(g•cm-3) | 1.05 | 0.81 | 0.88 |
| 水溶性 | 互溶 | 可溶(9g/100g水) | 微溶 |
(2)该实验生成物中除了乙酸丁酯外,写出两种还可能生成的
(3)制取乙酸丁酯的装置应选用
(4)实验中加入稍过量的乙酸,目的是
制备乙酸丁酯所得的混合物中分离、提纯乙酸丁酯时,需要经过多步操作。
(5)反应结束并冷却后,先将水层和有机层分离,其操作名称是
(6)为进一步除去有机层中的乙酸,可加入的试剂是
| A.1—丁醇 | B.乙醇 | C.NaOH溶液 | D.Na2CO3溶液 |
A.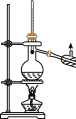 | B. | C.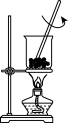 | D.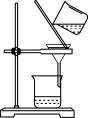 |
您最近一年使用:0次
名校
解题方法
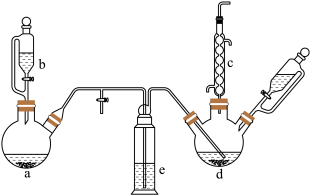
8 . 氯苯在染料、医药工业中用于制造苯酚、硝基氯苯、苯胺硝基酚等有机中间体。实验室中制备氯苯的装置如图所示(夹持仪器已略去)。请回答下列问题:_____ 。与普通分液漏斗相比,仪器b的优点是______ 。
(2)仪器d内盛有苯、FeCl3粉末,仪器a中生成的气体经过仪器e进入到仪器d中。
①仪器e是洗气瓶,瓶内盛装的试剂是______ 。
②仪器d中的反应进行过程中,保持温度在40~60℃,以减少副反应发生。仪器d的加热方式最好采用______ 加热。
(3)仪器c的作用是______ ;d中发生反应的化学方程式是______ 。
(4)该方法制备的氯苯中含有很多杂质,工业生产中通过水洗、碱洗、再水洗,最后通过分液得到含氯苯的混合物,该混合物的成分及各成分的沸点如表所示:
①碱洗前先进行水洗的目的是______ 。
②提取该混合物中的氯苯时,采用蒸馏的方法,收集_____ ℃左右的馏分。
(2)仪器d内盛有苯、FeCl3粉末,仪器a中生成的气体经过仪器e进入到仪器d中。
①仪器e是洗气瓶,瓶内盛装的试剂是
②仪器d中的反应进行过程中,保持温度在40~60℃,以减少副反应发生。仪器d的加热方式最好采用
(3)仪器c的作用是
(4)该方法制备的氯苯中含有很多杂质,工业生产中通过水洗、碱洗、再水洗,最后通过分液得到含氯苯的混合物,该混合物的成分及各成分的沸点如表所示:
| 有机物 | 苯 | 氯苯 | 邻二氯苯 | 间二氯苯 | 对二氯苯 |
| 沸点/℃ | 80 | 132.2 | 180.4 | 172.0 | 173.4 |
②提取该混合物中的氯苯时,采用蒸馏的方法,收集
您最近一年使用:0次
2023-04-23更新
|
496次组卷
|
4卷引用:山东省德州市第一中学2022-2023学年高二下学期4月期中化学试题
9 . 知:①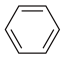 +HNO3
+HNO3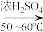
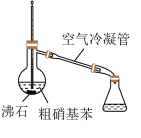
 +H2O △H<0;②硝基苯沸点为210.9℃,蒸馏时选用空气冷凝管。下列制取硝基苯的操作或装置(部分夹持装置略去),正确的是
+H2O △H<0;②硝基苯沸点为210.9℃,蒸馏时选用空气冷凝管。下列制取硝基苯的操作或装置(部分夹持装置略去),正确的是
 +HNO3
+HNO3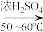
 +H2O △H<0;②硝基苯沸点为210.9℃,蒸馏时选用空气冷凝管。下列制取硝基苯的操作或装置(部分夹持装置略去),正确的是
+H2O △H<0;②硝基苯沸点为210.9℃,蒸馏时选用空气冷凝管。下列制取硝基苯的操作或装置(部分夹持装置略去),正确的是A | B | C | D |
|
|
|
|
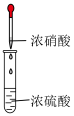
分液 | 配制混酸 | 水浴加热 | 蒸馏提纯 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-04-23更新
|
629次组卷
|
17卷引用:福建省莆田市2020年3月高三毕业班教学质量检测试理综化学试题
福建省莆田市2020年3月高三毕业班教学质量检测试理综化学试题山东省淄博市2020届高三下学期第二次网考化学试题(已下线)2020年高考化学押题预测卷01(山东卷)-《2020年高考押题预测卷》天津市第一中学2020届高三下学期第五次月考化学试题(已下线)第一单元 有机化合物的结构与性质 烃(基础过关)-2020-2021学年高二化学单元测试定心卷(鲁科版选修5)(已下线)【镇江新东方】高二上第一次月考一中三校联考福建省宁德市2020-2021学年高二下学期期末考试化学试题福建省莆田二中、晋江一中、南安一中2019-2020学年高二下学期三校期末联考化学试题辽宁省沈阳市二十七中学2021-2022学年高二下学期4月月考化学试题广东实验中学2021-2022学年高二下学期期中考试化学试题四川省成都市树德中学2021-2022学年高一下学期5月阶段性测试化学试题吉林省实验中学2021-2022学年高二下学期第三次月考化学试题福建省连城县第一中学2021-2022学年高二下学期月考(二)化学试题广东省广州中学2022-2023学年高二下学期期中考试化学试题山东省德州市第一中学2022-2023学年高二下学期4月期中化学试题河北省承德市双滦区实验中学2023-2024学年高二上学期期中考试化学试题山东省泰安第一中学2023-2024学年高二下学期3月月考化学试题
名校
解题方法
10 . 某研究小组用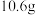 苯甲醛制备苯甲醇与苯甲酸,发生如下反应:
苯甲醛制备苯甲醇与苯甲酸,发生如下反应:
(苯甲醛)2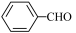
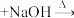 (苯甲醇)
(苯甲醇)

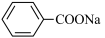
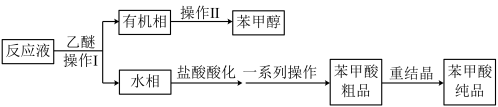
充分反应后,将所得到的反应液按如图步骤处理:
下表列出了有关物质的部分物理性质:
(1)操作I用到的关键仪器名称为_______ 。
(2)操作Ⅱ为蒸馏,蒸馏装置如下图所示,其中温度计所处的正确位置是_______ (填“a”或“b”或“c”)。方框甲内未画出的仪器为_______ 。

(3)重结晶过程为热水溶解 活性炭脱色
活性炭脱色 趁热过滤
趁热过滤 冷却结晶
冷却结晶 过滤
过滤 洗涤
洗涤 干燥。其中趁热过滤的目的是
干燥。其中趁热过滤的目的是_______ 。
(4)下列仪器中,可鉴别苯甲酸和苯甲醇的是_______。
(5)最终得到苯甲酸产品 ,则苯甲酸的产率为
,则苯甲酸的产率为_______ %(保留小数点后1位)。(产率 )
)
(6)如何检验重结晶后的苯甲酸晶体中,无机物杂质是否完全除尽?写出实验方案的具体操作_______ 。
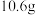 苯甲醛制备苯甲醇与苯甲酸,发生如下反应:
苯甲醛制备苯甲醇与苯甲酸,发生如下反应: (苯甲醛)2

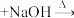 (苯甲醇)
(苯甲醇)

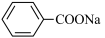
充分反应后,将所得到的反应液按如图步骤处理:

下表列出了有关物质的部分物理性质:
| 物质 | 相对分子质量 | 溶解性 |
| 苯甲醇 | 108 | 在水中溶解度较小,易溶于醚、醇 |
| 苯甲醛 | 106 | 微溶于水,易溶于醇、醚 |
| 苯甲酸 | 122 | 苯甲酸微溶于冷水,易溶于醚、醇 |
(2)操作Ⅱ为蒸馏,蒸馏装置如下图所示,其中温度计所处的正确位置是

(3)重结晶过程为热水溶解
 活性炭脱色
活性炭脱色 趁热过滤
趁热过滤 冷却结晶
冷却结晶 过滤
过滤 洗涤
洗涤 干燥。其中趁热过滤的目的是
干燥。其中趁热过滤的目的是(4)下列仪器中,可鉴别苯甲酸和苯甲醇的是_______。
| A.元素分析仪 | B.红外光谱仪 | C.质谱仪 | D.核磁共振氢谱 |
 ,则苯甲酸的产率为
,则苯甲酸的产率为 )
)(6)如何检验重结晶后的苯甲酸晶体中,无机物杂质是否完全除尽?写出实验方案的具体操作
您最近一年使用:0次
2023-04-23更新
|
445次组卷
|
2卷引用:浙江省杭州第二中学等四校联盟2022-2023学年高二下学期期中考试化学试题