17. Al、Fe、Cu是重要的材料元素,在生产生活中有着广泛的应用。回答下列问题:
(1)Fe
4[Fe(CN)
6]
3是较早发现的CN
-配合物,其中铁元素呈现两种不同的价态。配离子的中心原子核外电子排布式为
___。
(2)铁单质在一定条件下可与CO反应生成配位化合物——羰基铁[Fe(CO)
5],沸点102.8℃,熔点-21℃,羰基铁[Fe(CO)
5]属于
___晶体。从电负性角度分析,Fe(CO)
5中与Fe形成配位键的是原子
___(填名称)。
(3)已知Al的第一电离能为578 kJ/mol、第二电离能为1817 kJ/mol、第三电离能为2745 kJ/mol、第四电离能为11575 kJ/mol。请解释其第二电离能增幅较大的原因
___。
(4)甲醇重整制氢反应中,铜基催化剂如CuO/SiO
2具有重整温度低、催化选择性高的优点。Cu、Si、O元素电负性由大到小的顺序是
___;SiO
2中Si原子采取
___杂化。
(5)金刚砂(SiC)晶胞如图所示:
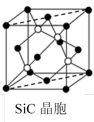
沿晶胞图中虚线方向的切面图为
___(填标号)。
a.
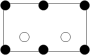
b.
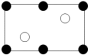
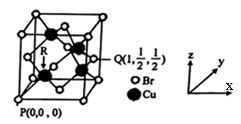
(6)一种铜的溴化物晶胞结构如图所示,该晶胞中铜的配位数是
___,由图中P点和Q点的原子坐标参数可确定R点的原子坐标参数为
___;已知晶胞参数为a pm,其密度为
___g/cm
3。(列出计算式即可)