江西省南昌市第二中学、临川市第一中学2017届高三下学期期中联考理综化学试题
江西
高三
期中
2017-07-07
303次
整体难度:
适中
考查范围:
认识化学科学、化学与STSE、有机化学基础、化学实验基础、物质结构与性质、化学反应原理、常见无机物及其应用
江西省南昌市第二中学、临川市第一中学2017届高三下学期期中联考理综化学试题
江西
高三
期中
2017-07-07
303次
整体难度:
适中
考查范围:
认识化学科学、化学与STSE、有机化学基础、化学实验基础、物质结构与性质、化学反应原理、常见无机物及其应用
一、单选题 添加题型下试题
单选题
|
较易(0.85)
名校
1. 《诗词大会》不仅弘扬了中国传统文化,还蕴含了许多化学知识。下列说法不合理的是( )
| A.李白的诗句:“日照香炉生紫烟,遥看瀑布挂前川。”生紫烟包含了物理变化。 |
| B.“熬胆矾铁釜,久之亦化为铜”,北宋沈括用胆矾炼铜的过程属于置换反应 |
| C.唐末五代时期丹学著作《元妙道要略》中有云“以硫黄、雄黄台硝石并蜜烧之;焰起,烧手面及烬屋舍者”。描述的是丹药的制作过程 |
| D.古剑沈卢“以济钢为刃,柔铁为茎干,不尔则多折断”。济钢为钢铁。 |
您最近一年使用:0次
2019-06-04更新
|
186次组卷
|
7卷引用:江西省南昌市第二中学、临川市第一中学2017届高三下学期期中联考理综化学试题
单选题
|
适中(0.65)
2. 设NA为阿伏伽德罗常数值。下列有关叙述不正确的是:
| A.5.8g熟石膏(2CaSO4·H2O)含有的结晶水分子数为0.02NA |
| B.在K37ClO3+6H35Cl(浓)=KCl+3Cl2↑+3H2O反应中,若有212克氯气生成,则反应中电子转移的数目为5NA |
| C.60克的乙酸和葡萄糖混合物充分燃烧消耗2NA个O2 |
| D.1mol CnH2n-2(n≥2)中所含的共用电子对数为(3n+1)NA |
【知识点】 阿伏加德罗常数的应用解读
您最近一年使用:0次
单选题
|
适中(0.65)
名校
解题方法
3. 法国、美国、荷兰的三位科学家因研究“分子机器的设计与合成”获得2016年诺贝尔化学奖。轮烷是一种分子机器的“轮子”,轮烷的一种合成原料由C、H、O三种元素组成,其球棍模型如图所示,下列说法正确的是
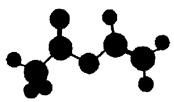

| A.该化合物的名称为乙酸乙酯 |
| B.该化合物与Br2的四氯化碳溶液不反应 |
| C.该化合物能发生水解反应,不能发生加聚反应 |
| D.该化合物的链状同分异构体中,能与NaHCO3反应放出CO2的只有3种 |
您最近一年使用:0次
2017-03-20更新
|
610次组卷
|
7卷引用:2017届河北省武邑中学高三下学期第二次质检考试理科综合化学试卷
单选题
|
适中(0.65)
名校
4. 下列依据实验操作及现象得出的结论正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向亚硫酸钠试样中滴入盐酸酸化的Ba(ClO)2 溶液 | 产生白色 沉淀 | 试样已氧化变质 |
| B | 向Co2O3中滴入浓盐酸 | 产生黄绿色 气体 | 氧化性: Co2O3>Cl2 |
| C | 向待测液中依次滴入氯水和KSCN溶液 | 溶液变为 红色溶液 | 待测液中含有Fe2+ |
| D | 向Na2SO4和Na2CO3混合溶液中滴入AgNO3 溶液 | 产生白色 浑浊 | Ksp(Ag2SO4)<Ksp(Ag2CO3) |
| A.A | B.B | C.C | D.D |
【知识点】 化学实验方案的设计与评价
您最近一年使用:0次
2017-03-20更新
|
247次组卷
|
6卷引用:2017届河北省武邑中学高三下学期第二次质检考试理科综合化学试卷
单选题
|
适中(0.65)
解题方法
5. W、X、Y、Z是原子序数依次最大的短周期元素,W的原子半径最小,W、Y同主族,X、Z同主族,X、Z的原子序数之和是W、Y原子序数之和的2倍,下列说法中不正确的是
| A.由X、Y、Z三种元素形成的化合物只能为Y2ZX3或Y2ZX4 |
| B.由W和X两种元素形成的化合物可能含有非极性共价键 |
| C.由W、X、Y、Z四种元素形成的化合物水溶液可能呈强酸性 |
| D.W、X、Y、Z四种元素两两之间形成二元化合物 |
您最近一年使用:0次
单选题
|
适中(0.65)
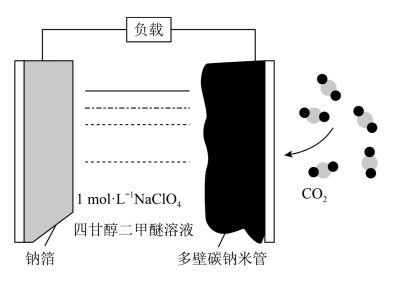
6. 可充电“钠-二氧化碳”电池(如图),电池总反应为:4Na+3CO2 2Na2CO3+C。下列说法错误的是
2Na2CO3+C。下列说法错误的是
 2Na2CO3+C。下列说法错误的是
2Na2CO3+C。下列说法错误的是
| A.放电时,Na+向正极移动 |
| B.放电时,电子从钠箔经负载流向多壁纳米碳管 |
| C.充电时,钠箔和外接电源的负极相连,发生氧化反应 |
| D.充电时,阳极的电极反应为:2Na2CO3+C-4e-=4Na++3CO2↑ |
【知识点】 二次电池 新型电池解读 原电池、电解池综合考查解读
您最近一年使用:0次
2017-04-09更新
|
363次组卷
|
3卷引用:2017届四川省资阳市高三4月模拟考理综化学试卷
单选题
|
较难(0.4)
7. 部分弱酸的电离常数如下表:
下列有关说法正确的是
弱酸 | HCOOH | HCN | H2S |
电离平衡常数(25℃) | Ka=1.8×10-4 | Ka=4.9 X 10-10 | Ka1=1.3×10-7 Ka2=7.1×10-15 |
| A.恰好中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者大于后者 |
| B.HCOO-、CN-、HS-在溶液中不可以大量共存 |
| C.NaHS溶液中加入适量KOH后:c (Na+)=c (H2S) +c (HS-) +2c (S2-) |
| D.等体积、等浓度的HCOONa和NaCN两溶液中所含离子总数目HCOONa大于NaCN |
您最近一年使用:0次
2017-04-26更新
|
296次组卷
|
2卷引用:江西省南昌市第二中学、临川市第一中学2017届高三下学期期中联考理综化学试题
二、解答题 添加题型下试题
解答题-实验探究题
|
适中(0.65)
8. 镁是一种性质活泼的金属,请回答下列问题:
(1)甲组同学通过实验探究Mg能否在CO2气体中燃烧,将镁条在空气中点燃后迅速插入盛有CO2气体的集气瓶中,观察到镁条剧烈燃烧,瓶内壁出现黑色固体颗粒等现象。写出Mg在CO2中燃烧的化学方程式:__________
(2)乙组同学根据甲组实验,推测Mg也能在NO2中燃烧,可能产物为MgO 、Mg3N2、和N2。请通过下图所给装置及药品来验证反应产物(夹持装置省略,部分仪器可重复使用)。
已知:a. Mg3N2遇水强烈水解。
b. NO2气体能被NaOH吸收。
c.25℃时,电离常数:CH3COOH的Ka=1.8×10-5NH3·H2O的Ka=1.8×10-5
回答下列问题:
①乙组同学实验装置连接的正确顺序为A→__________ (填装置字母);装置C中盛放的试剂是________ 。
②当实验过程中出现_________ 现象时,才能开始加热,确定产物中有N2生成的实验现象为_________ 。
③装置D中生成两种物质的量相等的钠盐,其离子方程式为___________ 。
(3)设计实验证明:
①产物中存在Mg3N2:__________________ 。
②Mg(OH)2与NH4+直接反应而溶解:_____________ 。
(1)甲组同学通过实验探究Mg能否在CO2气体中燃烧,将镁条在空气中点燃后迅速插入盛有CO2气体的集气瓶中,观察到镁条剧烈燃烧,瓶内壁出现黑色固体颗粒等现象。写出Mg在CO2中燃烧的化学方程式:
(2)乙组同学根据甲组实验,推测Mg也能在NO2中燃烧,可能产物为MgO 、Mg3N2、和N2。请通过下图所给装置及药品来验证反应产物(夹持装置省略,部分仪器可重复使用)。
已知:a. Mg3N2遇水强烈水解。
b. NO2气体能被NaOH吸收。
c.25℃时,电离常数:CH3COOH的Ka=1.8×10-5NH3·H2O的Ka=1.8×10-5
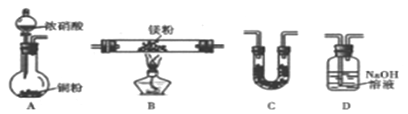
回答下列问题:
①乙组同学实验装置连接的正确顺序为A→
②当实验过程中出现
③装置D中生成两种物质的量相等的钠盐,其离子方程式为
(3)设计实验证明:
①产物中存在Mg3N2:
②Mg(OH)2与NH4+直接反应而溶解:
您最近一年使用:0次
2017-03-29更新
|
179次组卷
|
2卷引用:2017届安徽省合肥市高三第二次教学质量检测理综化学试卷
解答题-工业流程题
|
较难(0.4)
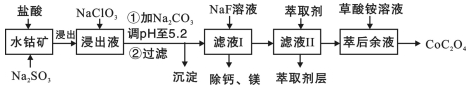
9. 草酸钴用途广泛,可用于指示剂和催化剂的制备。一种利用水钴矿[主要成分为Co2O3,含少量Fe2O3、Al2O3、MnO2、MgO、CaO等]制取草酸钴晶体(CoC2O4⋅2H2O)工艺流程如图:
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
(1)浸出过程中加入Na2SO3的离子方程式为________________________
(2)NaClO3的作用是_________________ 调PH至5.2,沉淀的主要成分为__________
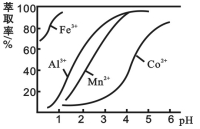
(3)萃取剂对金属离子的萃取率与pH的关系如图2所示。滤液Ⅱ中加入萃取剂的作用是___________________ ;使用萃取剂适宜的pH是_______________
A. 接近2.0 B.接近3.0 C.接近5.0
(4)除钙、镁是将溶液中Ca2+与Mg2+转化为MgF2、CaF2沉淀,已知Ksp(MgF2)=7.35×10−11、Ksp(CaF2)=1.05×10−10.当加入过量NaF后,所得滤液c(Mg2+):c(Ca2+)=________________ .
(5)已知含钴废料中含Co2O3质量分数为a%,若取mkg该含钴废料按照上述流程,理论上最多能制得草酸钴晶体的质量为_________________ g
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 完全沉淀的PH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)浸出过程中加入Na2SO3的离子方程式为
(2)NaClO3的作用是

(3)萃取剂对金属离子的萃取率与pH的关系如图2所示。滤液Ⅱ中加入萃取剂的作用是
A. 接近2.0 B.接近3.0 C.接近5.0
(4)除钙、镁是将溶液中Ca2+与Mg2+转化为MgF2、CaF2沉淀,已知Ksp(MgF2)=7.35×10−11、Ksp(CaF2)=1.05×10−10.当加入过量NaF后,所得滤液c(Mg2+):c(Ca2+)=
(5)已知含钴废料中含Co2O3质量分数为a%,若取mkg该含钴废料按照上述流程,理论上最多能制得草酸钴晶体的质量为
您最近一年使用:0次
解答题-原理综合题
|
适中(0.65)
解题方法
10. 霾天气严重影响人们的生活,其中氮氧化物和硫氧化物是造成雾霾天气的主要原因之一。消除氮氧化物和硫氧化物有多种方法。
(1)用活性炭还原法可以处理氮氧化物。某研究小组向某密闭容器中加入一定量的活性炭和NO,发生反应:C(s)+2NO(g) N2(g)+CO2(g) △H=Q kJ·mol-1。在T1℃时,反应进行到不同时间测得各物质的浓度如下:
N2(g)+CO2(g) △H=Q kJ·mol-1。在T1℃时,反应进行到不同时间测得各物质的浓度如下:
①0~10 min内,NO的平均反应速率v(NO)=_______________________ ,T1℃时,该反应的平衡常数K=____________ 。
②30 min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是_______ (填字母)。
a.升高温度 b.通入一定量的NO
c.适当缩小容器的体积 d.加入合适的催化剂
③若30 min后升高温度至T2℃,达到平衡时,容器中,NO、N2、CO2的浓度之比为5:3:3,则Q__________ (填“>”、“=”或“<”)0。
(2)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图所示:
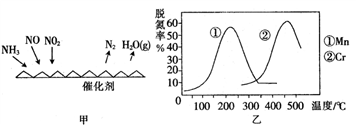
①由图甲可知,SCR技术中的氧化剂为_______________ 。已知c(NO2):c(NO)=1:1时脱氮效果最佳, 若生成1 mol N2时反应放出的热量为Q kJ。此时对应的脱氮反应的热化学方程式为__________________________
②图乙是不同催化剂Mn和Cr在不同温度下对应的脱氮率,由图可知工业使用的最佳的催化剂和相应的温度分别为___________________________ 。
(3)汽车尾气中的SO2可用石灰水来吸收,生成亚硫酸钙浊液。已知常温下Ka1(H2SO3)=1.8×10-2 , Ka2(H2SO3)=6.0×10-9。常温下,测得某纯CaSO3与水形成的浊液pH=9,忽略SO32-的第二步水解,则Ksp(CaSO3)=____________ 。
(1)用活性炭还原法可以处理氮氧化物。某研究小组向某密闭容器中加入一定量的活性炭和NO,发生反应:C(s)+2NO(g)
 N2(g)+CO2(g) △H=Q kJ·mol-1。在T1℃时,反应进行到不同时间测得各物质的浓度如下:
N2(g)+CO2(g) △H=Q kJ·mol-1。在T1℃时,反应进行到不同时间测得各物质的浓度如下:| 时间(min) 浓度(mol·L-1) | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 1.00 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
| N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
| CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
①0~10 min内,NO的平均反应速率v(NO)=
②30 min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是
a.升高温度 b.通入一定量的NO
c.适当缩小容器的体积 d.加入合适的催化剂
③若30 min后升高温度至T2℃,达到平衡时,容器中,NO、N2、CO2的浓度之比为5:3:3,则Q
(2)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图所示:

①由图甲可知,SCR技术中的氧化剂为
②图乙是不同催化剂Mn和Cr在不同温度下对应的脱氮率,由图可知工业使用的最佳的催化剂和相应的温度分别为
(3)汽车尾气中的SO2可用石灰水来吸收,生成亚硫酸钙浊液。已知常温下Ka1(H2SO3)=1.8×10-2 , Ka2(H2SO3)=6.0×10-9。常温下,测得某纯CaSO3与水形成的浊液pH=9,忽略SO32-的第二步水解,则Ksp(CaSO3)=
您最近一年使用:0次
解答题-结构与性质
|
较难(0.4)
名校
解题方法
11. 磷是人体含量较多的元素之一,磷的化合物在药物生产和农药制造等方面用途非常广泛。回答下列问题:
(1)基态磷原子的核外电子排布式为____________________ 。
(2)P4S3可用于制造火柴,其分子结构如图甲所示。
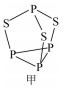
①第一电离能:磷_____________ 硫;电负性:磷_____________ 硫(填“>”或“<”)。
②P4S3分子中硫原子的杂化轨道类型为_____________ 。
③每个P4S3分子中含孤电子对的数目为______________ 。
(3)N、P、As、Sb均是第VA族的元素。
①上述元素的氢化物的沸点关系如图乙所示,沸点:PH3<NH3,其原因是____________ ;沸点:PH3<AsH3<SbH3,其原因是______________________________________ 。
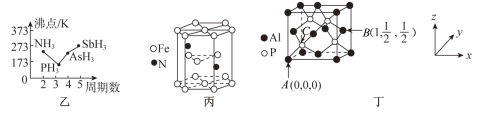
②某种磁性氮化铁的晶胞结构如图丙所示,该化合物的化学式为______ 。
(4)磷化铝熔点为2000℃,它与晶体硅互为等电子体,磷化铝晶胞结构如图丁所示。
①磷化铝晶体中磷与铝微粒间的作用力为_____________________ 。
②图中A点和B点的原子坐标参数如图丁所示,则C点的原子坐标参数为________ 。
③磷化铝晶体的密度为ρg·cm-3,用NA表示阿伏伽德罗常数的数值,则该晶胞中距离最近的两个铝原子之间的距离为___________ cm。
(1)基态磷原子的核外电子排布式为
(2)P4S3可用于制造火柴,其分子结构如图甲所示。

①第一电离能:磷
②P4S3分子中硫原子的杂化轨道类型为
③每个P4S3分子中含孤电子对的数目为
(3)N、P、As、Sb均是第VA族的元素。
①上述元素的氢化物的沸点关系如图乙所示,沸点:PH3<NH3,其原因是

②某种磁性氮化铁的晶胞结构如图丙所示,该化合物的化学式为
(4)磷化铝熔点为2000℃,它与晶体硅互为等电子体,磷化铝晶胞结构如图丁所示。
①磷化铝晶体中磷与铝微粒间的作用力为
②图中A点和B点的原子坐标参数如图丁所示,则C点的原子坐标参数为
③磷化铝晶体的密度为ρg·cm-3,用NA表示阿伏伽德罗常数的数值,则该晶胞中距离最近的两个铝原子之间的距离为
您最近一年使用:0次
2017-03-20更新
|
1450次组卷
|
7卷引用:2017届河北省武邑中学高三下学期第二次质检考试理科综合化学试卷
解答题-有机推断题
|
适中(0.65)
名校
12. 菠萝酯是一种带有浓郁的菠萝香气和香味的食用香料,其合成路线如下(部分反应条件及产物已略去):
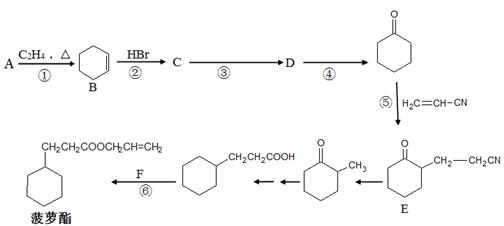
请回答下列问题:
(1) A可用于制备顺丁橡胶(顺式聚1,3-丁二烯),顺丁橡胶的结构简式为_________ ,若顺丁橡胶的平均相对分子质量为540108,则平均聚合度为__________ 。
(2) F的结构简式为__________ ,反应④的条件是________________ 。
(3) ①一⑥反应中属于取代反应的是__________ 。
(4) 下列有关B的说法正确的是__________ (填字母序号)。
(5) 写出反应③的化学方程式_________________ 。
(6) 同时满足下列条件的E的同分异构体的数目为__________ 种。
(7) 参照上述合成路线,现仅以A为有机原料,无机试剂任选,设计制备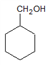 的合成路线。
的合成路线。
已知:①反应物分子的环外双键比环内双键更容易被氧化;
___________________________________________ 。

请回答下列问题:
(1) A可用于制备顺丁橡胶(顺式聚1,3-丁二烯),顺丁橡胶的结构简式为
(2) F的结构简式为
(3) ①一⑥反应中属于取代反应的是
(4) 下列有关B的说法正确的是
a. 元素分析仪可确定B的实验式为C6H10
b. 质谱仪可检测B的最大质荷比的数值为82
c. 红外光谱仪可测定B中六个碳原子一定在同一平面上
d. 核磁共振仪可测定B有两种类型氢原子吸收峰
(5) 写出反应③的化学方程式
(6) 同时满足下列条件的E的同分异构体的数目为
①遇氯化铁溶液显紫色 ②苯环上只有2个取代基且处于对位
(7) 参照上述合成路线,现仅以A为有机原料,无机试剂任选,设计制备
 的合成路线。
的合成路线。已知:①反应物分子的环外双键比环内双键更容易被氧化;
②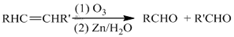 (R,R’代表烃基或氢)
(R,R’代表烃基或氢)
您最近一年使用:0次
2017-02-26更新
|
913次组卷
|
3卷引用:2016-2017学年云南省云天化中学高二上学期期末考试化学(理)试卷
试卷分析
整体难度:适中
考查范围:认识化学科学、化学与STSE、有机化学基础、化学实验基础、物质结构与性质、化学反应原理、常见无机物及其应用
试卷题型(共 12题)
题型
数量
单选题
7
解答题
5
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 物理变化与化学变化 四种基本反应类型 化学科学对人类文明发展的意义 金属与合金性能比较 | |
| 2 | 0.65 | 阿伏加德罗常数的应用 | |
| 3 | 0.65 | 有机反应类型 有机官能团的性质及结构 含碳碳双键物质的性质的推断 多官能团有机物的结构与性质 | |
| 4 | 0.65 | 化学实验方案的设计与评价 | |
| 5 | 0.65 | 元素周期表提供的元素信息 “位构性”关系理解及应用 结合物质计算的元素周期律、元素周期表相关推断 | |
| 6 | 0.65 | 二次电池 新型电池 原电池、电解池综合考查 | |
| 7 | 0.4 | 一元强酸与一元弱酸的比较 盐溶液中微粒间的电荷守恒、物料守恒、质子守恒原理 盐溶液中离子浓度大小的比较 | |
| 二、解答题 | |||
| 8 | 0.65 | 物质制备的探究 | 实验探究题 |
| 9 | 0.4 | 含氧化铝的混合物的提纯 溶度积常数相关计算 物质制备的探究 | 工业流程题 |
| 10 | 0.65 | 热化学方程式书写及正误判断 化学反应速率计算 化学平衡常数的有关计算 溶度积常数相关计算 | 原理综合题 |
| 11 | 0.4 | 电负性 分子的性质 杂化轨道理论 晶胞的有关计算 | 结构与性质 |
| 12 | 0.65 | 简单有机物同分异构体书写及辨识 有机物的合成 有机物的推断 根据题给物质选择合适合成路线 | 有机推断题 |



