解题方法
1 . 模拟工业上用黄铜灰渣(含有Cu、Zn、CuO、ZnO及少量FeO、Fe3O4、Fe2O3)生产Cu(NO3)2溶液的流程如下图所示。
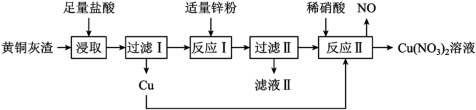
回答下列问题:
(1)写出“浸取”时Fe3O4反应的离子方程式:_______ 。
(2)过滤Ⅰ后所得滤液中是否含Fe3+,并说明理由_______ 。
(3)检验“滤液Ⅱ”中由铁元素形成的阳离子的方法是_______ 。
(4)“反应Ⅱ”所用稀硝酸可由质量分数为63%、密度为1.40g·cm-3的浓硝酸稀释获得。若要获得100mL1.4mol·L-1的稀硝酸,需要用_____ 量取浓硝酸的体积为________ mL。
(5)金属材料的使用见证了人类文明发展过程,铝合金是目前用途广泛的合金之一、例如,硬铝(一种铝合金)中含Cu 4%、Mg 0.5%、______ 0.5%、Si 0.7%,它的密度小、强度高、具有较强的抗腐蚀能力。(填元素符号)
(6)工业废电路板的铜常用FeCl3溶液来溶解处理回收。现将一块电路板浸泡在100 mL FeCl3溶液中使铜全部溶解得到浸泡液(电路板上其他物质均不发生反应),测得电路板质量减少了6.4g,在浸泡液中加足量的铁粉并使之充分反应,过滤并干燥固体,固体质量比加入的铁粉质量减少了4.8g,请回答下列问题:
①浸泡液中的溶质是________ (写化学式)。
②参与反应的铁粉的质量是______ g。
③假设溶液的体积不变,最后所得溶液c(Fe2+)=_____ mol·L-1。

回答下列问题:
(1)写出“浸取”时Fe3O4反应的离子方程式:
(2)过滤Ⅰ后所得滤液中是否含Fe3+,并说明理由
(3)检验“滤液Ⅱ”中由铁元素形成的阳离子的方法是
(4)“反应Ⅱ”所用稀硝酸可由质量分数为63%、密度为1.40g·cm-3的浓硝酸稀释获得。若要获得100mL1.4mol·L-1的稀硝酸,需要用
(5)金属材料的使用见证了人类文明发展过程,铝合金是目前用途广泛的合金之一、例如,硬铝(一种铝合金)中含Cu 4%、Mg 0.5%、
(6)工业废电路板的铜常用FeCl3溶液来溶解处理回收。现将一块电路板浸泡在100 mL FeCl3溶液中使铜全部溶解得到浸泡液(电路板上其他物质均不发生反应),测得电路板质量减少了6.4g,在浸泡液中加足量的铁粉并使之充分反应,过滤并干燥固体,固体质量比加入的铁粉质量减少了4.8g,请回答下列问题:
①浸泡液中的溶质是
②参与反应的铁粉的质量是
③假设溶液的体积不变,最后所得溶液c(Fe2+)=
您最近一年使用:0次
名校
解题方法
2 . 13.6gFe和Fe2O3的混合物,加入150mL足量的稀硫酸,在标准状况下收集到1.12LH2,向反应后的溶液中滴入KSCN溶液不变红。为中和过量的H2SO4,并使Fe元素恰好全部转化为Fe(OH)2沉淀,恰好消耗了200mL3mol/L的NaOH溶液(忽略溶液体积变化)。下列说法正确的是
| A.混合物中Fe2O3的物质的量为0.1mol |
| B.混合物中Fe的物质的量为0.5mol |
| C.原硫酸的浓度为2mol/L |
| D.与固体粉末反应的硫酸的物质的量为0.6mol |
您最近一年使用:0次
2023-03-13更新
|
378次组卷
|
3卷引用:吉林省吉林市普通高中2022-2023学年高一上学期期末考试化学试题
3 . 铟(In)是一种主要用于液晶显示屏和半导体生产的重要稀有金属。从铅、锌的冶炼过程中产生的高铟烟灰(主要含ZnO、PbO、Fe2O3、In2O3、In2S3)中提取铟的流程如图:

已知:滤液中铟以In3+的形式存在,In3+与Al3+相似,易水解。
回答下列问题:
(1)“氧化酸浸”需要加热,其目的是____ 。
(2)“氧化酸浸”时不能用浓盐酸代替硫酸,理由是____ (用化学方程式表示)。
(3)“氧化酸浸”过程中In2S3的硫元素被氧化为SO ,滤渣除含过量MnO2外,还有
,滤渣除含过量MnO2外,还有____ (填化学式)。
(4)“萃取”过程中的萃取剂可用H2A2表示,使In3+进入有机相,萃取过程In3+发生的反应方程式为:In3++3H2A2 In(HA2)3+3H+,平衡常数为K。“萃取”时萃取率的高低受溶液的pH影响很大,已知与萃取率(E%)的关系符合如下公式:lg
In(HA2)3+3H+,平衡常数为K。“萃取”时萃取率的高低受溶液的pH影响很大,已知与萃取率(E%)的关系符合如下公式:lg =lgK-lg
=lgK-lg 。当pH=2.30时,萃取率为50%,若将萃取率提升到95%,应调节溶液的pH=
。当pH=2.30时,萃取率为50%,若将萃取率提升到95%,应调节溶液的pH=____ (已知lg19=1.28忽略萃取剂浓度的变化,结果保留三位有效数字)。
(5)盐酸的浓度与铟、铁的反萃取率的关系如图所示。则“反萃取”过程中应选择盐酸的最佳浓度为____ mol•L-1。

(6)“置换”后所得浊液,需要经过过滤、洗涤、干燥等操作得到粗铟,在洗涤操作中,检验粗铟已洗涤干净的方法为____ 。

已知:滤液中铟以In3+的形式存在,In3+与Al3+相似,易水解。
回答下列问题:
(1)“氧化酸浸”需要加热,其目的是
(2)“氧化酸浸”时不能用浓盐酸代替硫酸,理由是
(3)“氧化酸浸”过程中In2S3的硫元素被氧化为SO
 ,滤渣除含过量MnO2外,还有
,滤渣除含过量MnO2外,还有(4)“萃取”过程中的萃取剂可用H2A2表示,使In3+进入有机相,萃取过程In3+发生的反应方程式为:In3++3H2A2
 In(HA2)3+3H+,平衡常数为K。“萃取”时萃取率的高低受溶液的pH影响很大,已知与萃取率(E%)的关系符合如下公式:lg
In(HA2)3+3H+,平衡常数为K。“萃取”时萃取率的高低受溶液的pH影响很大,已知与萃取率(E%)的关系符合如下公式:lg =lgK-lg
=lgK-lg 。当pH=2.30时,萃取率为50%,若将萃取率提升到95%,应调节溶液的pH=
。当pH=2.30时,萃取率为50%,若将萃取率提升到95%,应调节溶液的pH=(5)盐酸的浓度与铟、铁的反萃取率的关系如图所示。则“反萃取”过程中应选择盐酸的最佳浓度为

(6)“置换”后所得浊液,需要经过过滤、洗涤、干燥等操作得到粗铟,在洗涤操作中,检验粗铟已洗涤干净的方法为
您最近一年使用:0次
2022-10-29更新
|
608次组卷
|
3卷引用:吉林省吉林市普通中学2022-2023学年高三第一次调研测试化学试题
名校
解题方法
4 . 草酸亚铁晶体(FeC2O4•2H2O)常用作生产锂电池、涂料、着色剂以及感光材料的原材料,难溶于水,受热易分解。
I.制备草酸亚铁晶体:
①称取硫酸亚铁铵晶体5g,放入250mL三颈烧瓶中,加入10滴左右1.0mol•L-1H2SO4溶液和15mL蒸馏水加热溶解;
②加入25mL饱和草酸溶液,加热搅拌至沸腾停止加热,静置;
③待黄色晶体FeC2O4•2H2O沉淀后倾析,洗涤,加入约20mL蒸馏水搅拌并温热5min,静置,弃去上层清液,即得黄色草酸亚铁晶体。

(1)B的名称是____ ;B的出水口是____ (填“上口”或“下口”)。
(2)硫酸亚铁铵晶体中可能混有Fe3+,检验其是否含有Fe3+的试剂是____ 溶液,若混有Fe3+,观察到的现象是____ 。
II.将一定质量的草酸亚铁晶体(FeC2O4•2H2O)在氩气气氛中进行热重分析示意图(TG%表示残留固体质量占原样品总质量的百分数)。

(3)B处时残留物的化学式为____ 。
(4)取上述分解得到的600℃时的固体放在空气中继续加热时其质量增加,发生反应的化学方程式为____ 。
I.制备草酸亚铁晶体:
①称取硫酸亚铁铵晶体5g,放入250mL三颈烧瓶中,加入10滴左右1.0mol•L-1H2SO4溶液和15mL蒸馏水加热溶解;
②加入25mL饱和草酸溶液,加热搅拌至沸腾停止加热,静置;
③待黄色晶体FeC2O4•2H2O沉淀后倾析,洗涤,加入约20mL蒸馏水搅拌并温热5min,静置,弃去上层清液,即得黄色草酸亚铁晶体。

(1)B的名称是
(2)硫酸亚铁铵晶体中可能混有Fe3+,检验其是否含有Fe3+的试剂是
II.将一定质量的草酸亚铁晶体(FeC2O4•2H2O)在氩气气氛中进行热重分析示意图(TG%表示残留固体质量占原样品总质量的百分数)。

(3)B处时残留物的化学式为
(4)取上述分解得到的600℃时的固体放在空气中继续加热时其质量增加,发生反应的化学方程式为
您最近一年使用:0次
2022-10-29更新
|
177次组卷
|
4卷引用:吉林省吉林市普通中学2022-2023学年高三第一次调研测试化学试题
名校
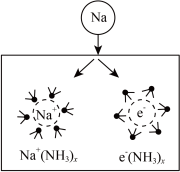
5 . 钠在液氨中溶剂化速度极快,生成蓝色的溶剂合电子,如图为钠投入液氨中的溶剂化图。钠沉入液氨中,快速得到深蓝色溶液,并慢慢产生气泡。下列说法错误的是

| A.钠的密度比液氨大 |
| B.溶液的导电性增强 |
| C.钠和液氨可发生以下反应:2NH3+2Na=2NaNH2+H2↑ |
| D.0.1mol钠投入液氨生成0.01molH2时,Na共失去0.02mol电子 |
您最近一年使用:0次
2021-05-07更新
|
1591次组卷
|
15卷引用:吉林省吉林市普通中学2022-2023学年高三第一次调研测试化学试题
吉林省吉林市普通中学2022-2023学年高三第一次调研测试化学试题吉林省吉林市普通中学2022-2023学年高三上学期10月调研化学试题山东省临沂市部分县区2020-2021学年高一下学期期中考试化学试题广东省广州市广州大学附属中学2020-2021学年高一下学期4月月考试题(已下线)课时14 钠及其化合物-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点13 钠及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点13 钠及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)重庆市第一中学校 2021-2022学年高二上学期入学摸底考试化学试题黑龙江省实验中学2021-2022高三上学期第三次月考(开学考)化学试题天津市耀华中学2021-2022学年高三上学期第一次月考化学试题浙江省湖州市三贤联盟2021-2022学年高一上学期期中考试化学试题天津市耀华中学2022-2023学年高一上学期期中考试化学试题吉林省延边第二中学2022-2023学年高三上学期10月月考化学试题河南省许昌市禹州市高级中学2023-2024学年高三上学期9月月考化学试题福建省莆田第一中学2023-2024学年高一上学期期末考试化学试题
名校
解题方法
6 . 一种由短周期主族元素组成的化合物(如图所示),具有良好的储氢性能,其中元素W、X、Y、Z的原子序数依次增大、且总和为24.下列有关叙述错误的是
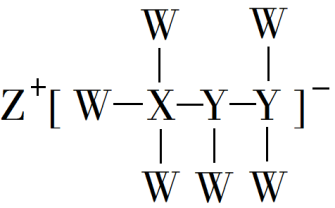
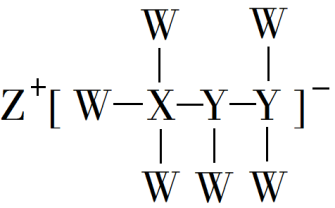
| A.该化合物中,W、X、Y之间均为共价键 |
| B.Z的单质能与水反应生成强碱 |
| C.Y的最高化合价氧化物的水化物为强酸 |
| D.X的氟化物XF3中原子均为8电子稳定结构 |
您最近一年使用:0次
2021-03-10更新
|
1558次组卷
|
4卷引用:吉林省吉林市第二中学2022-2023学年高一上学期1月期末考试化学试题
解题方法
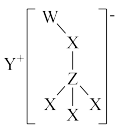
7 . 某离子化合物的结构如图所示,其中W、Y、Z是原子序数依次增大的短周期主族元素,W的最低负价与Y的最高正价代数和为0,W与X构成的某种化合物是一种绿色氧化剂,X与Z同主族。下列说法正确的是

| A.X、Y、Z三种元素组成的化合物的水溶液一定呈碱性 |
| B.原子半径大小:Y > Z >X>W |
| C.W、Y组成的化合物中各微粒均达8电子稳定结构 |
| D.最简单氢化物的稳定性:Z > X |
您最近一年使用:0次
2020-11-20更新
|
934次组卷
|
3卷引用:吉林省吉林市第二中学2020-2021学年高三上学期11月月考化学试题
名校
解题方法
8 . 有以下几种物质①碳酸氢钠晶体②液态氯化氢③铁④蔗糖⑤酒精⑥熔融的K2SO4⑦干冰⑧石墨填空回答:(填序号)
(1)以上物质能导电的是______
(2)以上物质中属于电解质的是______
(3)以上物质中属于非电解质的是______
(4)以上物质中溶于水后水溶液能导电的是______
(5)分别写出物质①、⑥在水溶液中的电离方程式_________________ 、_____________ .
(1)以上物质能导电的是
(2)以上物质中属于电解质的是
(3)以上物质中属于非电解质的是
(4)以上物质中溶于水后水溶液能导电的是
(5)分别写出物质①、⑥在水溶液中的电离方程式
您最近一年使用:0次
2019-11-04更新
|
177次组卷
|
2卷引用:吉林省吉林地区普通高中友好学校联合体第三十一届2019-2020学年高一上学期期中考试化学试题
10-11高一上·吉林·期中
解题方法
9 . 下图各物质中,A、B、C是常见金属单质,甲、乙、丙是气体且乙是有特殊颜色的气体(图中有些反应的产物和反应的条件没有全部标出)。

请根据以上信息回答下列问题:
(1)写出:H的化学式_________ ,乙的两种重要用途________________________
(2)写出有关反应的离子方程式:
反应①__________________________________________
反应②____________________________________
(3)判断反应③已经发生的常用试剂是______________________
(4)胶态磁流体(液溶胶)在医学上有重要用途,C单质对应元素的某种纳米级氧化物是磁流体中的重要粒子,该磁流体的主要制备过程如下:(Ⅰ)将NH3通入F、G的混合溶液(F、G物质的量比为1:2)中会生成两种碱。(Ⅱ)这两种碱恰好反应就得到该氧化物。写出(Ⅱ)中反应的化学方程式为:_________________________ ,确定该磁流体己成功制取的方法_________________________________

请根据以上信息回答下列问题:
(1)写出:H的化学式
(2)写出有关反应的离子方程式:
反应①
反应②
(3)判断反应③已经发生的常用试剂是
(4)胶态磁流体(液溶胶)在医学上有重要用途,C单质对应元素的某种纳米级氧化物是磁流体中的重要粒子,该磁流体的主要制备过程如下:(Ⅰ)将NH3通入F、G的混合溶液(F、G物质的量比为1:2)中会生成两种碱。(Ⅱ)这两种碱恰好反应就得到该氧化物。写出(Ⅱ)中反应的化学方程式为:
您最近一年使用:0次
真题
名校
10 . W、X、Y和Z是周期表中前20号元素,已知:
①W的阳离子和Y的阴离子具有相同的核外电子排布,且能形成组成为WY的化合物;
②Y和Z属同族元素,它们能形成两种常见化合物;
③X和Z属同一周期元素,它们能形成两种气态化合物;
④W和X能形成组成为WX2的化合物;
⑤X和Y不在同一周期,它们能形成组成为XY2的化合物。
请回答:
(1)W元素是____________ ;Z元素是____________ 。
(2)化合物WY和WX2的化学式分别是____________ 和____________ 。
(3)Y和Z形成的两种常见化合物的分子式是____________ 和____________ 。
(4)写出X和Z形成的一种气态化合物跟WZ反应的化学方程式:____________ 。
①W的阳离子和Y的阴离子具有相同的核外电子排布,且能形成组成为WY的化合物;
②Y和Z属同族元素,它们能形成两种常见化合物;
③X和Z属同一周期元素,它们能形成两种气态化合物;
④W和X能形成组成为WX2的化合物;
⑤X和Y不在同一周期,它们能形成组成为XY2的化合物。
请回答:
(1)W元素是
(2)化合物WY和WX2的化学式分别是
(3)Y和Z形成的两种常见化合物的分子式是
(4)写出X和Z形成的一种气态化合物跟WZ反应的化学方程式:
您最近一年使用:0次
2016-12-09更新
|
755次组卷
|
7卷引用:2015-2016学年吉林省吉林第一中学高一入学摸底化学试卷
2015-2016学年吉林省吉林第一中学高一入学摸底化学试卷2007年普通高等学校招生全国统一考试(全国卷Ⅰ)理综化学部分(已下线)2012届河南省南阳一中高三上学期第四次月考化学试卷陕西省黄陵中学高新部2018届高三上学期期末考试化学试题福建省福州市第一中学2020年高一在线自测自评质检化学试题河南省林州市第一中学2021-2022学年高一下学期开学检测化学试题(已下线)BBWYhjhx1008.pdf



