名校
解题方法
1 . 立德粉(主要成分为BaSO4 ZnS)常用作颜料。以粗氧化锌(主要成分为ZnO,还含少量CuO、Fe3O4等杂质)和BaS为原料制备立德粉的流程如图所示:
ZnS)常用作颜料。以粗氧化锌(主要成分为ZnO,还含少量CuO、Fe3O4等杂质)和BaS为原料制备立德粉的流程如图所示:___________ 。
(2)加入H2O2发生反应的离子方程式为___________ 。
(3)分离出Fe(OH)3的实验操作名称为___________ 。
(4)“除杂Ⅱ”中加入过量的锌粉主要除去___________ (填离子符号),该反应的反应类型为___________ 。
(5)“滤渣”的成分是___________ 。
(6)8.34 g绿矾(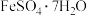 )晶体样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示:
)晶体样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示: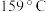 时固体N的化学式为
时固体N的化学式为___________ ,取适量  时所得的样品P,隔绝空气加热至
时所得的样品P,隔绝空气加热至 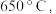 得到一种红棕色固体物质Q ,同时有两种无色气体生成,请写出该反应的化学方程式
得到一种红棕色固体物质Q ,同时有两种无色气体生成,请写出该反应的化学方程式___________ 。
 ZnS)常用作颜料。以粗氧化锌(主要成分为ZnO,还含少量CuO、Fe3O4等杂质)和BaS为原料制备立德粉的流程如图所示:
ZnS)常用作颜料。以粗氧化锌(主要成分为ZnO,还含少量CuO、Fe3O4等杂质)和BaS为原料制备立德粉的流程如图所示: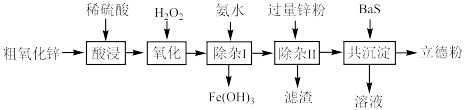
(2)加入H2O2发生反应的离子方程式为
(3)分离出Fe(OH)3的实验操作名称为
(4)“除杂Ⅱ”中加入过量的锌粉主要除去
(5)“滤渣”的成分是
(6)8.34 g绿矾(
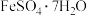 )晶体样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示:
)晶体样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示: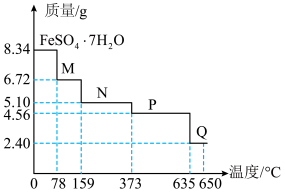
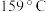 时固体N的化学式为
时固体N的化学式为 时所得的样品P,隔绝空气加热至
时所得的样品P,隔绝空气加热至 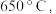 得到一种红棕色固体物质Q ,同时有两种无色气体生成,请写出该反应的化学方程式
得到一种红棕色固体物质Q ,同时有两种无色气体生成,请写出该反应的化学方程式
您最近一年使用:0次
2024-05-22更新
|
309次组卷
|
2卷引用:2024届重庆市乌江新高考协作体高三下学期模拟预测化学试题
解题方法
2 . 下列离子方程式正确的是
A.利用覆铜板制作印刷电路板: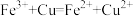 |
B.向 溶液中通入少量 溶液中通入少量 : :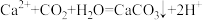 |
C.氧化铝与烧碱溶液反应: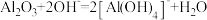 |
D.铝与 溶液反应: 溶液反应: |
您最近一年使用:0次
3 . 三氯化铬是有机金属化学中的重要原料,为紫色晶体,熔点为83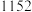 ℃,易潮解,高温下易被氧气氧化。实验室用
℃,易潮解,高温下易被氧气氧化。实验室用 和
和 加热到
加热到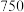 ℃时可制取
℃时可制取 ,同时还生成
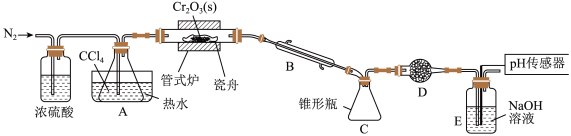
,同时还生成 ,其装置图如下
,其装置图如下 加热及夹持装置略去
加热及夹持装置略去 ,请回答下列问题:
,请回答下列问题:
已知: 沸点
沸点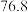 ℃;
℃; 有毒,沸点
有毒,沸点 ℃,遇水剧烈水解生成刺激性气味的气体。
℃,遇水剧烈水解生成刺激性气味的气体。
Ⅰ.制备 :
:
(1)仪器 的名称是
的名称是______ 。
(2)装置 、
、 的作用分别是
的作用分别是______ 、______ 。
(3)实验前先通入一段时间 的目的是
的目的是______ 。
(4)制备 的化学方程式为
的化学方程式为______ 。
(5)判断反应结束的依据是______ 。
Ⅱ.测定 纯度:
纯度:
称取 产品,在强碱性条件下,加入过量
产品,在强碱性条件下,加入过量 溶液,并小火加热,使
溶液,并小火加热,使 元素完全转化为
元素完全转化为 ;继续加热一段时间,冷却后配制成
;继续加热一段时间,冷却后配制成 溶液;取出
溶液;取出 ,滴加适量硫酸酸化后,用新配制的
,滴加适量硫酸酸化后,用新配制的 标准液滴定至终点,消耗标准液
标准液滴定至终点,消耗标准液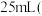 已知
已知 被
被 还原为
还原为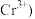 。
。
(6) 被
被 氧化成
氧化成 的离子方程式为
的离子方程式为______ 。
(7)产品中 的纯度为
的纯度为______  杂质不参与反应
杂质不参与反应 。
。
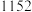 ℃,易潮解,高温下易被氧气氧化。实验室用
℃,易潮解,高温下易被氧气氧化。实验室用 和
和 加热到
加热到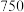 ℃时可制取
℃时可制取 ,同时还生成
,同时还生成 ,其装置图如下
,其装置图如下 加热及夹持装置略去
加热及夹持装置略去 ,请回答下列问题:
,请回答下列问题:
已知:
 沸点
沸点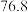 ℃;
℃; 有毒,沸点
有毒,沸点 ℃,遇水剧烈水解生成刺激性气味的气体。
℃,遇水剧烈水解生成刺激性气味的气体。Ⅰ.制备
 :
:(1)仪器
 的名称是
的名称是(2)装置
 、
、 的作用分别是
的作用分别是(3)实验前先通入一段时间
 的目的是
的目的是(4)制备
 的化学方程式为
的化学方程式为(5)判断反应结束的依据是
Ⅱ.测定
 纯度:
纯度:称取
 产品,在强碱性条件下,加入过量
产品,在强碱性条件下,加入过量 溶液,并小火加热,使
溶液,并小火加热,使 元素完全转化为
元素完全转化为 ;继续加热一段时间,冷却后配制成
;继续加热一段时间,冷却后配制成 溶液;取出
溶液;取出 ,滴加适量硫酸酸化后,用新配制的
,滴加适量硫酸酸化后,用新配制的 标准液滴定至终点,消耗标准液
标准液滴定至终点,消耗标准液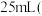 已知
已知 被
被 还原为
还原为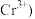 。
。(6)
 被
被 氧化成
氧化成 的离子方程式为
的离子方程式为(7)产品中
 的纯度为
的纯度为 杂质不参与反应
杂质不参与反应 。
。
您最近一年使用:0次
4 . 亚硝酸钙 广泛应用于钢筋混凝土工程中,主要用作水泥硬化促进剂和防冻阻锈剂,其为白色粉末,易潮解、易溶于水。实验室采用下列装置,用干燥的
广泛应用于钢筋混凝土工程中,主要用作水泥硬化促进剂和防冻阻锈剂,其为白色粉末,易潮解、易溶于水。实验室采用下列装置,用干燥的 与过氧化钙反应制取
与过氧化钙反应制取 。
。
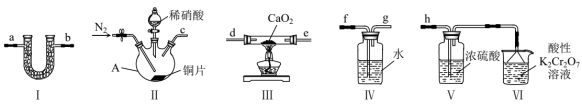
(1)仪器A的名称是
(2)装置的连接顺序是:c→
(3)滴入稀硝酸前需要通入一段时间
 ,待反应结束后还需继续通一会
,待反应结束后还需继续通一会 ,继续通
,继续通 的目的是
的目的是(4)装置Ⅱ中滴入稀硝酸后,A中观察到的现象是
(5)装置Ⅴ的作用是
(6)装置Ⅵ中氮元素被氧化成
 价,则反应的离子方程式为
价,则反应的离子方程式为(7)测定所得亚硝酸钙产品中硝酸钙的含量,实验步骤如下:

①除去 时,需要煮沸
时,需要煮沸 ,其反应的化学方程式为
,其反应的化学方程式为
②滴定时消耗标准液的体积为 ,则所得产品中硝酸钙的质量分数为
,则所得产品中硝酸钙的质量分数为
您最近一年使用:0次
5 . 某溶液中可能含有 、
、 、
、 、
、 、
、 中的几种离子。向该溶液中逐滴加入1
中的几种离子。向该溶液中逐滴加入1 的
的 溶液,生成沉淀的物质的量随
溶液,生成沉淀的物质的量随 溶液的体积变化如图所示。下列说法正确的是
溶液的体积变化如图所示。下列说法正确的是
 、
、 、
、 、
、 、
、 中的几种离子。向该溶液中逐滴加入1
中的几种离子。向该溶液中逐滴加入1 的
的 溶液,生成沉淀的物质的量随
溶液,生成沉淀的物质的量随 溶液的体积变化如图所示。下列说法正确的是
溶液的体积变化如图所示。下列说法正确的是
A.原溶液中一定含有 、 、 、 、 ,可能含有 ,可能含有 |
B.加入120  溶液时,溶液中的溶质只有 溶液时,溶液中的溶质只有 |
C.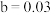 |
D.原溶液中 与 与 的物质的量之比为2∶1 的物质的量之比为2∶1 |
您最近一年使用:0次
2024-03-26更新
|
55次组卷
|
2卷引用:重庆市九龙坡区华岩中学2023-2024学年高一上学期第17周定时检测化学试题
解题方法
6 . 在工业生产中要制取某种物质,除了要考虑反应进行的可能性,还要考虑原料来源、成本高低和设备要求等因素,以选取最适当的方法。例如,工业上制取NaOH(a)一般不采用Na2O(b)与H2O(c)反应的方法(Na2O作为原料,来源少、成本高),而主要采用电解饱和食盐水的方法,过去也曾采用Na2CO3(d)与Ca(OH)2(e)反应的方法。回答下列问题:
(1)Na与水反应的离子方程式为______ 。
(2)电解饱和食盐水的化学方程式为2NaCl+2H2O 2NaOH+H2↑+Cl2↑。
2NaOH+H2↑+Cl2↑。
①该反应中的还原剂为______ 填化学式,下同),被氧化的物质为______ 。
②用双线桥法表示该反应中电子转移的方向和数目:______ 。
③每生成0.2gH2,同时生成Cl2的质量为______ g。
(3)d和e反应可制得a:将Na2CO3溶液加入澄清石灰水中,发生反应的离子方程式为______ 。
(1)Na与水反应的离子方程式为
(2)电解饱和食盐水的化学方程式为2NaCl+2H2O
 2NaOH+H2↑+Cl2↑。
2NaOH+H2↑+Cl2↑。①该反应中的还原剂为
②用双线桥法表示该反应中电子转移的方向和数目:
③每生成0.2gH2,同时生成Cl2的质量为
(3)d和e反应可制得a:将Na2CO3溶液加入澄清石灰水中,发生反应的离子方程式为
您最近一年使用:0次
解题方法
7 . 有一瓶澄清的无色溶液,其中可能含有H+、Na+、Mg2+、Ba2+、Fe3+、Cl-、CO 、SO
、SO 。取该溶液进行以下实验:
。取该溶液进行以下实验:
(1)由题干可知溶液中一定不存在_______ (填离子符号,下同);用pH试纸检验,溶液呈强酸性,可以排除_______ 的存在。
(2)取出部分溶液滴加过量的NaOH溶液,只产生白色沉淀,则可证明_______ (填离子符号)的存在,生成白色沉淀的离子方程式为_______ 。
(3)取出部分上述碱性溶液滴加Na2SO4溶液,有白色沉淀生成,证明______ (填离子符号,下同)的存在,同时可排除原溶液中______ 的存在,产生白色沉淀的离子方程式为______ 。
(4)根据上述实验事实可知原溶液中不能确定是否存在的离子有______ ,如果要确定该离子确实存在,可以通过______ 方法。
 、SO
、SO 。取该溶液进行以下实验:
。取该溶液进行以下实验:(1)由题干可知溶液中一定不存在
(2)取出部分溶液滴加过量的NaOH溶液,只产生白色沉淀,则可证明
(3)取出部分上述碱性溶液滴加Na2SO4溶液,有白色沉淀生成,证明
(4)根据上述实验事实可知原溶液中不能确定是否存在的离子有
您最近一年使用:0次
8 . 回答下列问题:
(1)①H2+CuO Cu+H2O②CaCO3+2HCl=CaCl2+CO2↑+H2O③3S+6NaOH
Cu+H2O②CaCO3+2HCl=CaCl2+CO2↑+H2O③3S+6NaOH 2Na2S+Na2SO3+3H2O④Cu2O+4HCl=2HCuCl2+H2O,上述反应中,属于氧化还原反应的有
2Na2S+Na2SO3+3H2O④Cu2O+4HCl=2HCuCl2+H2O,上述反应中,属于氧化还原反应的有______ (填序号)。
(2)用双线桥法表示下述反应的电子转移的方向和数目______ 。
MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O。
MnCl2+Cl2↑+2H2O。
(3)在反应KClO3+6HCl=3Cl2+KCl+3H2O中,氧化剂与还原剂的系数之比为______ 。
(4)配平下面两个反应:
____H2O+____Cl2+____SO2=____H2SO4+____HCl,(系数是1的也请填上)______ 。
____KMnO4+____HCl=____KCl+____MnCl2+____Cl2↑+____H2O(系数是1的也请填上)______ 。
根据以上两个反应反应,写出由KMnO4、K2SO4、MnSO4、SO2、H2O、H2SO4这六种物质组成的氧化还原反应的方程式并配平。______ 。
(1)①H2+CuO
 Cu+H2O②CaCO3+2HCl=CaCl2+CO2↑+H2O③3S+6NaOH
Cu+H2O②CaCO3+2HCl=CaCl2+CO2↑+H2O③3S+6NaOH 2Na2S+Na2SO3+3H2O④Cu2O+4HCl=2HCuCl2+H2O,上述反应中,属于氧化还原反应的有
2Na2S+Na2SO3+3H2O④Cu2O+4HCl=2HCuCl2+H2O,上述反应中,属于氧化还原反应的有(2)用双线桥法表示下述反应的电子转移的方向和数目
MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O。
MnCl2+Cl2↑+2H2O。(3)在反应KClO3+6HCl=3Cl2+KCl+3H2O中,氧化剂与还原剂的系数之比为
(4)配平下面两个反应:
____H2O+____Cl2+____SO2=____H2SO4+____HCl,(系数是1的也请填上)
____KMnO4+____HCl=____KCl+____MnCl2+____Cl2↑+____H2O(系数是1的也请填上)
根据以上两个反应反应,写出由KMnO4、K2SO4、MnSO4、SO2、H2O、H2SO4这六种物质组成的氧化还原反应的方程式并配平。
您最近一年使用:0次
解题方法
9 . I.现有下列7种物质:①二氧化硫;②稀硫酸;③铜;④氢氧化钾固体;⑤酒精(C2H5OH);⑥硝酸钾溶液;⑦氧化钠固体,请将上述物质按要求完成下列问题(用相应化学式填空):
(1)属于碱性氧化物的是______ ,属于电解质的有______ 。
Ⅱ.某课外活动小组进行Fe(OH)3胶体的制备实验并检验其相关性质。
(2)若将饱和FeCl3溶液分别滴入下列液体中,能形成胶体 是
是______ 。
(3)写出制备Fe(OH)3胶体的化学方程式:______ 。
(1)属于碱性氧化物的是
Ⅱ.某课外活动小组进行Fe(OH)3胶体的制备实验并检验其相关性质。
(2)若将饱和FeCl3溶液分别滴入下列液体中,能形成胶体
 是
是| A.冷水 | B.沸水 | C.NaOH浓溶液 | D.NaCl浓溶液 |
(3)写出制备Fe(OH)3胶体的化学方程式:
您最近一年使用:0次
解题方法
10 . 下列关于Na2CO3和NaHCO3性质的说法,正确的是
| A.在水中的溶解度:NaHCO3>Na2CO3 |
| B.可以用澄清的石灰水鉴别 |
| C.热稳定性:NaHCO3<Na2CO3 |
| D.Na2CO3不能转化成NaHCO3,而NaHCO3能转化成Na2CO3 |
您最近一年使用:0次



