名校
1 . 黄铁矿( )在酸性条件下发生催化氧化的反应历程如图所示。下列说法错误的是
)在酸性条件下发生催化氧化的反应历程如图所示。下列说法错误的是
 )在酸性条件下发生催化氧化的反应历程如图所示。下列说法错误的是
)在酸性条件下发生催化氧化的反应历程如图所示。下列说法错误的是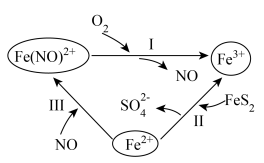
| A.反应Ⅰ、Ⅱ、Ⅲ均发生氧化还原反应 |
B.反应Ⅰ中氧化剂与还原剂的物质的量之比为 |
C.反应Ⅱ的离子方程式为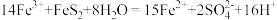 |
D.该过程的总反应为 |
您最近一年使用:0次
2024-06-05更新
|
173次组卷
|
2卷引用:2024年甘肃省张掖市第一中学模拟化学试题
名校
2 . 下列离子方程式书写正确的是
A.铅酸蓄电池放电时的负极反应: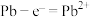 |
B.药物碘化钾片和加碘盐不可同时服用: |
C.向 溶液中加入足量NaOH溶液: 溶液中加入足量NaOH溶液: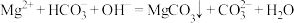 |
D.向食盐的氨水溶液中通入足量 气体后生成沉淀: 气体后生成沉淀: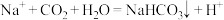 |
您最近一年使用:0次
2024-05-27更新
|
148次组卷
|
2卷引用:2024届甘肃省民乐县第一中学高三下学期5月模拟考试化学试卷
名校
解题方法
3 . 下列各组离子在指定溶液中能大量共存的是
A.无色透明溶液中: 、 、 、 、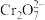 、 、 |
B.含有 的溶液中: 的溶液中: 、 、 、 、 、 、 |
C.使甲基橙变红的溶液中: 、 、 、 、 、 、 |
D.室温下,中性溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
名校
4 . 用含钴废料(主要成分为CoO、Fe3O4、Al2O3、ZnO、PbO、CaO、MgO(等))中的有效成分制备CoOOH的工艺流程如图所示:

已知:①ZnO与Al2O3化学性质相似,既能溶于强酸又能溶于强碱。
②各种沉淀pH数据。
③ ;HF的电离常数为
;HF的电离常数为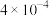 ;lg2=0.3.
;lg2=0.3.
回答下列问题:
(1)“浸出液”的主要成分是NaOH、_____ 。
(2)“酸浸”时“浸渣”的成分为_____ 。
(3)“除铁”过程中,先在40~50℃加入H2O2,其作用是_____ (用离子方程式表示);然后加氨水调节的pH范围为_____ 。
(4)“氧化”时将Co2+转化为CoOOH,则该反应的离子方程式为_____ 。
(5)“沉镁”时反应的离子方程式为_____ ,若Mg2+恰好完全沉淀时,溶液中的c(HF)与c(Mg2+)相等,则此时溶液的pH为_____ 。

已知:①ZnO与Al2O3化学性质相似,既能溶于强酸又能溶于强碱。
②各种沉淀pH数据。
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Mg(OH)2 |
| 开始沉淀pH | 2.7 | 7.6 | 7.6 | 7.8 |
| 完全沉淀pH | 3.7 | 9.6 | 9.2 | 8.8 |
 ;HF的电离常数为
;HF的电离常数为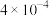 ;lg2=0.3.
;lg2=0.3.回答下列问题:
(1)“浸出液”的主要成分是NaOH、
(2)“酸浸”时“浸渣”的成分为
(3)“除铁”过程中,先在40~50℃加入H2O2,其作用是
(4)“氧化”时将Co2+转化为CoOOH,则该反应的离子方程式为
(5)“沉镁”时反应的离子方程式为
您最近一年使用:0次
名校
5 . 在给定条件下,下列选项所示的物质间转化无法实现的是
A.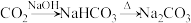 |
B.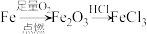 |
C.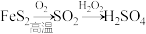 |
D.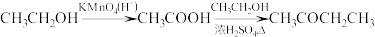 |
您最近一年使用:0次
名校
6 . 设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.22.4LCH4与足量Cl2完全反应,产生的HCl分子数为 |
B.含有12g碳原子的甲醇与丙三醇的混合物中羟基数目为 |
C.1L 酸化的K2Cr2O7溶液中 酸化的K2Cr2O7溶液中 的数目为 的数目为 |
D.1molCO2电催化转化为CH4,转移电子的数目为 |
您最近一年使用:0次
名校
7 . 宏观辨识与微观探析是化学学科核心素养之一、下列描述物质制备和应用的离子方程式中正确的是
A.向 溶液中滴入氨水: 溶液中滴入氨水: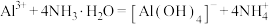 |
B.实验室常用硫酸铜溶液吸收尾气中的 : : |
C.向NaClO溶液中通入少量 : : |
D.沸水中滴加饱和 溶液至液体呈红褐色: 溶液至液体呈红褐色: |
您最近一年使用:0次
2024-01-05更新
|
117次组卷
|
2卷引用:甘肃省张掖市高台县第一中学2023-2024学年高三下学期模拟考化学试题
名校
8 . 铁、铝、铜等金属及其化合物在日常生活中应用广泛。
(1)生铁中含有一种铁碳化合物X,实验室测定该化合物X组成的实验如下,最终得到的固体2是Fe2O3。

①已知固体1有磁性,将其溶于过量盐酸后,溶液中含有的大量阳离子是H+和___________ 。
②X的化学式可表示为___________ ,X与足量的热浓硝酸反应能生成的气体是___________ 。
(2)某溶液中有Mg2+、 、
、 、
、 四种正离子,向其中加入过量的NaOH溶液后,过滤,将滤渣高温灼烧并将灼烧后的固体投入过量的稀盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是___________(填选项)。
四种正离子,向其中加入过量的NaOH溶液后,过滤,将滤渣高温灼烧并将灼烧后的固体投入过量的稀盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是___________(填选项)。
(3)氧化铁是重要工业颜料,煅烧FeCO3可得到此颜料。写出在空气中煅烧FeCO3的化学方程式________ 。
(4)向含有1molHNO3和0.7molH2SO4的混合溶液中逐渐加入铁粉至过量,溶液中金属阳离子a、b与所加铁粉的物质的量的关系如图所示(已知稀硝酸的还原产物只有NO)。

①a表示的是___________ 的变化曲线。
②n1=___________ 。
③向P点溶液中加入铜粉,最多可溶解铜粉的质量是___________ g。
(1)生铁中含有一种铁碳化合物X,实验室测定该化合物X组成的实验如下,最终得到的固体2是Fe2O3。

①已知固体1有磁性,将其溶于过量盐酸后,溶液中含有的大量阳离子是H+和
②X的化学式可表示为
(2)某溶液中有Mg2+、
 、
、 、
、 四种正离子,向其中加入过量的NaOH溶液后,过滤,将滤渣高温灼烧并将灼烧后的固体投入过量的稀盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是___________(填选项)。
四种正离子,向其中加入过量的NaOH溶液后,过滤,将滤渣高温灼烧并将灼烧后的固体投入过量的稀盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是___________(填选项)。| A.Mg2+ | B. | C. | D. |
(3)氧化铁是重要工业颜料,煅烧FeCO3可得到此颜料。写出在空气中煅烧FeCO3的化学方程式
(4)向含有1molHNO3和0.7molH2SO4的混合溶液中逐渐加入铁粉至过量,溶液中金属阳离子a、b与所加铁粉的物质的量的关系如图所示(已知稀硝酸的还原产物只有NO)。

①a表示的是
②n1=
③向P点溶液中加入铜粉,最多可溶解铜粉的质量是
您最近一年使用:0次
名校
解题方法
9 . 过氧化钠是重要的化工原料,具有多种用途。
(1)过氧化钠是_______ 色固体。
(2)过氧化钠可用作呼吸面具、潜水艇的供氧剂,写出 和
和 反应的化学方程式:
反应的化学方程式:_______ ,反应中转移的电子总数为_______ 个。
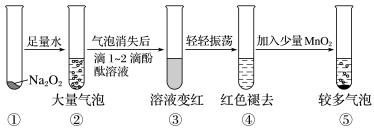
(3)某实验小组通过如图所示实验,探究 与水的反应,下列说法正确的是_______。
与水的反应,下列说法正确的是_______。
(4) 具有强氧化性,与
具有强氧化性,与 反应能生成硫酸钠,写出反应的化学方程式:
反应能生成硫酸钠,写出反应的化学方程式:_______ 。
(1)过氧化钠是
(2)过氧化钠可用作呼吸面具、潜水艇的供氧剂,写出
 和
和 反应的化学方程式:
反应的化学方程式:(3)某实验小组通过如图所示实验,探究
 与水的反应,下列说法正确的是_______。
与水的反应,下列说法正确的是_______。
| A.②中的大量气泡主要成分是氢气 |
| B.③中溶液变红,说明有酸性物质生成 |
| C.④中现象可能是由于溶液中含有强氧化性物质造成的 |
D.⑤中 的主要作用是降低了水中氧气的溶解度 的主要作用是降低了水中氧气的溶解度 |
(4)
 具有强氧化性,与
具有强氧化性,与 反应能生成硫酸钠,写出反应的化学方程式:
反应能生成硫酸钠,写出反应的化学方程式:
您最近一年使用:0次
名校
解题方法
10 . 关于物质分类的正确组合是
| 分类组合 | 碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 |
| A | 烧碱 |  | 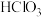 |  |  |
| B | 纯碱 |  | 石灰石 |  |  |
| C |  |  |  |  |  |
| D |  |  |  | 生石灰 | 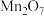 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



