名校
解题方法
1 . 中华文化博大精深,蕴含着许多化学知识。下列说法正确的是
| A.“何意百炼刚,化为绕指柔”中,经“百炼”的钢的硬度比纯铁的硬度小 |
B.“西真人醉忆仙家。飞佩丹霞羽化”中所呈现的丹霞地貌是由于岩层中含有 |
| C.杭州第19届亚运会吉祥物“琮琮”的名字源自良渚玉琮,玉琮的主要材质是铜锌合金 |
| D.明荷花纹玉壶的雕刻过程中发生了化学变化 |
您最近一年使用:0次
2024-06-02更新
|
268次组卷
|
2卷引用:甘肃省陇南市部分学校2023-2024学年高三下学期化学押题考试(三模)化学试题
解题方法
2 . 下列离子在 溶液中能大量存在的是
溶液中能大量存在的是
 溶液中能大量存在的是
溶液中能大量存在的是A. | B. | C. | D. |
您最近一年使用:0次
2023-07-14更新
|
86次组卷
|
3卷引用:甘肃省陇南市2022-2023学年高一下学期期末考试化学试题
3 . 某小组探究 与盐酸的反应。取
与盐酸的反应。取 固体分别溶于30mL盐酸、30mL水,测得温度变化如图所示。下列叙述正确的是
固体分别溶于30mL盐酸、30mL水,测得温度变化如图所示。下列叙述正确的是

 与盐酸的反应。取
与盐酸的反应。取 固体分别溶于30mL盐酸、30mL水,测得温度变化如图所示。下列叙述正确的是
固体分别溶于30mL盐酸、30mL水,测得温度变化如图所示。下列叙述正确的是
A. 固体溶于水的反应是放热反应 固体溶于水的反应是放热反应 |
B. 固体与盐酸的反应是放热反应 固体与盐酸的反应是放热反应 |
C. 固体与盐酸的反应属于非氧化还原反应 固体与盐酸的反应属于非氧化还原反应 |
D.在70s时向上述两溶液中均加入硝酸酸化的 溶液,均有白色沉淀生成 溶液,均有白色沉淀生成 |
您最近一年使用:0次
2023-07-14更新
|
103次组卷
|
2卷引用:甘肃省陇南市2022-2023学年高一下学期期末考试化学试题
4 . 关于下列仪器使用的说法正确的是
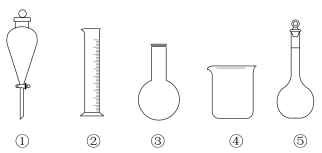

| A.①⑤在使用前均需检查是否漏液 | B.③⑤均可垫石棉网进行加热 |
| C.②④均可用于物质的分离 | D.②⑤均可以准确量取液体 |
您最近一年使用:0次
2023-07-14更新
|
60次组卷
|
2卷引用:甘肃省陇南市2022-2023学年高一下学期期末考试化学试题
名校
解题方法
5 . 下列实验或现象中的颜色变化,不涉及氧化还原反应的是
| A | B | C | D | |
| 实验 | 用稀盐酸除去铜制器皿表面的铜绿【Cu2(OH)2CO3】 | Na2O2露置在空气中 | 往FeCl3溶液中加入足量铁粉 | 向新制的氯水中通入足量SO2气体 |
| 现象 | 铜制器皿表面恢复红色,废液呈蓝色 | 固体粉末由淡黄色变为白色 | 溶液颜色由棕黄色变为浅绿色 | 氯水淡黄绿色褪去 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-09-19更新
|
80次组卷
|
3卷引用:甘肃省礼县第一中学2020-2021学年高一下学期期末测试化学试卷(B)
名校
解题方法
6 . 按纯净物、混合物、电解质和非电解质顺序排列的一组物质是
| A.盐酸、空气、醋酸、干冰 | B.淀粉胶体、食盐、烧碱、氯化钙 |
| C.胆矾、海水、硫酸钠、蔗糖 | D.胆矾、大理石、氯化钾、硫酸钡 |
您最近一年使用:0次
2022-09-19更新
|
329次组卷
|
8卷引用:甘肃省礼县第一中学2020-2021学年高一下学期期末测试化学试卷(B)
7 . 化学与生产、生活、科技等密切相关,下列说法错误的是
| A.开发利用太阳能、风能和氢能等新能源代替化石能源,利于实现低碳经济 |
| B.利用膜材料将含油污水中的油水分离,发生的是化学变化 |
| C.工业上用FeCl3溶液来腐蚀铜膜,制作印刷电路板 |
| D.二氧化硅是制备光导纤维的基本原料 |
您最近一年使用:0次
解题方法
8 . 如表是元素周期表的一部分,表中所列的数字分别代表某一种元素。
请完成下列空白。
(1)属于卤族元素的有_____ (填元素符号,下同);属于碱金属元素的有_____ 。
(2)②与③原子结构的相同点是____ ,决定了它们具有相似的化学性质,即_____ ;不同点是______ ,决定它们的化学性质具有递变性,即______ 。
(3)能证明元素⑧比⑨的非金属性强的实验事实有(用离子方程式表示):____ 。
(4)画出元素④的原子结构示意图:_____ ;与元素⑤同属于______ 族;预测它们单质化学性质的相似性是_____ 。
(5)元素⑥与⑦的原子最外层电子数都为_____ ;但预测⑥比⑦单质的氧化性______ ,其依据是____ ;预测元素⑥与⑦的气态氢化物的稳定性强弱:H2O____ H2S(填“>”或“<”)。
| 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ⑥ | |||||||
| 3 | ② | ④ | ⑦ | ⑧ | ||||
| 4 | ③ | ⑤ | ⑨ | |||||
请完成下列空白。
(1)属于卤族元素的有
(2)②与③原子结构的相同点是
(3)能证明元素⑧比⑨的非金属性强的实验事实有(用离子方程式表示):
(4)画出元素④的原子结构示意图:
(5)元素⑥与⑦的原子最外层电子数都为
您最近一年使用:0次
解题方法
9 . 六种主族元素A、B、C、D、X、Y的原子序数依次增大,且均小于54。常温下A2B呈液态,高纯度的单质C具有良好的半导体性能。D、X、Y原子核外最外层电子数均为7,过渡元素Z与B可形成多种化合物,其中红棕色粉末Z2B3常用作外墙涂料。请完成下列空白。
(1)将D2水溶液滴入浅绿色的ZD2溶液中,发生反应的离子方程式为___ 。
①甲认为X2和Y2都可能将Z2+氧化为Z3+,他推理的依据是___ 。
②乙认为X2和Y2都不能将Z2+氧化为Z3+;丙认为X2能将Z2+氧化为Z3+而Y2不能。乙、丙推理的依据是__ 。
(2)A与B可形成既含极性键又含非极性键的化合物W。W的水溶液呈弱酸性,常用作无公害的消毒杀菌剂等。W的电子式为__ 。
(3)铅(Pb)、锡(Sn)、锗(Ge)与元素C位于同主族,原子核外电子层数均小于7;常温下,锡、锗在空气中不反应,而铅表面会生成一层氧化铅。锗与盐酸不反应,而锡与盐酸反应。由此可得出以下结论:
①锗的原子序数为__ ;
②它们+4价氢氧化物的碱性由强到弱顺序为__ (填化学式)。
(1)将D2水溶液滴入浅绿色的ZD2溶液中,发生反应的离子方程式为
①甲认为X2和Y2都可能将Z2+氧化为Z3+,他推理的依据是
②乙认为X2和Y2都不能将Z2+氧化为Z3+;丙认为X2能将Z2+氧化为Z3+而Y2不能。乙、丙推理的依据是
(2)A与B可形成既含极性键又含非极性键的化合物W。W的水溶液呈弱酸性,常用作无公害的消毒杀菌剂等。W的电子式为
(3)铅(Pb)、锡(Sn)、锗(Ge)与元素C位于同主族,原子核外电子层数均小于7;常温下,锡、锗在空气中不反应,而铅表面会生成一层氧化铅。锗与盐酸不反应,而锡与盐酸反应。由此可得出以下结论:
①锗的原子序数为
②它们+4价氢氧化物的碱性由强到弱顺序为
您最近一年使用:0次
解题方法
10 . 下列有关元素周期表的说法中,正确的是
| A.含元素种类最多的周期是第四周期 |
| B.第IA族的元素只能形成离子键 |
| C.元素K比元素Br的质子数小16 |
| D.原子核外最外电子层有2个电子的元素都属于第IIA族 |
您最近一年使用:0次



