名校
解题方法
1 . 第112号化学元素元素符号为“Cn”,以纪念著名天文学家哥白尼,该元素的一种核素含有的中子数为165。下列关于Cn的说法不正确 的是
| A.Cn是第七周期元素 | B.Cn属于ds区元素 |
| C.Cn是金属元素 | D.Cn的一种核素可表示为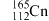 |
您最近一年使用:0次
2024-05-06更新
|
30次组卷
|
3卷引用:甘肃省定西市临洮中学2023-2024学年高二下学期3月第一次考试化学试题
甘肃省定西市临洮中学2023-2024学年高二下学期3月第一次考试化学试题黑龙江省绥化市绥棱县第一中学2023-2024学年高二上学期1月期末化学试题(已下线)1.2.1 原子结构与元素周期表课堂例题
名校
解题方法
2 . 我国著名化工实业家侯德榜提出了“联合制碱法”,该生产工艺流程如图所示。下列说法不正确 的是
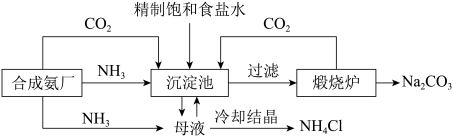
A.沉淀池发生反应: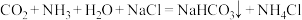 |
B.向饱和食盐水先通 ,再通 ,再通 ,更有利于 ,更有利于 析出 析出 |
C.该过程充分利用了合成氨提供的 和 和 |
D.吸收 可使母液中的 可使母液中的 转化为 转化为 ,以提高 ,以提高 纯度 纯度 |
您最近一年使用:0次
解题方法
3 . 下列图或表中,表示正确的是
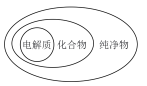 | 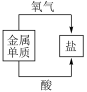 | 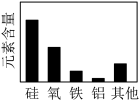 | 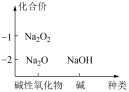 |
| A.物质的分类 | B.金属的性质 | C.地壳中元素含量顺序 | D.钠的价一类二维图 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
4 . 现有中学化学常见的金属单质甲、乙、丙和气体X、Y以及物质A、B、C、D、E、F,其中单质甲及化合物焰色为黄色,乙是生活中使用量最大的金属,丙的氧化物属于两性氧化物,气体X为黄绿色气体,它们之间的相互转化关系如图所示(图中某些反应的生成物和反应条件没有标出)。
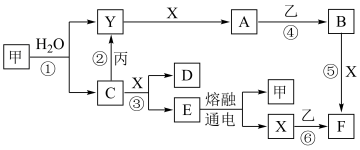
根据以上信息完成下列各题:
(1)写出下列物质的化学式:X________ ;B_______ 。
(2)反应②是管道疏通剂的疏通原理,写出对应的离子方程式:___________ ;金属丙与酸和碱均能反应生成H2,若生成相同质量的H2,消耗丙的质量______ (填“酸中多”“碱中多”或“一样多”)。
(3)若在B的溶液中加入C溶液,反应的实验现象为________ 。
(4)关于反应①的说法错误的是_______ (填字母)。
a.块状固体甲浮在水面上四处游动 b.溶液温度升高
c.反应后的溶液可使酚酞变红 d.反应中水既是氧化剂又是还原剂
(5)若将一块甲和丙的合金放入足量水中,充分反应后固体全部溶解,则合金中n(Na):n(Al)≥___ 。

根据以上信息完成下列各题:
(1)写出下列物质的化学式:X
(2)反应②是管道疏通剂的疏通原理,写出对应的离子方程式:
(3)若在B的溶液中加入C溶液,反应的实验现象为
(4)关于反应①的说法错误的是
a.块状固体甲浮在水面上四处游动 b.溶液温度升高
c.反应后的溶液可使酚酞变红 d.反应中水既是氧化剂又是还原剂
(5)若将一块甲和丙的合金放入足量水中,充分反应后固体全部溶解,则合金中n(Na):n(Al)≥
您最近一年使用:0次
解题方法
5 . 高铁酸盐(如K2FeO4)可用于净水。某化学小组同学进行以下两组实验,在制得氢氧化铁的基础上制备高铁酸盐。已知,①Fe2+对双氧水的分解有一定的催化作用;②制备高铁酸钾的反应原理为3C12+2Fe(OH)3+1OKOH=2K2FeO4+6KC1+8H2O。回答下列问题:
实验Ⅰ:取100mL饱和FeSO4溶液,滴加12%硫酸酸化的双氧水,再慢慢加入5mol/L的NaOH溶液;
(1)实验Ⅰ滴加双氧水的过程中,观察到溶液颜色变成黄色:其反应的离子方程式为_______ ,在溶液变成黄色的同时,看到不断有气泡产生,其原因是_________ 。
(2)完成实验Ⅰ后,及时对烧杯壁上附着的Fe(OH)3进行了清洗,但错把氢碘酸(HI,强酸)当成盐酸加入到了烧杯中,观察到清洗液偏棕色,并通过实验检测到了碘单质(I2)。他们认为可能是Fe(OH)3和HI反应生成了I2,配平该反应的离子方程式:______ ,__Fe(OH)3+___H++___I-=Fe2++__I2+H2O。
实验Ⅱ:在实验I的基础上用制得的Fe(OH)3合成K2FeO4,其装置如下(夹持仪器已略去):
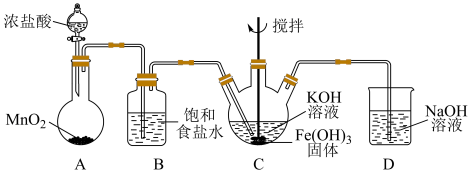
(3)上述装置中的明显错误是________ 。
(4)装置D中NaOH溶液的作用是______ 。
(5)若要制得19.8gK2FeO4,理论上需要浓盐酸的物质的量为_____ mol,但实验发现,浓盐酸的实际加入量远超过理论用量,分析出现该情况的原因:________ 。
(6)研究发现,酸性条件下,几种氧化剂的氧化性强弱关系为K2FeO4>KMnO4>Cl2,结合实验Ⅱ中信息,判断K2FeO4的氧化性强弱与_______ 有关。
实验Ⅰ:取100mL饱和FeSO4溶液,滴加12%硫酸酸化的双氧水,再慢慢加入5mol/L的NaOH溶液;
(1)实验Ⅰ滴加双氧水的过程中,观察到溶液颜色变成黄色:其反应的离子方程式为
(2)完成实验Ⅰ后,及时对烧杯壁上附着的Fe(OH)3进行了清洗,但错把氢碘酸(HI,强酸)当成盐酸加入到了烧杯中,观察到清洗液偏棕色,并通过实验检测到了碘单质(I2)。他们认为可能是Fe(OH)3和HI反应生成了I2,配平该反应的离子方程式:
实验Ⅱ:在实验I的基础上用制得的Fe(OH)3合成K2FeO4,其装置如下(夹持仪器已略去):

(3)上述装置中的明显错误是
(4)装置D中NaOH溶液的作用是
(5)若要制得19.8gK2FeO4,理论上需要浓盐酸的物质的量为
(6)研究发现,酸性条件下,几种氧化剂的氧化性强弱关系为K2FeO4>KMnO4>Cl2,结合实验Ⅱ中信息,判断K2FeO4的氧化性强弱与
您最近一年使用:0次
解题方法
6 . 元素周期表的建立和元素周期律的发现,特别是原子结构的奥秘被揭示,对人们从微观角度探索元素之间的内在联系,认识元素性质及其递变规律起到不可替代的作用。回答下列问题:
(1)元素性质周期性变化的根本原因是________ (填字母)。
a.原子核内中子数的变化 b.元素的相对原子质量逐渐增大
c.原子核外电子排布呈周期性变化 d.元素化合价呈周期性变化
(2)如图为元素周期表的一部分。按要求填空:
①以上元素对应的单质中,化学性质最稳定的是________ (填元素符号);最易与H2发生化合反应的单质是______ (填化学式)。
②Cl在元素周期表中的位置是______ ;Cl的最高价氧化物对应水化物的酸性比H2SO4______ (填“强”或“弱”),其电离方程式为_________ 。
③上表中第三周期元素对应的简单离子半径最大的是_______ (填离子符号);Na的最高价氧化物对应水化物与AI的最高价氧化物对应水化物反应的离子方程式为________ 。
(1)元素性质周期性变化的根本原因是
a.原子核内中子数的变化 b.元素的相对原子质量逐渐增大
c.原子核外电子排布呈周期性变化 d.元素化合价呈周期性变化
(2)如图为元素周期表的一部分。按要求填空:
| C | N | F | Ne | ||||
| Na | Al | S | Cl |
②Cl在元素周期表中的位置是
③上表中第三周期元素对应的简单离子半径最大的是
您最近一年使用:0次
7 . 下表是生活生产中常见的物质,表中列出了它们的化学式或主要成分,按要求填空:
(1)写出Fe粉与水蒸气反应制备少量磁性氧化铁的化学方程式:___________ ,②~⑥中属于电解质的是___________ (填序号)。
(2)次氯酸可用作棉、麻、纸张的漂白剂,但不稳定易分解,写出次氯酸在光照下分解的离子方程式:___________ 。
(3)次氯酸不稳定,人们制得了有漂白作用且较稳定的次氧酸盐,如将Cl2通入冷的石灰乳即可制得漂白粉,对应的化学方程式为___________ ,漂白粉的有效成分为___________ ,漂白粉在空气中久置也会变质,描述其变质原理:___________ 。
(4)胃舒平和小苏打均可用于治疗胃酸过多,写出治疗过程属于中和反应的离子方程式:___________ 。
| 名称 | 磁性氧化铁 | 次氯酸 | 胃舒平 | 小苏打 | 石灰乳 | 酒精 |
| 化学式或主要成分 | ①Fe3O4 | ②HClO | ③Al(OH)3 | ④NaHCO3 | ⑤Ca(OH)2 | ⑥C2H5OH |
(2)次氯酸可用作棉、麻、纸张的漂白剂,但不稳定易分解,写出次氯酸在光照下分解的离子方程式:
(3)次氯酸不稳定,人们制得了有漂白作用且较稳定的次氧酸盐,如将Cl2通入冷的石灰乳即可制得漂白粉,对应的化学方程式为
(4)胃舒平和小苏打均可用于治疗胃酸过多,写出治疗过程属于中和反应的离子方程式:
您最近一年使用:0次
8 . 某离子反应涉及H+、Bi3+、 、
、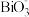 、Mn2+、H2O六种微粒。其中c(
、Mn2+、H2O六种微粒。其中c( )随反应进行逐渐增大。下列判断正确的是
)随反应进行逐渐增大。下列判断正确的是
 、
、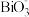 、Mn2+、H2O六种微粒。其中c(
、Mn2+、H2O六种微粒。其中c( )随反应进行逐渐增大。下列判断正确的是
)随反应进行逐渐增大。下列判断正确的是A.该反应中 作氧化剂 作氧化剂 |
| B.反应过程中溶液的pH变小 |
| C.氧化产物与还原产物的物质的量之比为5∶2 |
| D.若有1mol氧化剂参加反应,转移电子的物质的量为2mol |
您最近一年使用:0次
9 . 已知16O、17O、18O均属于氧元素。科学研究发现氧元素除了能形成O2、O3外,还能在一定条件下形成以亚稳态存在的分子四聚氧O4,也能在一个大气压和-218.79℃以下形成红氧O8,下列说法正确的是
A. 、 、 、 、 属于同一种核素 属于同一种核素 | B.O4和O8互为同位素 |
| C.O4的摩尔质量为64g | D.16O2和18O2的化学性质相同 |
您最近一年使用:0次
10 . 设NA代表阿伏加德罗常数的值,下列说法正确的是
| A.物质的量浓度为0.5mol/L的AlCl3溶液中,含有的Cl-数目为1.5NA |
| B.标准状况下,2.8gCO和N2的混合气体的体积无法确定 |
| C.相同质量的2H2O和H218O所含中子数相同 |
| D.5.6g铁与7.1g氯气充分反应,转移电子数为0.3NA |
您最近一年使用:0次



