1 . 三氯化铬是有机金属化学中的重要原料,为紫色晶体,熔点为83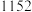 ℃,易潮解,高温下易被氧气氧化。实验室用
℃,易潮解,高温下易被氧气氧化。实验室用 和
和 加热到
加热到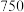 ℃时可制取
℃时可制取 ,同时还生成
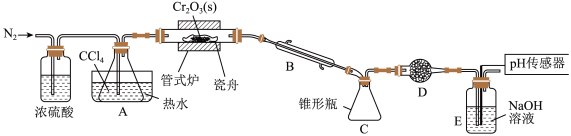
,同时还生成 ,其装置图如下
,其装置图如下 加热及夹持装置略去
加热及夹持装置略去 ,请回答下列问题:
,请回答下列问题:
已知: 沸点
沸点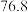 ℃;
℃; 有毒,沸点
有毒,沸点 ℃,遇水剧烈水解生成刺激性气味的气体。
℃,遇水剧烈水解生成刺激性气味的气体。
Ⅰ.制备 :
:
(1)仪器 的名称是
的名称是______ 。
(2)装置 、
、 的作用分别是
的作用分别是______ 、______ 。
(3)实验前先通入一段时间 的目的是
的目的是______ 。
(4)制备 的化学方程式为
的化学方程式为______ 。
(5)判断反应结束的依据是______ 。
Ⅱ.测定 纯度:
纯度:
称取 产品,在强碱性条件下,加入过量
产品,在强碱性条件下,加入过量 溶液,并小火加热,使
溶液,并小火加热,使 元素完全转化为
元素完全转化为 ;继续加热一段时间,冷却后配制成
;继续加热一段时间,冷却后配制成 溶液;取出
溶液;取出 ,滴加适量硫酸酸化后,用新配制的
,滴加适量硫酸酸化后,用新配制的 标准液滴定至终点,消耗标准液
标准液滴定至终点,消耗标准液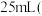 已知
已知 被
被 还原为
还原为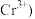 。
。
(6) 被
被 氧化成
氧化成 的离子方程式为
的离子方程式为______ 。
(7)产品中 的纯度为
的纯度为______  杂质不参与反应
杂质不参与反应 。
。
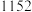 ℃,易潮解,高温下易被氧气氧化。实验室用
℃,易潮解,高温下易被氧气氧化。实验室用 和
和 加热到
加热到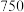 ℃时可制取
℃时可制取 ,同时还生成
,同时还生成 ,其装置图如下
,其装置图如下 加热及夹持装置略去
加热及夹持装置略去 ,请回答下列问题:
,请回答下列问题:
已知:
 沸点
沸点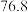 ℃;
℃; 有毒,沸点
有毒,沸点 ℃,遇水剧烈水解生成刺激性气味的气体。
℃,遇水剧烈水解生成刺激性气味的气体。Ⅰ.制备
 :
:(1)仪器
 的名称是
的名称是(2)装置
 、
、 的作用分别是
的作用分别是(3)实验前先通入一段时间
 的目的是
的目的是(4)制备
 的化学方程式为
的化学方程式为(5)判断反应结束的依据是
Ⅱ.测定
 纯度:
纯度:称取
 产品,在强碱性条件下,加入过量
产品,在强碱性条件下,加入过量 溶液,并小火加热,使
溶液,并小火加热,使 元素完全转化为
元素完全转化为 ;继续加热一段时间,冷却后配制成
;继续加热一段时间,冷却后配制成 溶液;取出
溶液;取出 ,滴加适量硫酸酸化后,用新配制的
,滴加适量硫酸酸化后,用新配制的 标准液滴定至终点,消耗标准液
标准液滴定至终点,消耗标准液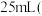 已知
已知 被
被 还原为
还原为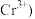 。
。(6)
 被
被 氧化成
氧化成 的离子方程式为
的离子方程式为(7)产品中
 的纯度为
的纯度为 杂质不参与反应
杂质不参与反应 。
。
您最近一年使用:0次
2 . 三种气体 X、Y、Z 的相对分子质量关系为 Mr(X)<Mr(Y)=0.5Mr(Z),下列说法正确的是
| A.原子数相等的三种气体,质量最大是 Z |
| B.若一定条件下,三种气体体积均为2.24L,则它们的物质的量一定均为0.1 mol |
| C.同温同压下,同质量的三种气体,气体密度最小的是X |
| D.同温下,体积相同的两容器分别充agY气体和2agZ气体,则压强之比为1:2 |
您最近一年使用:0次
2022-12-25更新
|
1613次组卷
|
52卷引用:重庆市万州纯阳中学2022-2023学年高三上学期8月月考化学试题
重庆市万州纯阳中学2022-2023学年高三上学期8月月考化学试题2016届湖北省武汉市高三下学期2月调研理综化学试卷2016-2017学年江西省南昌二中高一上月考一化学试卷2017届辽宁省沈阳东北育才学校高三上期中模拟化学卷2016届辽宁省葫芦岛市第一高级中学高三上学期第二次周考理综化学试卷河北省“名校联盟”(五校联考)2018届高三上学期教学质量监测(一)化学试题湖北省武汉市部分重点中学2017-2018学年高一上学期期中考试化学试题山东省沂水县第一中学2018届高三下学期第2次模拟化学试题【全国百强校】河北省邢台市第一中学2017-2018学年高二下学期第三次月考化学试题(已下线)【备战2019年浙江新高考-考点】——考点02 物质的量【市级联考】山东省泰安市2019届高三上学期期中考试化学试题【校级联考】安徽省滁州市定远县西片区2018-2019学年高一上学期期中考试化学试题云南省新平县一中2018-2019学年高一上学期12月月考化学试题云南省元江县一中2018-2019学年高一下学期2月份考试化学试题(已下线)2019年7月2日 《每日一题》2020年高考一轮复习-阿伏加德罗定律及其推论的应用河北省秦皇岛一中2019-2020学年高一上学期第一次月考化学试题四川省广安市邻水县邻水实验学校2019-2020学年高一上学期第一次月考化学试题河北省邯郸市2019-2020学年高一上学期期中考试化学试题内蒙古第一机械制造(集团)有限公司第一中学2019-2020学年高一10月月考化学试题广西南宁市第三中学2019-2020学年高一上学期期中考试化学试题安徽省合肥十中2019-2020学年高一上学期期中考试化学试题云南省云县第一中学2019-2020学年高二12月月考化学试题1内蒙古包钢第一中学2019-2020学年高一上学期10月月考化学试题广东省江门市第一中学2019-2020学年高一上学期10月月考化学试题山西省忻州市第一中学2019-2020学年高一上学期第二次月考化学试题安徽省合肥市肥东县第二中学2020-2021学年高一上学期期末考试化学试题内蒙古呼和浩特市第十六中学2020-2021学年高一上学期第一次质量检测化学试题专题1 第2课时气体摩尔体积-高中化学苏教2019版必修第一册(已下线)解密02 物质的量(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密02 物质的量(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)课时11 物质的量、气体摩尔体积-2022年高考化学一轮复习小题多维练(全国通用)福建省厦门一中2019-2020学年高一上学期第一次月考(10月)化学试题(已下线)考点02 化学用语和常用化学计量-备战2022年高考化学学霸纠错(全国通用)(已下线)解密02 物质的量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)提升卷02-【新高考新题型】2022年高考化学选择题标准化练习20卷(山东专用)(已下线)解密02 物质的量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)化学-2022年高考押题预测卷02(山东卷)(已下线)必刷卷04-2022年高考化学考前信息必刷卷(山东专用)(已下线)考点02 物质的量 气体摩尔体积-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第04讲 物质的量 气体摩尔体积 (练)-2023年高考化学一轮复习讲练测(新教材新高考)黑龙江省龙西北八校联合体2022-2023学年高三上学期开学考试化学试题河南省南阳市第一中学校2023届高三上学期第二次阶段考试化学试题(已下线)专题五 化学常用计量与化学计算-实战高考·二轮复习核心突破山东莒县第一中学2022-2023学年高一上学期12月月考化学试题山东省烟台第一中学2022-2023学年高一上学期月考化学试题山东省烟台第一中学2022-2023学年高一上学期期末调研化学试题安徽省安庆市桐城中学2022-2023学年高一上学期第二次教学质量检测化学试题第二章 物质的量化学实验基本技能 第6讲 物质的量山东省枣庄市第八中学南校2022-2023学年高一1月线上测试化学试题河北省石家庄二中教育集团2022-2023学年度高一年级上学期期末考试化学试题广西浦北中学2023-2024学年高一上学期10月月考化学试题福建省泉州市安溪一中、养正中学、惠安一中、实验中学2023-2024学年高一上学期期中考化学试题
3 . 现有如下反应: (提示:BrF3中F为
(提示:BrF3中F为 价),下列判断错误的是
价),下列判断错误的是
 (提示:BrF3中F为
(提示:BrF3中F为 价),下列判断错误的是
价),下列判断错误的是| A.BrF3既是氧化剂,又是还原剂 |
| B.被氧化的原子数与被还原的原子数之比为3∶2 |
| C.每当消耗3molBrF3,就有5molH2O被还原 |
| D.若反应转移3mol电子,则生成标准状况下11.2LO2 |
您最近一年使用:0次
名校
解题方法
4 . X、Y、Z、W是四种原子序数依次增大的短周期元素,W的最外层电子数比X的最外层电子数少1个,X、Y、Z为同一周期元素,X、Y、Z组成一种化合物(ZXY)2的结构式如图所示。下列说法错误的是
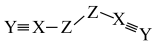
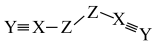
| A.化合物W2Z3是良好的耐热材料 |
| B.化合物(ZXY)2中Z元素的化合价为﹣2 |
| C.Y的氧化物对应的水化物可能是弱酸 |
| D.X元素能形成多种同素异形体 |
您最近一年使用:0次
10-11高二上·甘肃武威·阶段练习
名校
解题方法
5 . 在FeCl3、CuCl2、FeCl2的混合溶液中,Fe3+、Cu2+、Fe2+的物质的量之比为3:2:1,现加入适量铁粉,使溶液中三种离子物质的量浓度之比变为1:2:4,则参加反应的铁粉和原溶液中Fe3+的物质的量之比为
| A.2:1 | B.1:2 | C.1:3 | D.1:4 |
您最近一年使用:0次
2021-09-09更新
|
1685次组卷
|
28卷引用:重庆市三峡名校联盟2020-2021学年高一上学期12月联考化学试题
重庆市三峡名校联盟2020-2021学年高一上学期12月联考化学试题(已下线)2010年甘肃省武威五中高二11月月考化学试卷2015届河北省邯郸市高三上学期1月教学质量检测化学试卷2014-2015江西省新余市高一上学期期末考试化学试卷2014-2015学年辽宁师大附中高二下学期期末考试化学试卷2015-2016学年陕西省长安区一中高一上期末化学试卷(已下线)2019高考备考一轮复习精品资料 第三章 金属及其化合物 第3讲 铁及其化合物【押题专练】【全国百强校】黑龙江省哈尔滨市第六中学2018-2019学年高一上学期12月月考化学试题安徽省阜阳市第三中学2018-2019学年高一上学期小期末考试(期末模拟)化学试题河北省大名县第一中学2020届高三9月月考化学试题河北省武安市第一中学2020届高三9月月考化学试题甘肃省兰州市第一中学2020届高三9月月考化学试题宁夏石嘴山市第三中学2019-2020学年高一上学期第二次(12月)月考化学试题安徽省安庆一中2018-2019学年高一上学期期末考试化学试题安徽省太和第一中学2019-2020学年高一上学期期末考试化学试题人教版高中化学必修1第三章《金属及其化合物》测试卷2专题1.3 氧化还原反应(综合提升卷)——巅峰冲刺2020年高考化学二轮专项提升(已下线)3.1.2 铁的氢氧化物 铁盐和亚铁盐练习(1)——《高中新教材同步备课》(人教版 必修第一册)(已下线)第03章 铁 金属材料(B卷能力提高篇)——2020-2021学年高一化学必修第一册同步单元AB卷(新教材人教版)人教版(2019)高一必修第一册第三章 铁 金属材料 素养拓展区人教版(2019)高一必修第一册 第三章素养检测江西省鹰潭市第一中学2021届高三上学期期中考试化学试题四川省仁寿第一中学校南校区2020-2021学年高一下学期开学考试化学试题(已下线)8.1 铁及其化合物-2020-2021学年秋季班高二上学期化学教材知识点精讲练(沪科版)(已下线)3.1.2 不同价态铁元素之间的转化-2021-2022学年高一化学课后培优练(鲁科版2019必修第一册)黑龙江省七台河市勃利县高级中学2021-2022学年高三上学期期中考试化学试题广东省普宁市华侨中学2021—2022学年高一上学期第三次月考化学试题陕西省延安子长市中学2021-2022学年高三上学期期中考试化学试题
13-14高三·宁夏银川·阶段练习
名校
解题方法
6 . 足量铜与一定量的浓硝酸反应,得到硝酸铜溶液和二氧化氮、一氧化氮的混合气体2.24L(标准状况),这些气体与一定体积(标准状况)氧气混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入4mol·L-1氢氧化钠溶液至铜离子恰好完全沉淀,则消耗氢氧化钠溶液的体积是50mL,下列说法正确的是
| A.混合气体中含二氧化氮1.12L |
| B.消耗氧气的体积为1.68L |
| C.此反应过程中转移的电子为0.3mol |
| D.参加反应的硝酸是0.4mol |
您最近一年使用:0次
2021-08-25更新
|
797次组卷
|
30卷引用:2016届重庆市万州第二高级中学高三上学期期中测试理综化学试卷
2016届重庆市万州第二高级中学高三上学期期中测试理综化学试卷重庆市第七中学校2021-2022学年高一下学期3月月考化学试题(已下线)2015届宁夏银川一中高三第四次月考化学试卷2014-2015吉林省松原市扶余县一中高一上学期期末化学试卷2015届山东省滕州市三中上学期高三第四次月考理综化学试卷2016届河南省扶沟县高级中学高三上学期开学考试化学试卷2016届河南省三门峡市陕州中学高三上学期第一次精英对抗赛化学试卷2015-2016学年河北省冀州中学高一下开学考试化学试卷2016届河南省信阳市鸡公山风景区学校高三下2月月考化学试卷2015-2016学年安徽省六安一中高一下周末作业二化学试卷2015-2016学年安徽师大附中高一下学期期中考查化学试卷2015-2016学年山东省淄博六中高一下学科竞赛化学试卷2017届广西桂林市第十八中学高三上第二次月考化学试卷2018届高三一轮复习化学:考点21-铜及其化合物性质探究(已下线)《考前20天终极攻略》-5月26日 元素及其化合物福建省三明市第一中学2018-2019学年高二上学期开学考化学试题云南省新平县一中2018-2019学年高一上学期12月月考化学试题贵州省黔南布依族苗族自治州龙里中学2019-2020学年高一上学期期末考试化学试题辽宁省大连市一〇三中学2019-2020学年高一下学期期中考试化学试题河南省漯河市临颍县南街高级中学2020届高三阶段性测试化学试题安徽省芜湖市2021届高三第二次月考化学试题江西省高安中学2020-2021学年高一上学期期末考试化学试题四川省邻水实验学校2020-2021学年高一下学期第一次月考化学试题福建省福州第三中学2020-2021学年高一下学期期中考化学试题(已下线)专题02 氮及其化合物【专项训练】-2020-2021学年高一化学下学期期末专项复习(人教版2019必修第二册)(已下线)专题13 氮及其化合物 (热点讲义)-2022年高三毕业班化学常考点归纳与变式演练 浙江省诸暨市第二高级中学2020-2021学年高二下学期期中考试化学试题内蒙古自治区包钢第一中学2021-2022学年高三上学期10月月考化学试题云南省普洱市镇沅彝族哈尼族拉祜族自治县第一中学2021-2022学年高一下学期4月份考试化学试题湖南省怀化市沅陵县第一中学2021-2022学年高一下学期第一次月考化学试题
12-13高二下·黑龙江大庆·期末
名校
解题方法
7 . 铁、铝各1mol组成的混合物溶于一定量的盐酸,恰好完全反应后,再加入3molNa2O2固体使之充分反应,最终产物是
| A.Fe(OH)2、Al(OH)3、NaCl |
| B.Fe(OH)2、Al(OH)3、NaAlO2、NaCl |
| C.Fe(OH)3、NaAlO2、NaCl |
| D.Fe(OH)3、Al(OH)3、NaAlO2、NaCl |
您最近一年使用:0次
2021-05-22更新
|
743次组卷
|
7卷引用:重庆市乌江新高考协作体2023-2024学年高一下学期第二阶段性学业质量联合调研抽测化学试题
名校
8 . 探究是培养创新精神和实践能力的手段。用如下装置探究氯气的性质,图中三支试管口均放置浸有NaOH溶液的棉花。下列对实验现象的分析错误的是
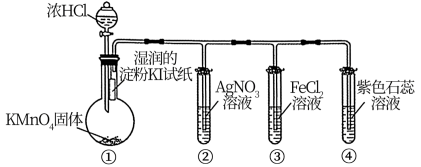

| A.①中淀粉KI试纸变蓝,说明氯气的氧化性强于碘 |
| B.②中产生白色沉淀,说明氯气与水反应生成Cl— |
| C.③中的溶液变为棕黄色,说明氯气有氧化性 |
| D.④溶液先变红后褪色,说明氯水有酸性和漂白性 |
您最近一年使用:0次
2021-03-18更新
|
5172次组卷
|
27卷引用:重庆市西南大学附中2020-2021学年高三下学期第四次月考化学试题
重庆市西南大学附中2020-2021学年高三下学期第四次月考化学试题重庆市育才中学校2022-2023学年高一上学期期中考试化学试题广东省广州市2021届高三3月第一次模拟考试化学试题广东省广州市2021届高三下学期毕业班综合测试(一)化学试题(已下线)第四章能力提升检测卷(精练)-2022年高考化学一轮复习讲练测(已下线)第9周 周测卷-备战2022年高考化学周测与晚练(新高考专用)(已下线)专题07 非金属及其化合物-2022年高考化学二轮复习重点专题常考点突破练广东省广州市三校2021-202学年高一上学期期末联考化学试题福建省厦门市同安第一中学2021-2022学年高一下学期第一次月考(3月)化学试题(已下线)第12讲 富集在海水中的元素——卤素(练)-2023年高考化学一轮复习讲练测(全国通用)第二节 氯及其化合物 第2课时 氯气的实验室制法及氯离子的检验江西省赣州市赣县第三中学2023届高三上学期月考强化训练(B8)化学试题辽宁省北镇市满族高级中学2022-2023学年高三上学期第一次质量检测化学试题广东省广州市海珠外国语实验中学2022-2023学年高一上学期第二次月考化学试题河南省安阳市第一中学2022-2023学年高一上学期12月月考化学试题山东省临沂第一中学文峰校区2022-2023学年高一上学期期末考试化学试题四川省成都市树德中学2022-2023学年高一上学期期末复习化学试题福建省尤溪县第七中学2022-2023学年高一下学期第一次阶段检测化学试题湖南省永州市第一中学2022-2023学年高一上学期期末考试化学试题 河南大学附属中学2022-2023学年高一下学期第一次月考化学试题湖南师范大学附属中学2023-2024学年高一上学期期中考试化学试题天津市双菱中学2023-2024学年高一上学期期中考试化学试卷陕西省西安市长安区第一中学2023-2024学年高一上学期期中考试化学试题河北省邯郸市涉县第一中学2023-2024学年高一上学期12月月考 化学试卷四川省成都市成华区某校2023-2024学年高一上学期12月月考化学试题湖南省长沙市雅礼中学2023-2024学年高三上学期一模化学试题黑龙江省哈尔滨市宾县第二中学2023-2024学年高一上学期第三次月考化学试题
名校
解题方法
9 . 某化学兴趣小组在学习铁及其化合物知识时,做了如下探究实验:
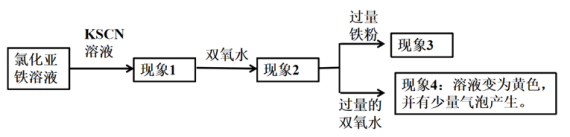
下列说法不正确 的是

下列说法
| A.若现象1有淡红色,说明有少量的Fe2+被氧化了 |
| B.现象2有血红色沉淀 |
| C.现象3为血红色褪去,说明发生了反应:2Fe3++Fe =3Fe2+ |
| D.由现象4可推测加入过量的双氧水后硫氰根离子可能被氧化生成了气体 |
您最近一年使用:0次
2021-01-30更新
|
468次组卷
|
6卷引用:重庆市2022-2023学年高一下学期6月月考化学试题
重庆市2022-2023学年高一下学期6月月考化学试题浙江省嘉兴市2020-2021学年高一上学期期末测试化学试题(已下线)【浙江新东方】在线化学60高一下(已下线)【浙江新东方】在线化学52高一上浙江之江教育评价2020-2021学年高一下学期期中联考化学试题浙江省乐清市知临中学2022-2023学年高一上学期期中考试化学试题(B)
名校
10 . 用蛇纹石(主要含3MgO·2SiO2·2H2O、FeO、Fe2O3、Al2O3及少量Cr2O3)制取MgO的工艺流程如图:
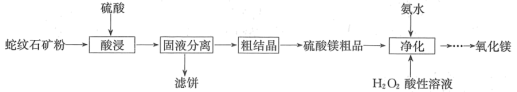
已知该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如表所示:
回答下列问题:
(1)“酸浸”时,当蛇纹石矿粉粒度一定、硫酸的浓度、活化剂用量及液固比一定时,提高浸取率还可采取的措施是___ (列举1条);3MgO·2SiO2·2H2O与硫酸反应的化学方程式为___ (生成产物之一为SiO2·nH2O)。
(2)“净化”过程包括“氧化”和“沉出杂质”两步骤。
①写出“氧化”时反应的离子方程式:___ 。
②“沉出杂质”加氨水时,应控制溶液pH的范围是___ 。
③氨水“净化”反应的温度对MgO纯度和产率的影响如图所示,在35~40℃,随温度升高,产率降低的主要原因是___ ;在25~50℃,温度越高,MgO纯度随温度升高而提高的主要原因是___ 。

(3)用2.76 t该蛇纹石(3MgO·2SiO2·2H2O含量为80%)原料按以上流程制取MgO,制取过程中Mg的损失率为6%,可以制得MgO的质量为___ kg。

已知该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如表所示:
| 金属离子 | Fe3+ | Al3+ | Cr3+ | Fe2+ | Mg2+ |
| 开始沉淀pH | 1.6 | 3.3 | 3.8 | 6.5 | 9.4 |
| 沉淀完全pH | 3.2 | 5.2 | 6.8 | 9.7 | 12.4 |
(1)“酸浸”时,当蛇纹石矿粉粒度一定、硫酸的浓度、活化剂用量及液固比一定时,提高浸取率还可采取的措施是
(2)“净化”过程包括“氧化”和“沉出杂质”两步骤。
①写出“氧化”时反应的离子方程式:
②“沉出杂质”加氨水时,应控制溶液pH的范围是
③氨水“净化”反应的温度对MgO纯度和产率的影响如图所示,在35~40℃,随温度升高,产率降低的主要原因是

(3)用2.76 t该蛇纹石(3MgO·2SiO2·2H2O含量为80%)原料按以上流程制取MgO,制取过程中Mg的损失率为6%,可以制得MgO的质量为
您最近一年使用:0次
2021-01-22更新
|
693次组卷
|
5卷引用:重庆市黔江新华中学校2021届高三毕业班第二次联合考试化学试题
重庆市黔江新华中学校2021届高三毕业班第二次联合考试化学试题河南省郑州、商丘市名师联盟2021届高三12月教学质量检测化学试题(已下线)大题02 化学工艺流程题(二)-【考前抓大题】备战2021年高考化学(全国通用)(已下线)专题11 无机工艺流程题—2022年高考化学二轮复习讲练测(全国版)-测试山东省菏泽市鄄城县第一中学2023-2024学年高三上学期1月月考化学试题



