名校
1 . 通过下列实验可以从废铜屑中制取CuSO4·5H2O。

下列说法正确的是

下列说法正确的是

| A.加入Na2CO3溶液的作用是除去废铜屑表面的油污 |
| B.“氧化”时反应的离子方程式:Cu+H2O2+2H+=Cu2++H2O |
| C.操作1是蒸发浓缩、冷却结晶 |
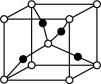
| D.将CuSO4·5H2O加热到1000℃以上会分解得到Cu2O,1个Cu2O晶胞(如图)中含1个氧原子 |
您最近一年使用:0次
2022-01-20更新
|
508次组卷
|
5卷引用:湖南省郴州市第二中学2022届高三下学期期中考试化学试题
湖南省郴州市第二中学2022届高三下学期期中考试化学试题江苏省无锡市普通高中2021-2022学年上学期高三期末调研考试化学试题(已下线)黄金卷1-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(江苏卷)江苏省泰州中学2021-2022学年高二下学期第一次质量检测化学试题(已下线)押江苏卷第9题 化学工艺流程选择题 -备战2022年高考化学临考题号押题(江苏卷)
名校
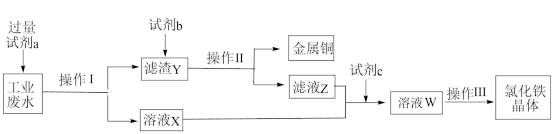
2 . 从某含有FeCl2、FeCl3、CuCl2的工业废液中回收铜并制备氯化铁晶体的流程如下:
则下列说法正确的是

则下列说法正确的是
| A.试剂a是铁、试剂b是稀盐酸 |
| B.操作Ⅰ、操作Ⅱ、操作Ⅲ所用仪器相同 |
| C.用KMnO4酸性溶液可检验溶液W中是否含有Fe2+ |
| D.试剂c是氯气,相应的反应为2Fe2++Cl2=2Fe3++2Cl- |
您最近一年使用:0次
2022-01-20更新
|
216次组卷
|
2卷引用:湖南省邵阳市新邵县2021-2022学年高一上学期期末质量检测化学试题
3 . 2020年突如其来的“新冠肺炎”使人们认识到日常杀菌消毒的重要性,其中含氯消毒剂在生产生活中有着广泛的用途。
Ⅰ.某化学兴趣小组用如图装置制备家用消毒液。

(1)写出装置B中反应的离子方程式___________ 。
(2)装置A中的溶液是___________ ,长玻璃导管的作用是___________ 。图中装置的连接顺序是B、___________ 。
(3)用化学方程式表示装置D中“84”消毒液的生成过程:___________ 。
(4)居家消毒时,不能将“84”消毒液与洁厕灵(主要成分是盐酸)混合使用,原因是___________ 。
(5)某温度下,将氯气通入NaOH溶液中,得到NaCl、NaClO和 的混合溶液,经测定
的混合溶液,经测定 与
与 的物质的量之比为1∶3。则该反应中,被氧化的Cl与被还原的Cl的质量之比为
的物质的量之比为1∶3。则该反应中,被氧化的Cl与被还原的Cl的质量之比为___________ 。
Ⅱ.世界卫生组织将定为A级高效安全灭菌消毒剂,它在食品保鲜、饮用水消毒等方面有广泛应用。
(6)消毒效率是用单位质量的消毒剂得电子数来表示的, 作消毒剂时和
作消毒剂时和 一样,还原产物均为
一样,还原产物均为 。
。 的消毒效率是
的消毒效率是 的
的___________ 倍(保留两位小数)。
Ⅰ.某化学兴趣小组用如图装置制备家用消毒液。

(1)写出装置B中反应的离子方程式
(2)装置A中的溶液是
(3)用化学方程式表示装置D中“84”消毒液的生成过程:
(4)居家消毒时,不能将“84”消毒液与洁厕灵(主要成分是盐酸)混合使用,原因是
(5)某温度下,将氯气通入NaOH溶液中,得到NaCl、NaClO和
 的混合溶液,经测定
的混合溶液,经测定 与
与 的物质的量之比为1∶3。则该反应中,被氧化的Cl与被还原的Cl的质量之比为
的物质的量之比为1∶3。则该反应中,被氧化的Cl与被还原的Cl的质量之比为Ⅱ.世界卫生组织将定为A级高效安全灭菌消毒剂,它在食品保鲜、饮用水消毒等方面有广泛应用。
(6)消毒效率是用单位质量的消毒剂得电子数来表示的,
 作消毒剂时和
作消毒剂时和 一样,还原产物均为
一样,还原产物均为 。
。 的消毒效率是
的消毒效率是 的
的
您最近一年使用:0次
4 . Ⅰ.次磷酸( )常用于化学镀银,反应为:
)常用于化学镀银,反应为: 。请回答下列问题:
。请回答下列问题:
(1) 中,P元素的化合价为
中,P元素的化合价为___________ ;该反应中,氧化产物是___________ 。
(2)配平该离子方程式:___________ 。
(3) 是一元弱酸,写出其与足量NaOH溶液反应的化学方程式:
是一元弱酸,写出其与足量NaOH溶液反应的化学方程式:___________ 。
(4)若该反应消耗 ,则镀件镀上银的质量为
,则镀件镀上银的质量为___________ g。
Ⅱ.酸性高锰酸钾溶液常用于物质的定性检验与定量分析。现用酸性高锰酸钾溶液测定某补血剂中亚铁的含量:称取含的补血剂a克,充分研磨后溶于水,配成100mL溶液,取25.00mL的该溶液与cmol/L的酸性高锰酸钾溶液反应,消耗酸性高锰酸钾溶液25.00mL。上述过程发生反应的化学方程式为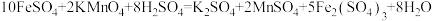 。
。
(5)该补血剂中 的质量分数为
的质量分数为___________ (用含a、c的代数式表示)。
 )常用于化学镀银,反应为:
)常用于化学镀银,反应为: 。请回答下列问题:
。请回答下列问题:(1)
 中,P元素的化合价为
中,P元素的化合价为(2)配平该离子方程式:
(3)
 是一元弱酸,写出其与足量NaOH溶液反应的化学方程式:
是一元弱酸,写出其与足量NaOH溶液反应的化学方程式:(4)若该反应消耗
 ,则镀件镀上银的质量为
,则镀件镀上银的质量为Ⅱ.酸性高锰酸钾溶液常用于物质的定性检验与定量分析。现用酸性高锰酸钾溶液测定某补血剂中亚铁的含量:称取含的补血剂a克,充分研磨后溶于水,配成100mL溶液,取25.00mL的该溶液与cmol/L的酸性高锰酸钾溶液反应,消耗酸性高锰酸钾溶液25.00mL。上述过程发生反应的化学方程式为
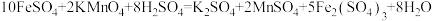 。
。(5)该补血剂中
 的质量分数为
的质量分数为
您最近一年使用:0次
名校
解题方法
5 . 下列说法正确的是
| A.用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗下口放出 |
| B.容量瓶、滴定管使用前均需用蒸馏水洗净并烘干 |
| C.用10 mL量筒量取2.5 mL浓硫酸用于配制一定浓度的稀硫酸 |
| D.向FeSO4溶液中滴加K3[Fe(CN)6]溶液,振荡,溶液变血红色 |
您最近一年使用:0次
名校
6 . 短周期主族元素X、Y、Z、Q、R的原子序数依次增大,X的简单阴离子与锂离子具有相同的电子层结构,Y原子最外层电子数等于内层电子数的2倍,Q的单质与稀硫酸剧烈反应生成X的单质。向100 mL X2R的水溶液中缓缓通入RZ2气体,溶液pH与RZ2体积关系如图。下列说法正确的是
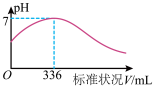

| A.RZ2通入BaCl2、Ba(NO3)2溶液中,现象不同 |
| B.X2R溶液的浓度为0.03 mol·L-1 |
| C.最简单气态氢化物的稳定性:Y>Z>R |
| D.工业上通常采用电解法冶炼Q的单质 |
您最近一年使用:0次
11-12高三上·湖南常德·阶段练习
解题方法
7 . 物质A~G均由短周期元素组成,A、B为非金属气体单质,B原子最外层电子数比次外层电子数的2倍还多1.甲、乙均为金属单质,且甲的原子半径在第三周期最大。各物质间的转化关系如下(部分生成物未给出,且未注明反应条件):
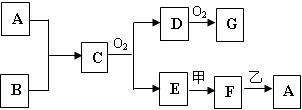
请回答:
(1)物质D的化学式_______ ;
(2)物质A的电子式是_______ ;
(3)实验室制取C的化学方程式_______ ;
(4)物质F和乙反应生成A的离子方程式_______ 。

请回答:
(1)物质D的化学式
(2)物质A的电子式是
(3)实验室制取C的化学方程式
(4)物质F和乙反应生成A的离子方程式
您最近一年使用:0次



