1 . 下表是元素周期表的一部分。按要求填写下列空白:
(1)②的某种核素常用于文物年代测定,该核素的符号为___________ 。⑧的简单阴离子的结构示意图为___________ 。
(2)①~⑧八种元素的最高价氧化物对应的水化物中,碱性最强的是___________ (填化学式,下同),酸性最强的是___________ 。
(3)元素④与⑦的简单气态氢化物中更稳定的是___________ (填化学式)。
(4)①与②形成的简单化合物的电子式为___________ ,⑤的氢氧化物中所含的化学键类型为___________ 。
(5)元素⑥常见氧化物溶于⑤的最高价氢氧化物水溶液的离子方程式为___________ 。
(6)为了证明⑦和⑧两种元素的非金属性强弱,下列说法或实验能提供证据的是___________(填序号)。
族 周期 | ⅠA | 0 | ||||||
| 一 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 二 | ② | ③ | ④ | |||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ |
(2)①~⑧八种元素的最高价氧化物对应的水化物中,碱性最强的是
(3)元素④与⑦的简单气态氢化物中更稳定的是
(4)①与②形成的简单化合物的电子式为
(5)元素⑥常见氧化物溶于⑤的最高价氢氧化物水溶液的离子方程式为
(6)为了证明⑦和⑧两种元素的非金属性强弱,下列说法或实验能提供证据的是___________(填序号)。
| A.比较两种元素的单质的熔点、沸点高低 |
| B.⑦的最高价含氧酸的酸性弱于⑧的最高价含氧酸的酸性 |
| C.将⑧的单质通入⑦的简单氢化物水溶液中 |
| D.比较⑦⑧形成的简单氢化物的相对分子质量的大小 |
您最近一年使用:0次
2 . 2019年是门捷列夫提出元素周期表150周年,根据元素周期表和周期律,回答问题。
Ⅰ.下表显示了元素周期表中短周期的一部分,①〜⑥代表6种短周期元素。其中②与氢元素形成的简单氢化物分子中含10个电子,能够使湿润的红色石蕊试纸变蓝。
(1)①在周期表中所处的位置为__________ 。
(2)与②同族的第四周期元素的原子结构示意图为__________ 。
(3)写出③与⑥的简单氢化物中沸点较高的分子的电子式__________ 。
(4)④的单质与水反应的离子方程式为__________ 。
(5)工业制取⑤的单质的化学方程式为__________ 。
Ⅱ.某同学欲利用下图装置验证同周期或同主族元素性质递变规律。
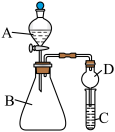
(6)干燥管D的作用是__________ 。
(7)证明非金属性:Cl>I。在A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液观察到C中溶液变蓝,则C试管中发生反应的离子方程式为__________ 。
(8)证明非金属性:N>C,在A中加稀硝酸,B中加碳酸钙,C中加澄清石灰水;观察到C中溶液__________ 的现象,该实验设计的原理是利用最高价氧化物对应水化物的酸性强弱来比较元素非金属性的强弱。
Ⅲ.到目前为止,元素周期表的第七周期已经被填满。
(9)请你设想一下,如果发现120号元素,下列有关它在周期表的位置或性质的说法错误的两项是__________ 。
①在第八周期ⅡA族;②最外层电子数是2;③比钙的熔点高;④与水反应放出氢气但比钙缓慢;⑤该元素单质需隔绝空气密封保存;⑥该元素的氧化物属于离子化合物
Ⅰ.下表显示了元素周期表中短周期的一部分,①〜⑥代表6种短周期元素。其中②与氢元素形成的简单氢化物分子中含10个电子,能够使湿润的红色石蕊试纸变蓝。
① | ② | ③ | ||||
④ | ⑤ | ⑥ |
(2)与②同族的第四周期元素的原子结构示意图为
(3)写出③与⑥的简单氢化物中沸点较高的分子的电子式
(4)④的单质与水反应的离子方程式为
(5)工业制取⑤的单质的化学方程式为
Ⅱ.某同学欲利用下图装置验证同周期或同主族元素性质递变规律。

(6)干燥管D的作用是
(7)证明非金属性:Cl>I。在A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液观察到C中溶液变蓝,则C试管中发生反应的离子方程式为
(8)证明非金属性:N>C,在A中加稀硝酸,B中加碳酸钙,C中加澄清石灰水;观察到C中溶液
Ⅲ.到目前为止,元素周期表的第七周期已经被填满。
(9)请你设想一下,如果发现120号元素,下列有关它在周期表的位置或性质的说法错误的两项是
①在第八周期ⅡA族;②最外层电子数是2;③比钙的熔点高;④与水反应放出氢气但比钙缓慢;⑤该元素单质需隔绝空气密封保存;⑥该元素的氧化物属于离子化合物
您最近一年使用:0次
2019-08-04更新
|
196次组卷
|
2卷引用:贵州省毕节市金沙县第一中学2020-2021学年高一下学期第一次月考化学试题
解题方法
3 . 几种元素在周期表中的位置如图所示,用化学用语(特殊标记的除外)回答下列问题:
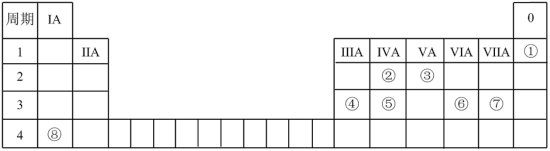
(1)表中所列元素中,①的元素符号是_______ ;金属性最强的是_______ ,该元素在周期表中的位置是_______ 。
(2)②有多种同素异形体,例如足球烯和_______ (填名称)
(3)元素③单质的化学式为_______ ;④的单质与 溶液反应的化学方程式为
溶液反应的化学方程式为_______ 。
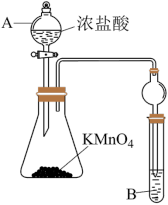
(4)已知 与浓盐酸在常温下反应生成氯气,利用如图装置验证氯元素和碘元素的非金属性强弱。仪器A的名称为
与浓盐酸在常温下反应生成氯气,利用如图装置验证氯元素和碘元素的非金属性强弱。仪器A的名称为_______ ,仪器B中盛放淀粉-碘化钾溶液,所发生的离子反应方程式为_______ ,当观察到_______ 现象时,即可证明非金属性: 。
。

(1)表中所列元素中,①的元素符号是
(2)②有多种同素异形体,例如足球烯和

(3)元素③单质的化学式为
 溶液反应的化学方程式为
溶液反应的化学方程式为(4)已知
 与浓盐酸在常温下反应生成氯气,利用如图装置验证氯元素和碘元素的非金属性强弱。仪器A的名称为
与浓盐酸在常温下反应生成氯气,利用如图装置验证氯元素和碘元素的非金属性强弱。仪器A的名称为 。
。
您最近一年使用:0次
解题方法
4 . 如图为化学“五元环”图案,在图案上分别写了 、
、 、
、 、
、 、
、 五种物质,图中相连的两种物质均可根据某种“分类依据”归属为一类,相交部分A、B、C、D为其相应的“分类依据”的代号。请回答下列问题:
五种物质,图中相连的两种物质均可根据某种“分类依据”归属为一类,相交部分A、B、C、D为其相应的“分类依据”的代号。请回答下列问题:

(1)分类依据A、B、C、D中可总结为“两种物质都是盐”的是___________ (填代号)。
(2)写出 的电离方程式:
的电离方程式:___________ 。
(3)潜水艇和消防员的呼吸面具中, 与呼出的
与呼出的 反应的化学方程式为
反应的化学方程式为___________ 。
(4)在烧杯中加入 蒸馏水,加热至沸腾,向烧杯中逐滴加入几滴饱和
蒸馏水,加热至沸腾,向烧杯中逐滴加入几滴饱和 溶液,继续加热至呈红褐色停止加热。证明有胶体生成的实验操作及现象是
溶液,继续加热至呈红褐色停止加热。证明有胶体生成的实验操作及现象是___________ 。
 、
、 、
、 、
、 、
、 五种物质,图中相连的两种物质均可根据某种“分类依据”归属为一类,相交部分A、B、C、D为其相应的“分类依据”的代号。请回答下列问题:
五种物质,图中相连的两种物质均可根据某种“分类依据”归属为一类,相交部分A、B、C、D为其相应的“分类依据”的代号。请回答下列问题:
(1)分类依据A、B、C、D中可总结为“两种物质都是盐”的是
(2)写出
 的电离方程式:
的电离方程式:(3)潜水艇和消防员的呼吸面具中,
 与呼出的
与呼出的 反应的化学方程式为
反应的化学方程式为(4)在烧杯中加入
 蒸馏水,加热至沸腾,向烧杯中逐滴加入几滴饱和
蒸馏水,加热至沸腾,向烧杯中逐滴加入几滴饱和 溶液,继续加热至呈红褐色停止加热。证明有胶体生成的实验操作及现象是
溶液,继续加热至呈红褐色停止加热。证明有胶体生成的实验操作及现象是
您最近一年使用:0次
2023-04-20更新
|
79次组卷
|
2卷引用:贵州省毕节市织金县第四中学2023-2024学年高一上学期11月考试化学试题
名校
5 . I.如图是利用电化学装置将SO2转化为重要的化工原料H2SO4的原理示意图。
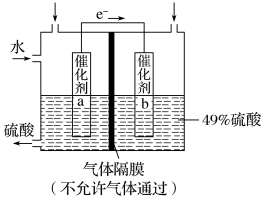
请回答下列问题:
(1)该装置将_______ 能转化为______ 能。
(2)催化剂b表面O2发生_______ 反应,其附近溶液酸性______ (填“增强”、“不变”或“减弱”)。
(3)催化剂a表面的电极反应式:_______ 。
II.某废料铁泥主要成分是Fe2O3、FeO和Fe,其他杂质不与硫酸反应。实验室用该废料提取Fe2O3,设计实验流程如图:

(4)步骤(I)充分反应后进行的实验操作名称是______ 。
(5)步骤(II)中加入H2O2溶液后需要适当加热但温度不能过高,原因是______ 。
(6)为了检验溶液B中是否有亚铁离子剩余,有同学提出只需要取少量溶液B于试管中并向其中滴加氢氧化钠溶液,然后观察现象即可证明。请你判断该同学的方法是否可行并说出理由______ 。
(7)步骤(III)中将NaOH溶液换成氨气也可以得到Fe(OH)3沉淀,反应的离子方程式为______ 。

请回答下列问题:
(1)该装置将
(2)催化剂b表面O2发生
(3)催化剂a表面的电极反应式:
II.某废料铁泥主要成分是Fe2O3、FeO和Fe,其他杂质不与硫酸反应。实验室用该废料提取Fe2O3,设计实验流程如图:

(4)步骤(I)充分反应后进行的实验操作名称是
(5)步骤(II)中加入H2O2溶液后需要适当加热但温度不能过高,原因是
(6)为了检验溶液B中是否有亚铁离子剩余,有同学提出只需要取少量溶液B于试管中并向其中滴加氢氧化钠溶液,然后观察现象即可证明。请你判断该同学的方法是否可行并说出理由
(7)步骤(III)中将NaOH溶液换成氨气也可以得到Fe(OH)3沉淀,反应的离子方程式为
您最近一年使用:0次
2023-05-19更新
|
711次组卷
|
2卷引用:贵州省遵义市仁怀市高中教育联盟2022-2023学年高一下学期5月期中考试化学试题
6 . 2021年,贵阳市空气质量优良率达98.9%,这得益于贵阳市对含硫化合物等排放的有效控制。回答下列问题:
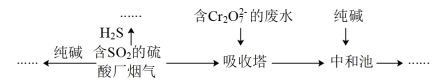
(1)燃煤的烟气中含有 ,为了治理雾霾,工厂采用如图所示多种方法实现烟气脱硫。
,为了治理雾霾,工厂采用如图所示多种方法实现烟气脱硫。
①写出 与
与 反应的化学方程式
反应的化学方程式___________ 。
②用含 的烟气处理含
的烟气处理含 的酸性废水时,所发生的离子反应为
的酸性废水时,所发生的离子反应为___________ :
___________ +___________
+___________ +___________
+___________ =___________
=___________ +___________
+___________ +___________
+___________
配平该离子反应,并判断该处理方式利用了 的
的___________ 性。
(2)实验室提供以下试剂:浓 、稀
、稀 、酸性
、酸性 溶液、
溶液、 溶液、Cu、品红溶液。若要实现
溶液、Cu、品红溶液。若要实现 的转化,可选择的试剂是
的转化,可选择的试剂是___________ ,所发生反应的化学方程式为___________ ;设计实验,证明能实现该转化的操作和现象为___________ 。
(1)燃煤的烟气中含有
 ,为了治理雾霾,工厂采用如图所示多种方法实现烟气脱硫。
,为了治理雾霾,工厂采用如图所示多种方法实现烟气脱硫。
①写出
 与
与 反应的化学方程式
反应的化学方程式②用含
 的烟气处理含
的烟气处理含 的酸性废水时,所发生的离子反应为
的酸性废水时,所发生的离子反应为___________
 +___________
+___________ +___________
+___________ =___________
=___________ +___________
+___________ +___________
+___________
配平该离子反应,并判断该处理方式利用了
 的
的(2)实验室提供以下试剂:浓
 、稀
、稀 、酸性
、酸性 溶液、
溶液、 溶液、Cu、品红溶液。若要实现
溶液、Cu、品红溶液。若要实现 的转化,可选择的试剂是
的转化,可选择的试剂是
您最近一年使用:0次
2022-07-14更新
|
376次组卷
|
2卷引用:贵州省贵阳市普通中学2021-2022学年高一下学期期末监测化学试题
解题方法
7 . 电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。
(1)检验溶液中Fe3+存在的常用试剂是___ ,证明Fe3+存在的现象是____ ,配制含Fe2+的溶液时,常常向溶液中加入少量___ ,使被氧气氧化形成的Fe3+还原为Fe2+。
(2)写出FeCl3溶液与金属铜发生反应的化学方程式:___ 。
(3)某工程师为了从使用过的腐蚀废液中回收铜,并重新获得FeCl3溶液,准备采用下列步骤:
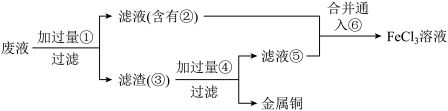
A.请写出上述实验中加入或生成的有关物质的化学式。
①___ ,②___ ,③___ ,④____ ,⑤____ ,⑥_____ 。
B.请写出相关反应的化学方程式。_______ 。
(1)检验溶液中Fe3+存在的常用试剂是
(2)写出FeCl3溶液与金属铜发生反应的化学方程式:
(3)某工程师为了从使用过的腐蚀废液中回收铜,并重新获得FeCl3溶液,准备采用下列步骤:

A.请写出上述实验中加入或生成的有关物质的化学式。
①
B.请写出相关反应的化学方程式。
您最近一年使用:0次
2020-01-07更新
|
268次组卷
|
4卷引用:贵州省黎平第二中学2019-2020学年高一上学期期末考试化学试题
贵州省黎平第二中学2019-2020学年高一上学期期末考试化学试题云南省临沧市耿马县民族中学2019-2020学年高一上学期12月月考化学试题广西壮族自治区崇左市天等县民族高中2019-2020学年高一上学期期末考试化学试题(已下线)3.1.1 铁及其化合物练习(1)——《高中新教材同步备课》(鲁科版 必修第一册)
名校
8 . 有下列物质:①液态氯化氢,②氯化铁溶液,③盐酸,④氯化铵晶体,⑤蔗糖溶液,⑥四氯化碳,⑦硫酸钡固体,⑧淀粉溶液,⑨熔融氢氧化钠,⑩铜。回答下面问题:
(1)上述物质中能够导电的是______ (填序号,下同),属于电解质的是_____ ,属于非电解质是____ 。
(2)写出④在溶液中的电离方程式:____________________________ 。
(3)证明⑧是胶体的方法是___________________ 。
(1)上述物质中能够导电的是
(2)写出④在溶液中的电离方程式:
(3)证明⑧是胶体的方法是
您最近一年使用:0次
2018-12-19更新
|
472次组卷
|
2卷引用:贵州省黔西县一中2018-2019学年高一第一学期12月考试化学试题
解题方法
9 . 电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。
(1)检验溶液中Fe3+存在的试剂是______________ ,证明Fe3+存在的现象是______________ 。
(2)写出FeCl3溶液与金属铜发生反应的离子方程式_________________
(3)某工程师为了从使用过的腐蚀溶液中回收铜,并重新获得FeCl3溶液,准备采用下列步骤:
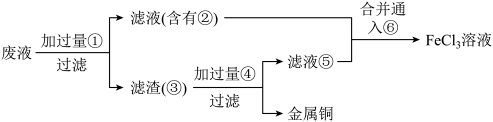
请写出上述实验中加入或生成的有关物质的化学式
①_____ ②_____ ③_____ ④_____ ⑤_____ ⑥_____ 。
(1)检验溶液中Fe3+存在的试剂是
(2)写出FeCl3溶液与金属铜发生反应的离子方程式
(3)某工程师为了从使用过的腐蚀溶液中回收铜,并重新获得FeCl3溶液,准备采用下列步骤:

请写出上述实验中加入或生成的有关物质的化学式
①
您最近一年使用:0次
名校
解题方法
10 . 铁是人类较早使用的金属之一,回答下列问题。
(1)下列所含铁元素只有还原性的物质是___________ (填字母)。
(2)血红蛋白(Hb)中的铁元素呈正二价,能与O2分子结合成氧合血红蛋白(HbO)从而有输送氧的能力。NaNO2因具有氧化性能使血红蛋白丧失与O2结合的能力,药品美蓝是其有效的解毒剂,下列说法中正确的是___________ (填字母)。
(3)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔(转化为Cu2+)来制造印刷电路板。写出FeCl3溶液与铜发生反应的化学方程式___________ ,若向FeCl3和CuCl2的混合溶液中加入一定量铁粉,最终有固体剩余,则下列有关说法中正确的是___________ (填字母)。
(4)高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂。工业上湿法制备高铁酸钾的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、 、Cl-、H2O。写出并配平该反应的离子方程式
、Cl-、H2O。写出并配平该反应的离子方程式___________ ;若反应过程中转移了0.3 mol电子,则还原产物的物质的量为___________ mol。
(5)某“铁基脱氧剂”的主要成分是还原Fe粉,使用一段时间后会部分变质为Fe2O3。将一包使用过一段时间后的脱氧剂用稀盐酸浸泡,浸泡过程中粉末表面有大量细小无色气泡产生。溶液中的反应有: 、
、 、
、___________ (写离子方程式)。
(1)下列所含铁元素只有还原性的物质是
A.Fe B.FeCl3 C.FeSO4
(2)血红蛋白(Hb)中的铁元素呈正二价,能与O2分子结合成氧合血红蛋白(HbO)从而有输送氧的能力。NaNO2因具有氧化性能使血红蛋白丧失与O2结合的能力,药品美蓝是其有效的解毒剂,下列说法中正确的是
A.药品美蓝发生还原反应 B.药品美蓝是还原剂 C.药品美蓝被还原
(3)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔(转化为Cu2+)来制造印刷电路板。写出FeCl3溶液与铜发生反应的化学方程式
A.固体中一定有铜 B.固体中一定有铁
C.溶液中一定有Fe2+ D.溶液中一定有Cu2+
(4)高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂。工业上湿法制备高铁酸钾的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、
 、Cl-、H2O。写出并配平该反应的离子方程式
、Cl-、H2O。写出并配平该反应的离子方程式(5)某“铁基脱氧剂”的主要成分是还原Fe粉,使用一段时间后会部分变质为Fe2O3。将一包使用过一段时间后的脱氧剂用稀盐酸浸泡,浸泡过程中粉末表面有大量细小无色气泡产生。溶液中的反应有:
 、
、 、
、
您最近一年使用:0次
2023-10-11更新
|
514次组卷
|
4卷引用:贵州省安顺市 镇宁布依族苗族自治县第一高级中学(镇宁实验学校)2023-2024学年高一上学期12月月考化学试题



