名校
解题方法
1 . 某硫酸厂以硫铁矿焙烧后的烧渣(其主要成分为 、
、 、
、 )为原料来制取铵明矾晶体
)为原料来制取铵明矾晶体 的一种工艺流程如图。
的一种工艺流程如图。
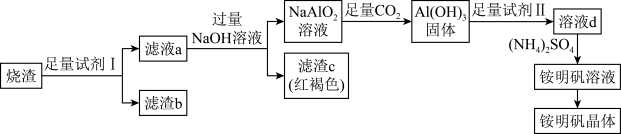
已知:① 是酸性氧化物,难溶于水,酸浸时不发生反应。
是酸性氧化物,难溶于水,酸浸时不发生反应。
② 固体可溶于
固体可溶于 等强碱溶液。
等强碱溶液。
请回答下列问题:
(1)写出 中含有的化学键类型:
中含有的化学键类型:_______ 。
(2)“试剂Ⅰ”为_______ (填试剂名称),“滤渣b”为_______ (填化学式)。
(3)写出“滤液a”和 溶液反应的离子方程式:
溶液反应的离子方程式:_______ 、_______ 。
(4)“滤渣c”的化学式为_______ ,证明铁元素已沉淀完全的实验方法是_______ 。
(5)向 溶液中通入足量
溶液中通入足量 的离子方程式为
的离子方程式为_______ 。
(6)从铵明矾溶液中获得铵明矾晶体的实验操作依次为蒸发浓缩、冷却结晶、_______ (填操作名称)、洗涤、干燥。
 、
、 、
、 )为原料来制取铵明矾晶体
)为原料来制取铵明矾晶体 的一种工艺流程如图。
的一种工艺流程如图。
已知:①
 是酸性氧化物,难溶于水,酸浸时不发生反应。
是酸性氧化物,难溶于水,酸浸时不发生反应。②
 固体可溶于
固体可溶于 等强碱溶液。
等强碱溶液。请回答下列问题:
(1)写出
 中含有的化学键类型:
中含有的化学键类型:(2)“试剂Ⅰ”为
(3)写出“滤液a”和
 溶液反应的离子方程式:
溶液反应的离子方程式:(4)“滤渣c”的化学式为
(5)向
 溶液中通入足量
溶液中通入足量 的离子方程式为
的离子方程式为(6)从铵明矾溶液中获得铵明矾晶体的实验操作依次为蒸发浓缩、冷却结晶、
您最近一年使用:0次
解题方法
2 . 我国食盐可分为原盐、精盐、特种食盐以及营养盐等,其中特种食盐又分为低钠盐、加碘盐、加硒盐、加锌盐、加铁盐等。低钠盐是以加碘食盐为基础,添加一定量 ,适用于中老年人和患有高血压病患者长期食用。加铁盐中添加一定量亚铁盐,如
,适用于中老年人和患有高血压病患者长期食用。加铁盐中添加一定量亚铁盐,如 ,适用于铁缺乏人群。
,适用于铁缺乏人群。
I.某一实验小组对低钠盐进行研究。
(1) 检验:用洁净的铂丝蘸取低钠盐固体,灼烧,直接观察火焰呈黄色,甲同学认为含
检验:用洁净的铂丝蘸取低钠盐固体,灼烧,直接观察火焰呈黄色,甲同学认为含 ,无
,无 。但乙同学进行实验,透过蓝色钴玻璃观察到火焰呈
。但乙同学进行实验,透过蓝色钴玻璃观察到火焰呈_______ 色,否定了甲同学的观点。
(2) 的含量测定:取
的含量测定:取 的低钠盐溶于水配成溶液,加足量稀硝酸和硝酸银溶液,充分反应后,得到干燥的白色沉淀质量为
的低钠盐溶于水配成溶液,加足量稀硝酸和硝酸银溶液,充分反应后,得到干燥的白色沉淀质量为 ,便可以计算低钠盐中
,便可以计算低钠盐中 的含量。你认为该方案是否可行?
的含量。你认为该方案是否可行?_______ (若可行,请写出含量表达式:若不可行,请写出不可行理由)。
Ⅱ.另一实验小组对加铁盐进行研究。
(3)配制溶液:准确称量 该加铁盐,配制
该加铁盐,配制 加铁盐溶液。需要使用的玻璃仪器:烧杯、量筒、玻璃棒、
加铁盐溶液。需要使用的玻璃仪器:烧杯、量筒、玻璃棒、 容量瓶、
容量瓶、_______ 。
(4)定性检验:检验该加铁盐中是否添加有 ,并检验其是否变质。实验小组设计了以下实验,请完成表格。
,并检验其是否变质。实验小组设计了以下实验,请完成表格。
(5)定量测定:加铁盐国标是含铁量为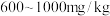 。取
。取 所配溶液,加入足量
所配溶液,加入足量 溶液,充分反应后过滤,加热固体至质量不再变化,称得剩余红棕色固体为
溶液,充分反应后过滤,加热固体至质量不再变化,称得剩余红棕色固体为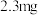 ,计算该盐含铁量为
,计算该盐含铁量为_______ 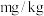 。
。
 ,适用于中老年人和患有高血压病患者长期食用。加铁盐中添加一定量亚铁盐,如
,适用于中老年人和患有高血压病患者长期食用。加铁盐中添加一定量亚铁盐,如 ,适用于铁缺乏人群。
,适用于铁缺乏人群。I.某一实验小组对低钠盐进行研究。
(1)
 检验:用洁净的铂丝蘸取低钠盐固体,灼烧,直接观察火焰呈黄色,甲同学认为含
检验:用洁净的铂丝蘸取低钠盐固体,灼烧,直接观察火焰呈黄色,甲同学认为含 ,无
,无 。但乙同学进行实验,透过蓝色钴玻璃观察到火焰呈
。但乙同学进行实验,透过蓝色钴玻璃观察到火焰呈(2)
 的含量测定:取
的含量测定:取 的低钠盐溶于水配成溶液,加足量稀硝酸和硝酸银溶液,充分反应后,得到干燥的白色沉淀质量为
的低钠盐溶于水配成溶液,加足量稀硝酸和硝酸银溶液,充分反应后,得到干燥的白色沉淀质量为 ,便可以计算低钠盐中
,便可以计算低钠盐中 的含量。你认为该方案是否可行?
的含量。你认为该方案是否可行?Ⅱ.另一实验小组对加铁盐进行研究。
(3)配制溶液:准确称量
 该加铁盐,配制
该加铁盐,配制 加铁盐溶液。需要使用的玻璃仪器:烧杯、量筒、玻璃棒、
加铁盐溶液。需要使用的玻璃仪器:烧杯、量筒、玻璃棒、 容量瓶、
容量瓶、(4)定性检验:检验该加铁盐中是否添加有
 ,并检验其是否变质。实验小组设计了以下实验,请完成表格。
,并检验其是否变质。实验小组设计了以下实验,请完成表格。| 步骤 | 操作 | 现象 | 结论 |
| 步骤1 | 取所配溶液,加入① | 无明显现象该 | 加铁盐中添加 且未变质 且未变质 |
| 步骤2 | 向步骤1所得溶液中加入② | ③ |
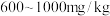 。取
。取 所配溶液,加入足量
所配溶液,加入足量 溶液,充分反应后过滤,加热固体至质量不再变化,称得剩余红棕色固体为
溶液,充分反应后过滤,加热固体至质量不再变化,称得剩余红棕色固体为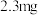 ,计算该盐含铁量为
,计算该盐含铁量为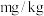 。
。
您最近一年使用:0次
解题方法
3 . 氯气是重要的化工原料,大量用于制造盐酸、有机溶剂和药品等。某小组同学利用下列装置在实验室制备氯气,并进行相关物质性质的探究。回答下列问题:
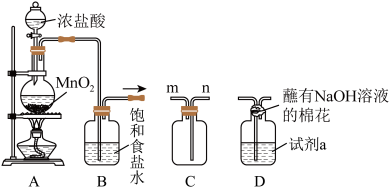
I.连接装置A→B→C,制备并收集 。
。
(1)装置A中发生反应的离子方程式_______ 。
(2)装置B中饱和食盐水的作用是_______ 。
(3)利用装置C收集 时,气体应该从
时,气体应该从_______ 口进(填“m”或“n”)。
Ⅱ.连接装置A→B→D,制备氯水。
(4)装置D中试剂a为 ,通入
,通入 即可制得氯水,则
即可制得氯水,则 与水反应的化学方程式为
与水反应的化学方程式为_______ 。
(5)将装置D制备的氯水转移至三颈烧瓶内,将pH传感器、氯离子传感器、氧气传感器分别插入三颈烧瓶中(图1),用强光照射氯水,进行实验并采集数据,获得相关变化曲线。
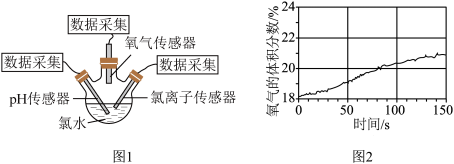
解释图2中曲线变化的原因_______ ,依此可判定实验过程中溶液 的变化趋势是
的变化趋势是_______ (填“增大”、“减小”或“不变”)。
Ⅲ.连接装置A→B→D,探究氯气的性质。
(6)将装置D中试剂a更换为紫色石蕊溶液,通入过量的 实验现象为
实验现象为_______ 。
(7)将装置D中试剂a更换为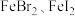 的混合溶液,通入一定量氯气,溶液中各种离子物质的量的变化如图3所示。已知还原性:
的混合溶液,通入一定量氯气,溶液中各种离子物质的量的变化如图3所示。已知还原性: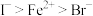 ,线段
,线段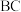 表示
表示_______ (填离子符号)物质的量的变化,原混合溶液中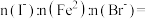
_______ 。


I.连接装置A→B→C,制备并收集
 。
。(1)装置A中发生反应的离子方程式
(2)装置B中饱和食盐水的作用是
(3)利用装置C收集
 时,气体应该从
时,气体应该从Ⅱ.连接装置A→B→D,制备氯水。
(4)装置D中试剂a为
 ,通入
,通入 即可制得氯水,则
即可制得氯水,则 与水反应的化学方程式为
与水反应的化学方程式为(5)将装置D制备的氯水转移至三颈烧瓶内,将pH传感器、氯离子传感器、氧气传感器分别插入三颈烧瓶中(图1),用强光照射氯水,进行实验并采集数据,获得相关变化曲线。

解释图2中曲线变化的原因
 的变化趋势是
的变化趋势是Ⅲ.连接装置A→B→D,探究氯气的性质。
(6)将装置D中试剂a更换为紫色石蕊溶液,通入过量的
 实验现象为
实验现象为(7)将装置D中试剂a更换为
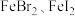 的混合溶液,通入一定量氯气,溶液中各种离子物质的量的变化如图3所示。已知还原性:
的混合溶液,通入一定量氯气,溶液中各种离子物质的量的变化如图3所示。已知还原性: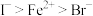 ,线段
,线段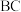 表示
表示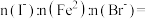

您最近一年使用:0次
解题方法
4 . 下图是中学化学中常见物质的转化关系,部分物质和反应条件略去。

(1)写出单质B与强碱溶液反应的离子方程式___________________________ ,写出由沉淀J生成H溶液的离子方程式_______________________________ 。
(2)溶液E中加入氨水时,先生成白色沉淀L,白色沉淀L最终变为红褐色沉淀G,写出L变为G的化学反应方程式______________________________ 。
(3) K是一种集消毒与净水为一体的新型净水剂,试写出G→K的化学方程式:_______________
(4)溶液I中所含金属离子是__________________ 。

(1)写出单质B与强碱溶液反应的离子方程式
(2)溶液E中加入氨水时,先生成白色沉淀L,白色沉淀L最终变为红褐色沉淀G,写出L变为G的化学反应方程式
(3) K是一种集消毒与净水为一体的新型净水剂,试写出G→K的化学方程式:
(4)溶液I中所含金属离子是
您最近一年使用:0次



