9-10高二下·山东潍坊·期末
名校
解题方法
1 . 要证明某溶液中不含Fe3+,而可能含有Fe2+,进行如下实验操作的最佳顺序为
①加入足量氯水②加入足量KMnO4(H+)溶液③加入少量KSCN溶液
①加入足量氯水②加入足量KMnO4(H+)溶液③加入少量KSCN溶液
| A.①③ | B.③① | C.①②③ | D.③②① |
您最近一年使用:0次
2023-01-09更新
|
366次组卷
|
113卷引用:新疆可克达拉市镇江高级中学2022-2023学年高一上学期期末考试化学试题
新疆可克达拉市镇江高级中学2022-2023学年高一上学期期末考试化学试题新疆石河子第一中学2023-2024学年高一上学期11月月考化学试题(已下线)2010年潍坊市高二下学期新课程期末测试化学(已下线)2010年江苏省泰兴市重点中学高三上学期第一次检测化学试题(已下线)2010年上海市吴淞中学高二上学期期中考试化学试卷(已下线)2010—2011年福建省厦门市杏南中学高一12月月考化学卷(已下线)2012届上海市松江二中高三上学期期中考试化学试卷(已下线)2011-2012学年上海市崇明中学高二上学期期中考试化学试卷(已下线)2011-2012学年江苏省泰州中学高三化学期中化学试卷(已下线)2011-2012学年内蒙古巴彦淖尔市中学高三期中考试化学试卷(已下线)2011-2012学年黑龙江省庆安三中高一上学期期末考试化学试卷(已下线)2011-2012学年云南省玉溪一中高一下学期期中考试化学试卷(已下线)2013届辽宁朝阳柳城高级中学高三上学期第二次月考化学试卷(已下线)2015河北保定某重点中学同步作业(必修1苏教版)3.2.2铜铁及其化合物(已下线)2014-2015学年福建省三明一中高一上学期期中化学试卷2015-2016学年黑龙江省哈尔滨六中高一上期末化学试卷2015-2016学年河北省冀州中学高一下开学考试化学试卷2015-2016学年广东省清远市高一上学期期末考试化学试卷2016届江西省宜春市铜鼓中学高三二模化学试卷2015-2016学年黑龙江省海林林业局一中高一上学期期末化学试卷2015-2016学年河南省安阳三十六中高二6月月考化学试卷2015-2016学年辽宁省庄河高中高一下期末化学试卷2015-2016学年山西晋城市高平市特立高级中学高二下期中理科化学卷2017届河北省故城县高级中学高三上学期期中化学试卷2016-2017学年福建省三明一中高一上期中化学卷2016-2017学年吉林省实验中学高一上学期期末化学试卷上海市金山中学2016-2017学年高二上学期期末等级考试化学试题宁夏银川市兴庆区2018届高三上学期第二次月考化学试题河南省鹤壁市淇滨高级中学2017-2018学年高一上学期第三次月考化学试题安徽省濉溪县临涣中学2017-2018学年高一上学期第二次月考化学试题河北省辛集中学2017-2018学年高一上学期第三次阶段考试化学试题湖北省长阳中学2017-2018学年高一化学上学期期末考试题山东省昌邑市第一中学2017-2018学年高一上学期第二次期末模拟考试化学试题湖南省石门县第一中学2016-2017学年高一下学期期末考试化学试题内蒙古阿拉善左旗高级中学2017-2018学年高二下学期期末考试化学试题黑龙江省伊春市第二中学2017-2018学年高二下学期期末考试化学试题人教版2017-2018学年高一化学必修1:3.2 几种重要的金属化合物 同步测试1(已下线)2019高考备考一轮复习精品资料 第三章 金属及其化合物 第3讲 铁及其化合物【教学案】【全国校级联考】新疆维吾尔自治区昌吉市教育共同体2019届高三上学期9月月考化学试题吉林省辽源市田家炳高级中学等五校2017-2018学年高一上学期期末联考(第64届)化学试题(已下线)2019高考热点题型和提分秘籍 第三章 金属及其化合物 第3讲 铁及其化合物 (教学案)【全国百强校】云南省玉溪市第一中学2018-2019学年高一上学期第一次月考化学试题山东省泰安市宁阳一中2018-2019学年高一上学期阶段性考试二(12月)化学试题【全国百强校】黑龙江省牡丹江市第一高级中学2018-2019学年高一上学期期末考试化学试题内蒙古开来中学2018-2019学年高二下学期期末考试化学试题新疆疏勒县八一中学2018-2019学年高一上学期期末考试化学试题黑龙江省牡丹江市第三高级中学2018-2019学年高二下学期期末考试化学试题云南省易门一中2019-2020学年高二开学考试化学试题(已下线)上海市华东师范大学第二附属中学2016-2017学年高二上学期期末考试化学试题上海市吴淞中学2017-2018学年高二上第一次月考化学试题上海市复旦中学2019-2020学年高二上学期第一次月考化学试题上海市上海交大附中2017-2018高二上期末化学题2019学年上海市奉贤区曙光中学高二化学上学期期中考试试卷福建省三明第一中学2019-2020学年高一上学期期中考试化学试题浙江省金华市东阳中学2019-2020学年高一上学期期中考试化学试题山东省德州市夏津县双语中学2019-2020学年高一12月月考化学试题宁夏青铜峡市高级中学2019-2020学年高一上学期期末考试化学试题甘肃省武威第八中学2019—2020学年高一上学期期末考试化学试题四川省三台县芦溪中学2017—2018学年高一上学期第三次月考化学试题四川省绵阳市三台县芦溪中学2017-2018学年高一上学期第三次月考化学试题上海市华东师大二附中2016-2017学年高二(上)期末化学试卷人教版高中化学必修一第三章《金属及其化合物》测试卷1山西省运城市盐湖五中2019-2020学年高一上学期期中考试化学试题上海市青浦二中2016届高三上学期8月摸底考试化学试题(已下线)上海市建平中学2013届高三第一次模拟化学试题(已下线)【南昌新东方】湾里一中2019-2020 高一(上)期末吉林省长春市九台区第四中学2019-2020高一上学期期末测试化学试题海南省海南枫叶国际学校2019-2020学年高一上学期期末考试化学试题甘肃省武威市第十八中学2019-2020学年高一上学期期末考试化学试题辽宁省阜新市第二高级中学2019-2020学年高一下学期期末考试化学试题上海南洋中学2019-2020学年高二上学期期中复习卷(沪科版)化学试题广东省中山市中山纪念中学2020届高三第二次质量检测化学试题(已下线)3.1.2 铁及其化合物之间的转化关系练习(1)——《高中新教材同步备课》(鲁科版 必修第一册)人教版(2019)高一必修第一册第三章 铁 金属材料 第一节 铁及其化合物 课时2 铁盐、亚铁盐鲁科版(2019)高一必修第一册第三章第1节 铁的多样性 课时1 亚铁盐和铁盐铁 铁的氧化物和铁的氢氧化物陕西省榆林市第十二中学2021届高三上学期第一次月考化学试题福建省莆田第二十五中学2021届高三上学期月考二化学试题(已下线)第三章 铁 金属材料(能力提升)-2020-2021学年高一化学单元测试定心卷(人教版2019必修第一册)(已下线)3.1.2 铁的重要化合物-2020-2021学年高一化学同步课堂帮帮帮(人教版2019必修第一册)(已下线)【浙江新东方】71.河北省石家庄市第二中学西校区2020-2021学年高一上学期12月月考化学试卷陕西省榆林市子洲中学2021届高三上学期第一次月考化学试题(已下线)专题05 金属及其重要化合物-备战2021届高考化学二轮复习题型专练辽宁省阜新市第二高级中学2020-2021学年高一上学期期末考试化学试题宁夏青铜峡市高级中学2020-2021学年高一上学期期末考试化学试题黑龙江省大庆市肇州县肇州中学2020-2021学年高一下学期第一次月考化学试题黑龙江省伊春市伊美区第二中学2020-2021学年高一上学期第三次月考化学试题新疆新源县第二中学2019-2020学年高一上学期期末考试化学试题福建省莆田第十五中学2018-2019学年高一下学期期中测试化学试题(苏教版2019)必修第二册专题9 金属与人类文明 第二单元 探究铁及其化合物的转化(已下线)微专题13 亚铁离子、三价铁离子的性质及检验-备战2022年高考化学考点微专题广东省普宁二中实验学校2021-2022学年高三上学期第一次月考化学试题黑龙江省双鸭山市第一中学2020-2021学年高一第二次月考化学试题上海市向明中学2021-2022学年高二上学期期中考试化学试题上海市向明中学2021-2022学年高三上学期期中考试化学试题浙江省乐清市知临中学2021-2022学年高一上学期期中考试化学(B)试题黑龙江省牡丹江市第三高级中学2021-2022学年高一上学期期末考试化学试题黑龙江省牡丹江市第三高级中学2021-2022学年高一下学期开学考试化学试题第三章 铁金属材料 本章复习提升(已下线)第07讲 铁及其化合物(练)-2023年高考化学一轮复习讲练测(新教材新高考)黑龙江省牡丹江市第三高级中学2022-2023学年高三上学期第一次月考化学试题黑龙江省嫩江市第一中学2021-2022学年高一下学期开学考试化学试题甘肃省武威市古浪县第二中学2021-2022学年高一上学期期末考试化学试题四川省凉山州宁南中学2022-2023学年高一上学期第二次月考化学试题辽宁省大石桥市第三高级中学2021-2022学年高一12月月考化学试题新疆阿克苏市实验中学2021-2022学年高一上学期期末考试化学(文)试题云南省大姚县第一中2021-2022学年高一下学期3月份考试化学试题新疆阿克苏市实验中学2021-2022学年高一上学期期末考试化学(理)试题吉林省永吉县第四中学2022-2023学年高一上学期期末考试化学试题黑龙江省富锦市第一中学2022-2023学年高一下学期第一次考试化学试题新疆昌吉州行知学校2022-2023学年高一下学期第一次月考化学试题第1课时 亚铁盐和铁盐四川省宜宾市兴文第二中学校2023-2024学年高一下学期开学化学试题
解题方法
2 . 金属及其化合物在人类生产、生活中发挥着重要作用。
(1)常温下,金属钠露置在空气中会发生变化,实验室通常把钠保存在_______ (填 “煤油”或“水”)中,金属钠着火时可以用_______ 灭火,钠元素所形成的氧化物呈淡黄色的是_______ (填“Na2O2”或“Na2O”)。
(2)实验室在保存含有Fe2+的溶液时,为了防止Fe2+变质,经常向其中加入_______ (填“铁粉”或“铜粉”);检验溶液是否变质时可用_______ 试剂检验(填化学式),若溶液已变质则会出现的现象为:_______ 。
(3)氯化铁可用于五金蚀刻,不锈钢广告牌上的图形和文字就是用氯化铁溶液蚀刻而成,该过程发生的主要反应的离子方程式为_______ ,该反应说明_______ (填化学式)具有氧化性。
(1)常温下,金属钠露置在空气中会发生变化,实验室通常把钠保存在
(2)实验室在保存含有Fe2+的溶液时,为了防止Fe2+变质,经常向其中加入
(3)氯化铁可用于五金蚀刻,不锈钢广告牌上的图形和文字就是用氯化铁溶液蚀刻而成,该过程发生的主要反应的离子方程式为
您最近一年使用:0次
3 . 构建知识网络是一种有效的学习方法,化学学习中的“价一类”二维图就是其中一种,如图所示是铁及其化合物的“价一类”二维图,下列有关叙述或化学方程式书写错误的是
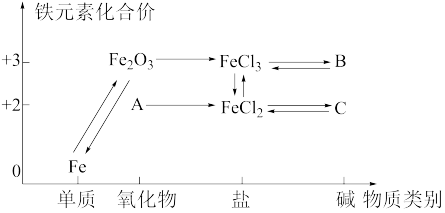
| A.物质A是氧化亚铁 |
B.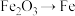 可能是 可能是 |
C. 在空气中的现象是白色沉淀迅速变成灰绿色,最终变成红褐色 在空气中的现象是白色沉淀迅速变成灰绿色,最终变成红褐色 |
D. 的反应类型只能是复分解反应 的反应类型只能是复分解反应 |
您最近一年使用:0次
2022-08-03更新
|
1586次组卷
|
7卷引用:新疆石河子第一中学2023-2024学年高一上学期11月月考化学试题
新疆石河子第一中学2023-2024学年高一上学期11月月考化学试题河南省郑州市巩义,中牟,登封等六县2021-2022学年高一上学期期末联考化学试题(已下线)第三章 铁 金属材料(A卷·知识通关练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第一册)四川省成都市第七中学2022-2023学年高一上学期期末考试化学试题(已下线)【知识图鉴】单元讲练测必修第一册第三单元01讲核心(已下线)考点巩固卷03 金属及其化合物(4大考点48题)-2024年高考化学一轮复习考点通关卷(新高考通用)江西省南昌市第十九中学2022-2023学年高一上学期12月第二次月考化学试卷
名校
解题方法
4 . 以含钴废催化剂(主要成分为Co、Fe、SiO2)为原料制取复合氧化钴(CoxOy)的流程如下:
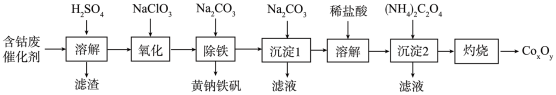
(1)用H2SO4溶解后过滤,得到的滤渣是_______ (填化学式)。将滤渣洗涤2~3次,再将洗液与滤液合并的目的是_______ 。
(2)在加热搅拌条件下加入NaClO3将Fe2+氧化成Fe3+,反应的离子方程式是_______ 。
(3)已知:铁氰化钾的化学式为K3[Fe(CN)6];亚铁氰化钾的化学式为K4[Fe(CN)6]
3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2 (蓝色沉淀)
4Fe3++3[Fe(CN)6]4-=Fe4[Fe(CN)6]3 (蓝色沉淀)
确定Fe2+是否氧化完全的方法是_______ 。
(仅供选择的试剂:铁氯化钾溶液、亚铁氯化钾溶液、铁粉、KSCN溶液)
(4)“除铁”工艺中加入适量的Na2CO3,调节pH约为2,使之生成黄钠铁矾[Na2Fe6(SO4)4(OH)12]沉淀,写出该反应的化学方程式:_______ 。

(1)用H2SO4溶解后过滤,得到的滤渣是
(2)在加热搅拌条件下加入NaClO3将Fe2+氧化成Fe3+,反应的离子方程式是
(3)已知:铁氰化钾的化学式为K3[Fe(CN)6];亚铁氰化钾的化学式为K4[Fe(CN)6]
3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2 (蓝色沉淀)
4Fe3++3[Fe(CN)6]4-=Fe4[Fe(CN)6]3 (蓝色沉淀)
确定Fe2+是否氧化完全的方法是
(仅供选择的试剂:铁氯化钾溶液、亚铁氯化钾溶液、铁粉、KSCN溶液)
(4)“除铁”工艺中加入适量的Na2CO3,调节pH约为2,使之生成黄钠铁矾[Na2Fe6(SO4)4(OH)12]沉淀,写出该反应的化学方程式:
您最近一年使用:0次
2022-06-24更新
|
284次组卷
|
3卷引用:新疆石河子第一中学2022-2023学年高三10月月考化学试题
名校
解题方法
5 . 验证Fe3+与Fe2+能够相互转化。
下列分析不合理的是
| 按下列顺序实验 | 对应现象 |
| ①向FeCl3溶液中加入过量铁粉 | i.溶液由黄色变成浅绿色 |
| ②滴加KSCN溶液 | ii.溶液无明显变化 |
| ③再滴加几滴氯水 | iii.溶液变红 |
| A.解释现象i的反应:2Fe3++Fe=3Fe2+ |
| B.实验②与③可以调换顺序 |
| C.溶液变红涉及的反应:Cl2+2Fe2+=2Cl-+2Fe3+ |
| D.氧化性:Cl2>Fe3+>Fe2+ |
您最近一年使用:0次
2022-04-04更新
|
1144次组卷
|
17卷引用:新疆石河子第二中学2021-2022学年高一上学期第二次月考化学试卷题
新疆石河子第二中学2021-2022学年高一上学期第二次月考化学试卷题北京市朝阳区2017-2018学年高一上学期期末考试化学试题【全国百强校】福建省三明市第一中学2018-2019学年高一下学期开学考试化学试题2020届高三化学二轮冲刺新题专练——仪器的连接和实验的操作顺序(提升练)高一必修第一册(鲁科2019)第3章 第1节 铁的多样性 教材帮人教版(2019)高一必修第一册 第三章 铁 金属材料 第一节 铁及其化合物 教材帮(已下线)【浙江新东方】双师151高一下江苏省苏州市相城区黄埭中学2020-2021学年高一下学期3月月考化学试题四川省内江市威远中学2021-2022学年高一上学期第二次月考化学试题第三章 铁金属材料 本章复习提升(已下线)3.1.2铁及其化合物-同步学习必备知识吉林省德惠市实验中学2022-2023学年高一上学期12月月考化学试题第2课时 铁盐和亚铁盐安徽省肥东县综合高中2022-2023学年高一上学期11月期中化学试题黑龙江省牡丹江市第三高级中学2023-2024学年高一上学期期末考试化学试题四川省绵阳市东辰中学2023-2024学年高一上学期12月份月考化学试卷贵州省安顺市 镇宁布依族苗族自治县第一高级中学(镇宁实验学校)2023-2024学年高一上学期12月月考化学试题
名校
解题方法
6 . 下列离子方程式正确的是
①碳酸氢钙溶液与过量烧碱溶液混合:
②碳酸镁与稀硫酸: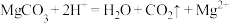
③醋酸与大理石: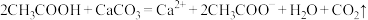
④向 溶液中逐滴加入
溶液中逐滴加入 溶液至
溶液至 刚好沉淀完全:
刚好沉淀完全:
⑤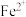 与
与 在酸性溶液中的反应:
在酸性溶液中的反应:
①碳酸氢钙溶液与过量烧碱溶液混合:

②碳酸镁与稀硫酸:
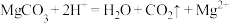
③醋酸与大理石:
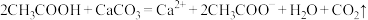
④向
 溶液中逐滴加入
溶液中逐滴加入 溶液至
溶液至 刚好沉淀完全:
刚好沉淀完全:
⑤
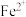 与
与 在酸性溶液中的反应:
在酸性溶液中的反应:
| A.①②③④⑤ | B.②③④ | C.②③④⑤ | D.①③④ |
您最近一年使用:0次
2021-01-29更新
|
233次组卷
|
6卷引用:新疆生产建设兵团第十师北屯高级中学2021-2022学年高一上学期10月月考化学试卷
名校
解题方法
7 . 在稀盐酸溶液中加入适量铁粉,反应完全后再加入足量NaOH溶液,放置片刻,从反应体系中观察到颜色的变化是( )
| A.无色→灰绿→红褐 | B.灰绿→红褐→蓝灰色→红棕 |
| C.无色→白色→浅绿→灰绿→红褐 | D.无色→浅绿→白色→灰绿→红褐 |
您最近一年使用:0次
2019-11-28更新
|
458次组卷
|
10卷引用:新疆石河子第二中学2021-2022学年高一上学期第二次月考化学试卷题
新疆石河子第二中学2021-2022学年高一上学期第二次月考化学试卷题湖北省沙市中学2019-2020学年高一上学期期中考试化学试题云南省富宁县三中2019-2020学年高一上学期期末考试化学试题(已下线)第3章 总结与检测(2)——《高中新教材同步备课》(鲁科版 必修第一册)(已下线)第三单元 物质的性质与转化(能力提升)-2020-2021学年高一化学必修第一册单元测试定心卷 (鲁科版2019)湖北省利川市第五中学2019-2020学年高一上学期期末选考化学试题黑龙江省哈尔滨市宾县第二中学2020-2021学年高一上学期第三次月考化学试题黑龙江省哈尔滨市宾县第二中学2021-2022学年高一上学期期末考试化学试题吉林省长春市汽车经济技术开发区第三中学2023-2024学年高一上学期期中考试化学试题宁夏回族自治区石嘴山市第三中学2023-2024学年高一上学期1月期末化学试题
名校
解题方法
8 . 下列关于离子共存或离子反应的说法正确的是
A.某无色溶液中可能大量存在H+、Cl-、MnO 、K+ 、K+ |
B.使红色石蕊试纸变蓝的溶液中,H+、Al3+、Cl-、NO |
| C.Fe2+与H2O2在酸性溶液中的反应:2Fe2++H2O2+2H+=2Fe3++2H2O |
D.稀硫酸与Ba(OH)2溶液的反应:H++SO +Ba2++OH-=BaSO4↓+H2O +Ba2++OH-=BaSO4↓+H2O |
您最近一年使用:0次
2017-12-09更新
|
155次组卷
|
4卷引用:新疆五家渠市兵团二中金科实验中学2021-2022学年高一下学期开学考试化学试题
解题方法
9 . 金属及其化合物在生产生活中占有极其重要的地位,请结合金属及其化合物的相关知识回答下列问题。
(1)含碳量在0.03%~2%之间某合金,是目前使用量最大的合金,这种合金是_______。
(2)FeCl3溶液用于腐蚀铜箔印刷线路板,反应的离子方程式为_______ 。
(3)某溶液中有Mg2+、Fe2+、Al3+、Cu2+等离子,向其中加入足量的Na2O2后,过滤,将滤渣投入足量的盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是 (填字母)
(4)Fe(NO3)3的高纯度结晶体是一种紫色潮解性固体,适合于制磁性氧化铁纳米粉末,工业上用废铁屑(含Fe和Fe2O3及其它不反应的物质)制取Fe(NO3)3晶体的方法如下:

①第1步反应若温度过高,将导致硝酸分解,浓硝酸受热分解的化学方程式为_____ 。
②磁性氧化铁的化学式为_____ ,试写出Fe2O3与硝酸反应的离子方程式_____ 。
③操作1的名称为_____ ,操作2的步骤为:_____ ,过滤,洗涤。
(1)含碳量在0.03%~2%之间某合金,是目前使用量最大的合金,这种合金是_______。
| A.铝合金 | B.青铜 | C.镁合金 | D.钢 |
(3)某溶液中有Mg2+、Fe2+、Al3+、Cu2+等离子,向其中加入足量的Na2O2后,过滤,将滤渣投入足量的盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是 (填字母)
| A.Mg2+ | B.Fe2+ | C.Al3+ | D.Cu2+ |

①第1步反应若温度过高,将导致硝酸分解,浓硝酸受热分解的化学方程式为
②磁性氧化铁的化学式为
③操作1的名称为
您最近一年使用:0次
2017-05-12更新
|
543次组卷
|
2卷引用:新疆石河子市兵团八师一四三团第一中学2018-2019学年高一上学期期末考试化学试题



