解题方法
1 . K3[Fe(C2O4)3]•3H2O(三草酸合铁酸钾)为亮绿色晶体。小李和小赵同学在老师的指导下探究K3[Fe(C2O4)3]•3H2O的热分解产物。
【查阅资料】①碱石灰可用于吸收CO2、水蒸气
②含有Fe2+的盐溶液可与K3[Fe(CN)6]发生反应产生蓝色沉淀
③含有Fe3+的盐溶液可与KSCN发生反应生成红色溶液
【提出问题】样品完全分解后,除水蒸气外还生成哪些产物?
(1)【猜想与假设】猜想一:气体产物中含有CO。
猜想二:气体产物中含有CO2。
猜想三:气体产物中含有______ 。
【实验探究】
(2)探究气体产物。
小李同学对气体产物进行探究,设计如图实验(夹持装置及部分装置省略):

实验中观察到装置B中澄清石灰水变浑浊,装置D中的固体变为红色。由此判断猜想______ 正确。
(3)探究固体产物。
小赵同学对固体产物进行如表探究:取K3[Fe(C2O4)3]•3H2O热分解后的固体产物(经实验证明无磁性物质)于试管中,加水充分溶解、过滤,再进行如表实验:
【实验结论】K3[Fe(C2O4)3]•3H2O的热分解产物有______ 种。
【查阅资料】①碱石灰可用于吸收CO2、水蒸气
②含有Fe2+的盐溶液可与K3[Fe(CN)6]发生反应产生蓝色沉淀
③含有Fe3+的盐溶液可与KSCN发生反应生成红色溶液
【提出问题】样品完全分解后,除水蒸气外还生成哪些产物?
(1)【猜想与假设】猜想一:气体产物中含有CO。
猜想二:气体产物中含有CO2。
猜想三:气体产物中含有
【实验探究】
(2)探究气体产物。
小李同学对气体产物进行探究,设计如图实验(夹持装置及部分装置省略):

实验中观察到装置B中澄清石灰水变浑浊,装置D中的固体变为红色。由此判断猜想
(3)探究固体产物。
小赵同学对固体产物进行如表探究:取K3[Fe(C2O4)3]•3H2O热分解后的固体产物(经实验证明无磁性物质)于试管中,加水充分溶解、过滤,再进行如表实验:
| 实验 | 现象 | 结论 | |
| 取滤液加入硫酸 | ① | 固体中含有K2CO3 | |
| 取滤渣加入硫酸溶解后,分成两份 | 一份中加入K3[Fe(CN)6] | ② | 固体中含有FeO |
| 另一份中加入KSCN | 溶液变为红色 | 固体中含有③ | |
您最近一年使用:0次
名校
解题方法
2 . 某混合气体可能由O2、CO、CO2中的一种或几种组成,为确定其组成,在老师的指导下,化学实验小组的同学对该混合气体的组成进行了如图的探究实验:
【查阅资料】脱氧剂(还原铁粉能够吸收氧气和水蒸气)。
【实验设计】用如图所示的装置进行实验(已略去夹持装置)。

【实验步骤】①检查装置气密性;②先通入一定量的氮气之后;③再通入该混合气体,点燃酒精灯。
【实验现象】步骤③实验过程中,A装置中无明显现象,B和F装置均出现白色沉淀,E装置中黑色粉末变成了红色。
(1)【实验结论】该混合气体由____ 组成。
【实验反思】
(2)B、C装置的作用分别是____ 、_____ 。
(3)步骤②先通入一定量氮气的目的是____ 。
(4)E装置中氧化铜粉末发生反应的化学方程式为____ 。
(5)F中需要处理的尾气主要成分是___ ,具体处理方法可以是____ 。
【查阅资料】脱氧剂(还原铁粉能够吸收氧气和水蒸气)。
【实验设计】用如图所示的装置进行实验(已略去夹持装置)。

【实验步骤】①检查装置气密性;②先通入一定量的氮气之后;③再通入该混合气体,点燃酒精灯。
【实验现象】步骤③实验过程中,A装置中无明显现象,B和F装置均出现白色沉淀,E装置中黑色粉末变成了红色。
(1)【实验结论】该混合气体由
【实验反思】
(2)B、C装置的作用分别是
(3)步骤②先通入一定量氮气的目的是
(4)E装置中氧化铜粉末发生反应的化学方程式为
(5)F中需要处理的尾气主要成分是
您最近一年使用:0次
2022-08-22更新
|
250次组卷
|
3卷引用:云南省昆明第一中学2022-2023学年高一上学期入学考试化学试题
云南省昆明第一中学2022-2023学年高一上学期入学考试化学试题(已下线)云南师范大学附属中学2023-2024学年高一上学期开学考试化学试题云南师范大学附属中学2023-2024学年高一上学期开学考试化学试题
3 . 膨松剂是一种食品添加剂。它在面包制作过程中发生反应产生气体,使面包变得松软,已知某膨松剂含碳酸氢钠、碳酸氢铵中的一种或两种,某化学兴趣小组对该膨松剂的成分进行了探究。在硬质玻璃管中加入该膨松剂,按如图所示连接好装置(装置气密性良好,且装置内空气已排尽)。
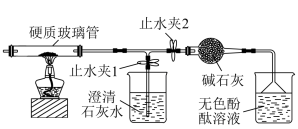
点燃酒精灯,观察现象:
(1)关闭止水夹2,打开止水夹1,澄清石灰水变浑浊,说明产物中有二氧化碳,溶液中发生反应的化学方程式为___ 。
(2)打开止水夹2,关闭止水夹1,观察到的现象是___ ,说明产物中有氨气。
(3)充分加热后,硬质玻璃管中有固体剩余。实验结论:该膨松剂的成分是___ 。

点燃酒精灯,观察现象:
(1)关闭止水夹2,打开止水夹1,澄清石灰水变浑浊,说明产物中有二氧化碳,溶液中发生反应的化学方程式为
(2)打开止水夹2,关闭止水夹1,观察到的现象是
(3)充分加热后,硬质玻璃管中有固体剩余。实验结论:该膨松剂的成分是
您最近一年使用:0次
解题方法
4 . 某化学兴趣小组进行了下列实验。
实验1:
(1)实验1-2中,燃烧的蜡烛熄灭的原因是___________ 。
(2)实验1-3中,反应生成氧气的化学方程式为___________ 。
实验2:
【提出问题】实验1-3中燃烧的蜡烛为什么会熄灭?
【猜想】I.蜡烛燃烧生成的二氧化碳导致其熄灭。
II.过氧化氢分解时吸收热量,蜡烛周围的温度降低到着火点以下,导致其熄灭。
III.过氧化氢分解产生的水雾导致蜡烛熄灭。
【进行实验】
【解释与结论】
(3)甲同学认为猜想I不成立,他的依据是___________ 。
(4)通过实验验证,可以得出猜想___________ (填序号)成立。
【反思与评价】
(5)依据上述实验,若保持实验1-3中蜡烛不熄灭,可采用的方法有___________ 。
实验3:取实验1、2中使用的二氧化锰样品进行图甲实验,加热时发现导管口有气泡产生,澄清石灰水变浑浊。于是小组同学对气体来源进行探究。
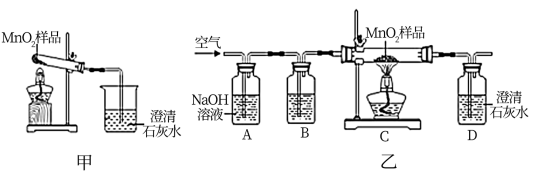
【猜想】二氧化锰样品中可能混有炭粉,炭粉发生反应生成了该气体。
(6)【进行实验】利用图乙所示的装置进行实验,其中B装置的作用是检验A中的反应是否完全,则B中的试剂是___________ ,实验中观察到D处澄清石灰水变浑浊。他们又用氮气代替空气(氮气不参与该实验中的任何反应),重复上述实验,发现D处澄清的石灰水也变浑浊。
(7)【结论】通过实验证明,二氧化锰中混有炭粉,炭粉与___________ 反应产生了二氧化碳。
实验1:
| 序号 | 1-1 | 1-2 | 1-3 |
| 操作 | 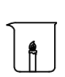 | 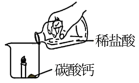 | 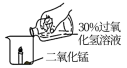 |
| 现象 | 燃烧的蜡烛保持原状 | 燃烧的蜡烛熄灭 | 剧烈反应,有大量气泡和水雾生成,燃烧的蜡烛熄灭了 |
(2)实验1-3中,反应生成氧气的化学方程式为
实验2:
【提出问题】实验1-3中燃烧的蜡烛为什么会熄灭?
【猜想】I.蜡烛燃烧生成的二氧化碳导致其熄灭。
II.过氧化氢分解时吸收热量,蜡烛周围的温度降低到着火点以下,导致其熄灭。
III.过氧化氢分解产生的水雾导致蜡烛熄灭。
【进行实验】
| 序号 | 2-1 | 2-2 | 2-3 |
| 操作 | 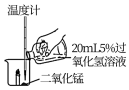 | 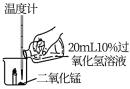 |  |
| 现象 | 有气泡产生,蜡烛火焰无明显变化,温度升高不明显 | 有较多气泡和少量水雾产生,蜡烛燃烧更旺,火焰明亮,温度升高较明显 | 剧烈反应,有大量气泡和水雾生成,燃烧的蜡烛熄灭,温度升高明显。 |
(3)甲同学认为猜想I不成立,他的依据是
(4)通过实验验证,可以得出猜想
【反思与评价】
(5)依据上述实验,若保持实验1-3中蜡烛不熄灭,可采用的方法有
实验3:取实验1、2中使用的二氧化锰样品进行图甲实验,加热时发现导管口有气泡产生,澄清石灰水变浑浊。于是小组同学对气体来源进行探究。

【猜想】二氧化锰样品中可能混有炭粉,炭粉发生反应生成了该气体。
(6)【进行实验】利用图乙所示的装置进行实验,其中B装置的作用是检验A中的反应是否完全,则B中的试剂是
(7)【结论】通过实验证明,二氧化锰中混有炭粉,炭粉与
您最近一年使用:0次
名校
5 . 小明同学为探究二氧化碳的性质,设计了下列实验:

(1)装置A中的实验现象是___ ,说明CO2具有的性质是___ 。
(2)装置B中倒入适量澄清的石灰水后,迅速拧紧软塑料瓶的瓶盖并振荡,实验现象是___ ,瓶内发生反应的化学反应方程式是___ 。
(3)取一朵用石蕊溶液染成紫色的干燥小花,将小花的一半用水喷湿,放入装置C中,可观察到的实验现象是___ ,此现象说明CO2具有的化学性质是___ (用化学方程式回答)。
(4)小明在查阅资料时发现镁条能在CO2中燃烧,他在装置D中进行实验,发现镁条剧烈燃烧,发出白光,放热,产生一种白色固体和一种黑色固体。向产生的固体中加入稀盐酸,无气泡产生,则镁条燃烧产生的白色固体是___ ;这个实验使你对燃烧条件产生的新认识是___ 。

(1)装置A中的实验现象是
(2)装置B中倒入适量澄清的石灰水后,迅速拧紧软塑料瓶的瓶盖并振荡,实验现象是
(3)取一朵用石蕊溶液染成紫色的干燥小花,将小花的一半用水喷湿,放入装置C中,可观察到的实验现象是
(4)小明在查阅资料时发现镁条能在CO2中燃烧,他在装置D中进行实验,发现镁条剧烈燃烧,发出白光,放热,产生一种白色固体和一种黑色固体。向产生的固体中加入稀盐酸,无气泡产生,则镁条燃烧产生的白色固体是
您最近一年使用:0次
2021高一·全国·专题练习
解题方法
6 . 按如图安装好实验装置,在收集满CO2气体的锥形瓶中滴加足量的NaOH浓溶液,可以很快地观察到烧杯中水倒吸入锥形瓶中,请按下列要求回答问题:

(1)锥形瓶中发生反应的化学方程式为____ 。
(2)发生倒吸的原因是____ 。
(3)受此原理启发,某同学又设计出以下装置,请分别写出两个装置中发生的实验现象:
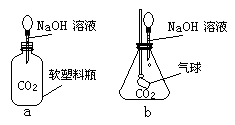
a装置:_____ ;b装置:____ 。

(1)锥形瓶中发生反应的化学方程式为
(2)发生倒吸的原因是
(3)受此原理启发,某同学又设计出以下装置,请分别写出两个装置中发生的实验现象:

a装置:
您最近一年使用:0次
名校
解题方法
7 . Na2O2常用作呼吸面具供氧剂。化学兴趣小组设计如下实验装置探究Na2O2与CO2反应的原理(夹持装置略)。查阅资料知:干燥的CO2与Na2O2不反应,湿润的CO2能与Na2O2反应。
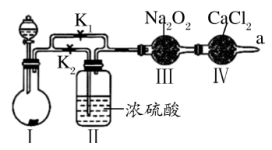
回答下列问题:
(1)实验开始前应先进行的操作是___________ 。
(2)装置Ⅰ中加入试剂的最优方案是___________ (填字母)。
A.稀盐酸 B.稀硫酸 C.小苏打 D.石灰石
装置Ⅰ中发生反应的离子方程式为___________ 。
(3)探究过程如下:
①先打开K2关闭K1进行实验,将带火星的木条置于a处,木条没有复燃。
②然后打开K1,关闭K2进行实验,将带火星的木条置于a处,带火星的木条仍然没有复燃。原因可能是___________ ,若要观察到木条复燃现象,对装置Ⅳ的改进措施为___________ 。
(4)为进一步证明最终CO2与Na2O2发生反应,应继续补充的实验是:取反应后Ⅲ中固体于试管中,___________ 。(可供选择的试剂:稀盐酸、酚酞溶液、紫色石蕊溶液、澄清石灰水)

回答下列问题:
(1)实验开始前应先进行的操作是
(2)装置Ⅰ中加入试剂的最优方案是
A.稀盐酸 B.稀硫酸 C.小苏打 D.石灰石
装置Ⅰ中发生反应的离子方程式为
(3)探究过程如下:
①先打开K2关闭K1进行实验,将带火星的木条置于a处,木条没有复燃。
②然后打开K1,关闭K2进行实验,将带火星的木条置于a处,带火星的木条仍然没有复燃。原因可能是
(4)为进一步证明最终CO2与Na2O2发生反应,应继续补充的实验是:取反应后Ⅲ中固体于试管中,
您最近一年使用:0次
2021-11-17更新
|
273次组卷
|
2卷引用:山东省潍坊(安丘市、诸城市、高密市)2021-2022学年高一上学期期中考试化学试题
8 . 某中学化学兴趣小组按照课本实验方法(如图甲),做木炭与氧化铜反应实验时,发现很难观察到紫红色铜的生成,却往往有暗红色固体出现。他们决定对这个实验进行探究和改进。
【提出问题】暗红色的固体是什么?如何选择合适的条件,使木炭还原氧化铜的实验现象更明显?
【查阅资料】铜有 和
和 两种化合价,通常情况下,氧的化合价为
两种化合价,通常情况下,氧的化合价为 ,碳的化合价为
,碳的化合价为 或
或 。
。
【猜想与假设】

 同学们认为这种暗红色固体可能是一种化合物,并猜测它的化学式为
同学们认为这种暗红色固体可能是一种化合物,并猜测它的化学式为___ 。同学们还认为,通过改变反应物的状态、质量比,以及反应装置,可以使该实验现象更加明显,减少出现暗红色固体的情况。
【分析与交流】
(2)小吴建议用超细炭粉与氧化铜粉末进行实验,你认为这样建议的原理是_______ 。
(3)小周建议用图乙装置替代甲装置。与甲相比较,乙装置中将试管直立放置的作用是__ 。
(4)对下列三种氧化铜和碳的质量比例,小施建议选择__ (填选项序号)的比例。
A.32:3 B. 40:3 C.48:3
你认为小施这样选择的理由是__ 。
【实验与结论】
(5)同学们决定按改进后的方案进行实验,他们在检验了乙装置的___ 后,往试管中加入已干燥的药品并开始加热,当看到澄清的石灰水刚出现浑浊时,___ (填“可以”或“不能”)确定氧化铜和炭粉已经开始反应;不久,即可看到试管底部变红热,停止加热后,仍能看到红热现象,并沿试管底部自下而上蔓延,这个现象说明该反应是___ (填“吸”或“放”)热反应;待反应结束,先将导气管从石灰水中取出,然后关闭止水夹,让产物自然冷却,若不关闭止水夹,可能出现的问题是_ ;待产物冷却后,同学们终于找到了期待已久的紫红色铜珠,实验获得了圆满成功。
【提出问题】暗红色的固体是什么?如何选择合适的条件,使木炭还原氧化铜的实验现象更明显?
【查阅资料】铜有
 和
和 两种化合价,通常情况下,氧的化合价为
两种化合价,通常情况下,氧的化合价为 ,碳的化合价为
,碳的化合价为 或
或 。
。【猜想与假设】

 同学们认为这种暗红色固体可能是一种化合物,并猜测它的化学式为
同学们认为这种暗红色固体可能是一种化合物,并猜测它的化学式为【分析与交流】
(2)小吴建议用超细炭粉与氧化铜粉末进行实验,你认为这样建议的原理是
(3)小周建议用图乙装置替代甲装置。与甲相比较,乙装置中将试管直立放置的作用是
(4)对下列三种氧化铜和碳的质量比例,小施建议选择
A.32:3 B. 40:3 C.48:3
你认为小施这样选择的理由是
【实验与结论】
(5)同学们决定按改进后的方案进行实验,他们在检验了乙装置的
您最近一年使用:0次
2024高三下·全国·专题练习
解题方法
9 . TiCl4是制备Ti的重要中间产物,实验室以TiO2和CCl4为原料制取液态TiCl4的装置如图所示(部分夹持装置省略)。
请回答下列问题:
(1)TiCl4还可由TiO2、焦炭和氯气在加热条件下制得,同时生成CO和CO2混合气体,请设计实验验证产物中CO气体:_______ 。
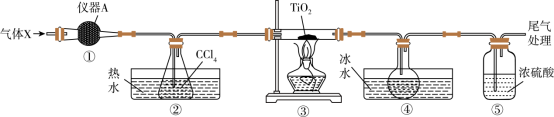
| 物质 | 熔点/℃ | 沸点/℃ | 其他 |
| CCl4 | -23 | 76 | 与TiCl4互溶 |
| TiCl4 | -25 | 136 | 遇潮湿空气产生白雾,在550℃时能被氧气氧化 |
| TiO2 | 1830 | 3200 | 无 |
(1)TiCl4还可由TiO2、焦炭和氯气在加热条件下制得,同时生成CO和CO2混合气体,请设计实验验证产物中CO气体:
您最近一年使用:0次
解题方法
10 . 工业级碳酸锂常含有Na+、K+、Ca2+、 等杂质离子,实验室模拟工业级碳酸锂制备电池级碳酸锂,具体步骤如下:
等杂质离子,实验室模拟工业级碳酸锂制备电池级碳酸锂,具体步骤如下:
某实验小组采用如下装置进行氢化反应。
2.B装置是除杂装置,所用试剂是_____。
3.装置C中发生反应的化学方程式为_____ 。
4.氢化反应选择在常温下进行,温度越高,Li2CO3的转化率越低的原因可能是_____ 。
 等杂质离子,实验室模拟工业级碳酸锂制备电池级碳酸锂,具体步骤如下:
等杂质离子,实验室模拟工业级碳酸锂制备电池级碳酸锂,具体步骤如下:
某实验小组采用如下装置进行氢化反应。
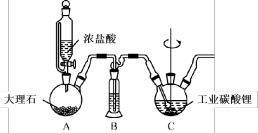
| A.分液漏斗 | B.冷凝管 | C.恒压漏斗 | D.容量瓶 |
| A.饱和食盐水 | B.饱和碳酸氢钠溶液 | C.浓硫酸 | D.四氯化碳 |
4.氢化反应选择在常温下进行,温度越高,Li2CO3的转化率越低的原因可能是
您最近一年使用:0次



