解题方法
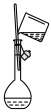
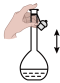
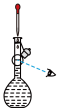
1 . 综合利用粉煤灰既有利于环境保护,又有利于资源节约。某种粉煤灰(主要含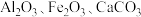 )的铝、铁分离工艺流程如下:
)的铝、铁分离工艺流程如下: 发生反应的离子方程式为
发生反应的离子方程式为_______ 。
②提高浸出率的措施有_______ (写出一点即可)。
③当硫酸浓度大于 时,铝、铁的浸出率下降,可能的原因是
时,铝、铁的浸出率下降,可能的原因是_______ 。
(2)已知:部分氢氧化物开始沉淀和沉淀完全的 如下表所示。
如下表所示。
①“分离”过程中加入氨水调“浸出液” 的范围是
的范围是 ,其目的是
,其目的是_______ 。
②“浸出液”中加铁粉的作用是_______ 。
(3)燃煤烟气中 的捕集可通过如图所示的物质转化实现。
的捕集可通过如图所示的物质转化实现。 溶液与石灰乳反应的化学方程式为
溶液与石灰乳反应的化学方程式为_______ ,载人航天器内,常用 固体而很少用
固体而很少用 固体吸收空气中的
固体吸收空气中的 ,其原因是
,其原因是_______ 。
 )的铝、铁分离工艺流程如下:
)的铝、铁分离工艺流程如下: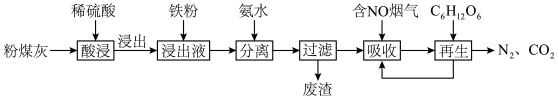
 发生反应的离子方程式为
发生反应的离子方程式为②提高浸出率的措施有
③当硫酸浓度大于
 时,铝、铁的浸出率下降,可能的原因是
时,铝、铁的浸出率下降,可能的原因是(2)已知:部分氢氧化物开始沉淀和沉淀完全的
 如下表所示。
如下表所示。| 氢氧化物 |  |  |  |
| 开始沉淀的pH | 1.5 | 3.2 | 7.1 |
| 沉淀完全的pH | 3.1 | 4.9 | 8.9 |
 的范围是
的范围是 ,其目的是
,其目的是②“浸出液”中加铁粉的作用是
(3)燃煤烟气中
 的捕集可通过如图所示的物质转化实现。
的捕集可通过如图所示的物质转化实现。
 溶液与石灰乳反应的化学方程式为
溶液与石灰乳反应的化学方程式为 固体而很少用
固体而很少用 固体吸收空气中的
固体吸收空气中的 ,其原因是
,其原因是
您最近一年使用:0次
2024高三下·全国·专题练习
解题方法
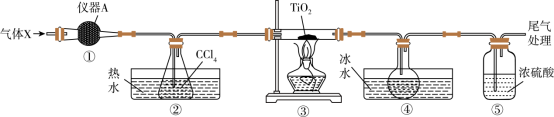
2 . TiCl4是制备Ti的重要中间产物,实验室以TiO2和CCl4为原料制取液态TiCl4的装置如图所示(部分夹持装置省略)。
请回答下列问题:
(1)TiCl4还可由TiO2、焦炭和氯气在加热条件下制得,同时生成CO和CO2混合气体,请设计实验验证产物中CO气体:_______ 。
| 物质 | 熔点/℃ | 沸点/℃ | 其他 |
| CCl4 | -23 | 76 | 与TiCl4互溶 |
| TiCl4 | -25 | 136 | 遇潮湿空气产生白雾,在550℃时能被氧气氧化 |
| TiO2 | 1830 | 3200 | 无 |
(1)TiCl4还可由TiO2、焦炭和氯气在加热条件下制得,同时生成CO和CO2混合气体,请设计实验验证产物中CO气体:
您最近一年使用:0次
解题方法
3 . 工业级碳酸锂常含有Na+、K+、Ca2+、 等杂质离子,实验室模拟工业级碳酸锂制备电池级碳酸锂,具体步骤如下:
等杂质离子,实验室模拟工业级碳酸锂制备电池级碳酸锂,具体步骤如下:
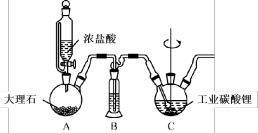
某实验小组采用如下装置进行氢化反应。
2.B装置是除杂装置,所用试剂是_____。
3.装置C中发生反应的化学方程式为_____ 。
4.氢化反应选择在常温下进行,温度越高,Li2CO3的转化率越低的原因可能是_____ 。
 等杂质离子,实验室模拟工业级碳酸锂制备电池级碳酸锂,具体步骤如下:
等杂质离子,实验室模拟工业级碳酸锂制备电池级碳酸锂,具体步骤如下:
某实验小组采用如下装置进行氢化反应。
| A.分液漏斗 | B.冷凝管 | C.恒压漏斗 | D.容量瓶 |
| A.饱和食盐水 | B.饱和碳酸氢钠溶液 | C.浓硫酸 | D.四氯化碳 |
4.氢化反应选择在常温下进行,温度越高,Li2CO3的转化率越低的原因可能是
您最近一年使用:0次
4 . 已知A~G是初中化学常见的七种物质,其中B、C、D含有一种相同的元素,E、F、G含有同一种金属元素,A常用于制玻璃、洗涤剂,B是胃酸的主要成分,C是密度最小的单质,F是常见建筑材料的主要成分,相互间存在如图所示的反应与转化关系“——”表示反应关系,“―→”表示转化关系。请问:
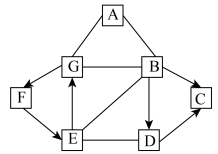
(1)写出物质F的化学式_____ 。
(2)物质D的一种用途是_____ 。
(3)B和E发生的反应,属于_____ 反应。(填基本反应类型)
(4)A与G发生反应的化学方程式为_____ 。

(1)写出物质F的化学式
(2)物质D的一种用途是
(3)B和E发生的反应,属于
(4)A与G发生反应的化学方程式为
您最近一年使用:0次
名校
5 . 物质的量在实验与科研中应用广泛。请回答下列问题:
(1)实验室欲用 的浓硫酸配制
的浓硫酸配制 稀硫酸
稀硫酸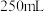 。
。
①下列操作正确的是_____________ (填序号)。
②用量筒量取浓硫酸的体积为_____________  。
。
③配制溶液的过程中,其他操作都正确,下列不当操作对所配溶液浓度的影响:
 用量筒量取浓硫酸时俯视读数:
用量筒量取浓硫酸时俯视读数:_____________ (填“偏大”“偏小”或“无影响”,下同)。
 稀释浓硫酸时,未冷却到室温即转移到容量瓶中:
稀释浓硫酸时,未冷却到室温即转移到容量瓶中:_____________ 。
 将量取浓硫酸后的量筒进行洗涤,并将洗涤液转移到容量瓶中:
将量取浓硫酸后的量筒进行洗涤,并将洗涤液转移到容量瓶中:_____________ 。
(2)室温下测得 的密度为
的密度为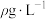 ,则室温下
,则室温下 的气体摩尔体积为
的气体摩尔体积为_________  (用含
(用含 的代数式表示)。
的代数式表示)。
(3)为测定 溶液的浓度,某同学设计了如下实验方案。
溶液的浓度,某同学设计了如下实验方案。
实验原理: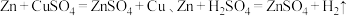 。
。
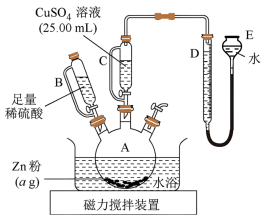
实验步骤:
ⅰ.按图安装装置(夹持仪器略去),并检查装置气密性;
ⅱ.在各仪器中加入图示试剂;
ⅲ.调整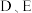 中两液面使其相平,使
中两液面使其相平,使 中液面保持在0或略低于0刻度位置,读数并记录;
中液面保持在0或略低于0刻度位置,读数并记录;
ⅳ.将 液全部滴入A中并搅拌,反应完成后,再滴加稀硫酸至体系不再有气体产生;
液全部滴入A中并搅拌,反应完成后,再滴加稀硫酸至体系不再有气体产生;
ⅴ.待体系恢复到室温,移动 管,保持
管,保持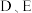 中两液面相平,读数并记录、处理数据。
中两液面相平,读数并记录、处理数据。
①步骤ⅲ需“调整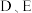 中两液面使其相平”的原因是
中两液面使其相平”的原因是_________________________________ 。
②将实验过程中测得的数据转化为 的质量时,其质量为
的质量时,其质量为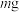 ,则
,则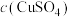 为
为_________________  (列出计算式)。
(列出计算式)。
③有同学认为用同样的装置和方法不能测定 溶液的浓度,其原因为
溶液的浓度,其原因为_________ 。
(1)实验室欲用
 的浓硫酸配制
的浓硫酸配制 稀硫酸
稀硫酸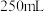 。
。①下列操作正确的是
操作 |
|
|
|
|
选项 |
|
|
|
|
 。
。③配制溶液的过程中,其他操作都正确,下列不当操作对所配溶液浓度的影响:
 用量筒量取浓硫酸时俯视读数:
用量筒量取浓硫酸时俯视读数: 稀释浓硫酸时,未冷却到室温即转移到容量瓶中:
稀释浓硫酸时,未冷却到室温即转移到容量瓶中: 将量取浓硫酸后的量筒进行洗涤,并将洗涤液转移到容量瓶中:
将量取浓硫酸后的量筒进行洗涤,并将洗涤液转移到容量瓶中:(2)室温下测得
 的密度为
的密度为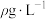 ,则室温下
,则室温下 的气体摩尔体积为
的气体摩尔体积为 (用含
(用含 的代数式表示)。
的代数式表示)。(3)为测定
 溶液的浓度,某同学设计了如下实验方案。
溶液的浓度,某同学设计了如下实验方案。实验原理:
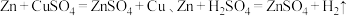 。
。
实验步骤:
ⅰ.按图安装装置(夹持仪器略去),并检查装置气密性;
ⅱ.在各仪器中加入图示试剂;
ⅲ.调整
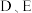 中两液面使其相平,使
中两液面使其相平,使 中液面保持在0或略低于0刻度位置,读数并记录;
中液面保持在0或略低于0刻度位置,读数并记录;ⅳ.将
 液全部滴入A中并搅拌,反应完成后,再滴加稀硫酸至体系不再有气体产生;
液全部滴入A中并搅拌,反应完成后,再滴加稀硫酸至体系不再有气体产生;ⅴ.待体系恢复到室温,移动
 管,保持
管,保持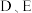 中两液面相平,读数并记录、处理数据。
中两液面相平,读数并记录、处理数据。①步骤ⅲ需“调整
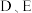 中两液面使其相平”的原因是
中两液面使其相平”的原因是②将实验过程中测得的数据转化为
 的质量时,其质量为
的质量时,其质量为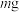 ,则
,则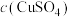 为
为 (列出计算式)。
(列出计算式)。③有同学认为用同样的装置和方法不能测定
 溶液的浓度,其原因为
溶液的浓度,其原因为
您最近一年使用:0次
名校
解题方法
6 . 制造牙膏的常用摩擦剂有①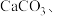 ②
② ③
③ ④
④ 。某实验室设计两种工艺流程制取超细
。某实验室设计两种工艺流程制取超细 ,其原理如图所示。回答下列问题:
,其原理如图所示。回答下列问题:
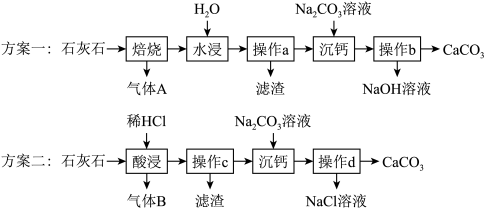
(1)上述摩擦剂属于盐的是_____ (填化学式)。
(2)气体 的化学式为
的化学式为_____ ,操作 的名称为
的名称为_____ 。
(3)方案一“沉钙”时发生反应的离子方程式为_____
(4)方案二“酸浸”时发生反应的化学方程式为_____ ,若生成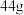 气体
气体 ,则消耗
,则消耗_____ 
 。
。
(5)“操作 ”完成后,洗涤
”完成后,洗涤 的目的是
的目的是_____ 。
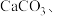 ②
② ③
③ ④
④ 。某实验室设计两种工艺流程制取超细
。某实验室设计两种工艺流程制取超细 ,其原理如图所示。回答下列问题:
,其原理如图所示。回答下列问题:
(1)上述摩擦剂属于盐的是
(2)气体
 的化学式为
的化学式为 的名称为
的名称为(3)方案一“沉钙”时发生反应的离子方程式为
(4)方案二“酸浸”时发生反应的化学方程式为
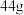 气体
气体 ,则消耗
,则消耗
 。
。(5)“操作
 ”完成后,洗涤
”完成后,洗涤 的目的是
的目的是
您最近一年使用:0次
7 . 运用分类的方法研究物质性质及变化的规律是学习化学的有效途径
I.二氧化硅和碳酸钙是牙膏中常用的摩擦剂。
(1)物质分类。判断二氧化硅和碳酸钙所属的物质类别并填入下表(填“酸”“碱”“盐“酸性氧化物”或“碱性氧化物”)。
(2)性质预测。根据用途可推测二氧化硅________ (填“易溶”或“难溶”)于水。根据二氧化硅所属的物质类别,预测其与CaO在高温下反应的化学方程式:________ 。
(3)物质制备。以石灰石为原料制备摩擦剂碳酸钙的实验方案如下:
方案 1:石灰石 生石灰
生石灰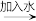 熟石灰
熟石灰 碳酸钙
碳酸钙
方案 2:石灰石 氯化钙
氯化钙 碳酸钙
碳酸钙
①写出方案 2 中石灰石与稀盐酸反应的离子方程式:________ 。
②为了减少碳排放,上述两个方案中,均需回收利用的物质是________ (填化学式);与方案1相比,方案2的优点是________ 。
Ⅱ.可以从不同角度认识化学反应,四种基本反应类型与氧化还原反应的关系如图所示
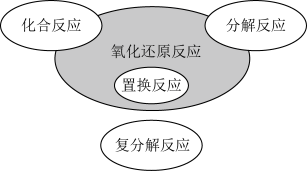
(4)下列化学反应属于阴影区域的是________ (填字母序号)。
a.SO2+H2O2=H2SO4 b.Fe2O3+3CO=2Fe+3CO2
c.2Na2O2+2CO2 = 2Na2CO3+O2 d.Br2+2KI=l2+2KBr
e.2Fe(OH)3=Fe2O3+3H2O
I.二氧化硅和碳酸钙是牙膏中常用的摩擦剂。
(1)物质分类。判断二氧化硅和碳酸钙所属的物质类别并填入下表(填“酸”“碱”“盐“酸性氧化物”或“碱性氧化物”)。
| 摩擦剂 | 二氧化硅 | 磷酸钙 |
| 物质类别 |
(2)性质预测。根据用途可推测二氧化硅
(3)物质制备。以石灰石为原料制备摩擦剂碳酸钙的实验方案如下:
方案 1:石灰石
 生石灰
生石灰 熟石灰
熟石灰 碳酸钙
碳酸钙方案 2:石灰石
 氯化钙
氯化钙 碳酸钙
碳酸钙①写出方案 2 中石灰石与稀盐酸反应的离子方程式:
②为了减少碳排放,上述两个方案中,均需回收利用的物质是
Ⅱ.可以从不同角度认识化学反应,四种基本反应类型与氧化还原反应的关系如图所示

(4)下列化学反应属于阴影区域的是
a.SO2+H2O2=H2SO4 b.Fe2O3+3CO=2Fe+3CO2
c.2Na2O2+2CO2 = 2Na2CO3+O2 d.Br2+2KI=l2+2KBr
e.2Fe(OH)3=Fe2O3+3H2O
您最近一年使用:0次
名校
解题方法
8 . 回答下列问题:
(1)成语“信口雌黄”中的雌黄分子式为As2S3,分子结构如图,As原子的杂化方式为_______ ,雌黄和SnCl2在盐酸中反应转化为雄黄(As4S4)和SnCl4并放出H2S气体,SnCl4的结构与SiCl4相似,其分子的空间结构为_______ 。

(2)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。ZnCO3中,阴离子空间结构为_______ ,C原子的杂化方式为_______ ;明代宋应星所著的《天工开物》中记载了利用C和ZnCO3进行火法炼锌的反应,反应中还生成一种具有还原性的气体,请写出上述的化学方程式:_______ 。
(3)某绿色农药结构简式如图,回答下列问题:

分子中编号为①的碳原子和与其成键的另外几个原子构成的空间结构为_______ ;试比较CO2、H2O、CCl4三种分子的键角_______ (按由大到小顺序排列)。
(1)成语“信口雌黄”中的雌黄分子式为As2S3,分子结构如图,As原子的杂化方式为

(2)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。ZnCO3中,阴离子空间结构为
(3)某绿色农药结构简式如图,回答下列问题:

分子中编号为①的碳原子和与其成键的另外几个原子构成的空间结构为
您最近一年使用:0次
9 . 研究发现百多种植物富含草酸,尤以菠菜、苋菜、甜菜、马齿苋、芋头、甘薯和大黄等植物中含量最高,由于草酸可降低矿质元素的生物利用率,在人体中容易与钙离子形成草酸钙导致肾结石,草酸往往被认为是一种矿质元素吸收利用的拮抗物。
已知:草酸( )是一种弱酸,不稳定,受热或遇浓硫酸会发生分解。
)是一种弱酸,不稳定,受热或遇浓硫酸会发生分解。
(1)草酸的制备:在浓硫酸催化作用下,用硝酸氧化葡萄糖可制取草酸,实验装置如图所示。
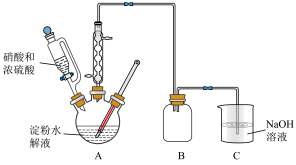
①55~60℃时,装置A中生成 ,同时生成NO。写出该反应的化学方程式:
,同时生成NO。写出该反应的化学方程式:___________ 。
②该实验中催化剂浓硫酸用量不宜过量的原因是___________ 。(答出一点即可)
③装置C的作用是___________ 。
(2)下列事实不能证明草酸是弱电解质的是___________(填字母)。
(3)向10mL
 溶液中加入
溶液中加入 NaOH溶液中含碳微粒的物质的量分数随溶液pH变化如图所示:
NaOH溶液中含碳微粒的物质的量分数随溶液pH变化如图所示:
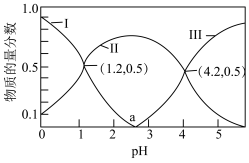
①写出草酸的一级电离方程式:___________ 。
②25℃时,碳酸电离平衡常数分别是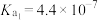 ,
, ,写出少量草酸和过量碳酸钠反应的离子方程式:
,写出少量草酸和过量碳酸钠反应的离子方程式:___________ 。
已知:草酸(
 )是一种弱酸,不稳定,受热或遇浓硫酸会发生分解。
)是一种弱酸,不稳定,受热或遇浓硫酸会发生分解。(1)草酸的制备:在浓硫酸催化作用下,用硝酸氧化葡萄糖可制取草酸,实验装置如图所示。

①55~60℃时,装置A中生成
 ,同时生成NO。写出该反应的化学方程式:
,同时生成NO。写出该反应的化学方程式:②该实验中催化剂浓硫酸用量不宜过量的原因是
③装置C的作用是
(2)下列事实不能证明草酸是弱电解质的是___________(填字母)。
A.草酸能使酸性 溶液褪色 溶液褪色 |
B.常温下,0.1mol/L的 溶液的pH=2 溶液的pH=2 |
C.相同条件下,浓度均为0.1mol/L的 溶液的导电能力比硫酸的导电能力弱 溶液的导电能力比硫酸的导电能力弱 |
D. 溶液中存在 溶液中存在 分子,呈酸性 分子,呈酸性 |

 溶液中加入
溶液中加入 NaOH溶液中含碳微粒的物质的量分数随溶液pH变化如图所示:
NaOH溶液中含碳微粒的物质的量分数随溶液pH变化如图所示:
①写出草酸的一级电离方程式:
②25℃时,碳酸电离平衡常数分别是
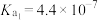 ,
, ,写出少量草酸和过量碳酸钠反应的离子方程式:
,写出少量草酸和过量碳酸钠反应的离子方程式:
您最近一年使用:0次
名校
10 . CO2是一种温室气体。一种吸收空气中的CO2并催化加氢合成CH3OH的流程如下:
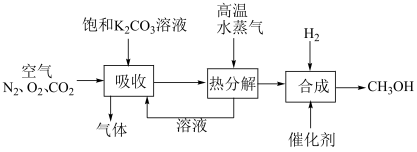
(1)“吸收”步骤反应的化学方程式是___________ 。
(2)“吸收”“热分解”两步的目的是___________ 。
(3)乙酸甲酯(C3H6O2)是合成某些香料的原料,可由甲醇与乙酸在浓硫酸、加热条件下反应得到。生成乙酸甲酯的化学反应方程式是___________ 。

(1)“吸收”步骤反应的化学方程式是
(2)“吸收”“热分解”两步的目的是
(3)乙酸甲酯(C3H6O2)是合成某些香料的原料,可由甲醇与乙酸在浓硫酸、加热条件下反应得到。生成乙酸甲酯的化学反应方程式是
您最近一年使用:0次
2023-07-29更新
|
223次组卷
|
3卷引用:2023年江苏省扬州市普通高中学业水平合格性模拟试卷(二)化学试题