名校
1 . 我国科学家利用高效固体催化剂LDH,实现了在常温常压、可见光下人工固氮,其原理如图所示。下列有关该反应说法不正确的是
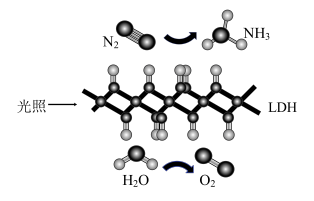

| A.存在极性键、非极性键的断裂与形成 |
| B.反应过程中存在太阳能转化为化学能 |
C.使用LDH,可同时提高反应速率和 的转化率 的转化率 |
D.反应生成1.7g  时转移电子数目为0.3mol 时转移电子数目为0.3mol |
您最近一年使用:0次
2022-03-01更新
|
764次组卷
|
8卷引用:湖北省十堰市郧阳中学、恩施高中、随州二中、襄阳三中2022-2023学年高二下学期5月联考化学试题
湖北省十堰市郧阳中学、恩施高中、随州二中、襄阳三中2022-2023学年高二下学期5月联考化学试题广东省汕头市2022届高三下学期第一次模拟考试化学试题(已下线)专项10 化学反应与能量-备战2022年高考化学阶段性新题精选专项特训(全国卷)(3月期)(已下线)化学-2022年高考押题预测卷02(广东卷)北京市通州区2022届高三查缺补漏化学试题北京市顺义牛栏山第一中学2022届高三下学期保温练习化学试题北京市第十七中学2021-2022学年高三下学期5月模拟考试化学试题(已下线)选择题11-14
2 . 设[aX+bY]为a个X微粒和b个Y微粒组成的一个微粒集合体,NA为阿伏加德罗常数的值。下列说法中不正确的是
| A.500 mL0.5 mol·L-1的NaCl溶液中微粒数大于0.5NA |
B.H2O(g)通过Na2O2(s)使其增重b g时,反应中转移的电子数为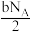 |
| C.合成氨工业中,投料l mol[N2(g)+3H2(g)]可生成NH3(g)的分子数为2NA |
| D.58 g正丁烷和异丁烷的混合物中共价键数目为13NA |
您最近一年使用:0次
2022-02-25更新
|
281次组卷
|
3卷引用:湖北省问津联合体2021-2022学年高一下学期5月质量检测化学试题
3 . 某液体化合物X2Y4常用作火箭燃料。16g X2Y4在一定量的O2中恰好完全燃烧,反应的化学方程式为X2Y4(l)+O2(g)=X2(g)+2Y2O(l)(l表示纯液态)。冷却后标准状况下测得生成物的体积为11.2L,其密度为1.25g·L-1,下列说法不正确的是
| A.反应前O2的体积(标准状况下)为11.2L |
| B.X2的摩尔质量为28g·mol-1 |
| C.氧元素最高化合价与最低化合价的代数和为4 |
| D.若反应生成0.1mol X2,则转移电子的物质的量为0.4mol |
您最近一年使用:0次
2022-02-19更新
|
105次组卷
|
2卷引用:湖北省恩施州高中教育联盟2021-2022学年高一上学期期末考试化学试题
4 . ClO2是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得ClO2:2KClO3+H2C2O4+H2SO4=2ClO2↑+K2SO4+2CO2↑+2H2O。下列说法正确的是
| A.1 mol H2C2O4参加反应有2mol电子转移 | B.ClO2是氧化产物 |
| C.H2C2O4在反应中被还原 | D.KClO3在反应中失去电子 |
您最近一年使用:0次
5 . 每年10月23日上午6:02到晚上6:02被誉为“摩尔日”(Mole Day),这个时间的美式写法为6:02,10/23,外观与阿伏加德罗常数6.02×1023相似。用NA表示阿伏加德罗常数,下列说法正确的是
| A.32g由O2和O3组成的混合气体中含有的原子数为2NA |
| B.1 mol·L-1MgCl2溶液中,Cl-的数目为2NA |
| C.7.8g Na2O2中含有阴离子的数目为0.2NA |
| D.1 mol Cl2与足量Fe反应,转移电子数为3NA |
您最近一年使用:0次
6 . 关于反应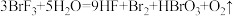 ,下列说法正确的是
,下列说法正确的是
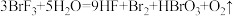 ,下列说法正确的是
,下列说法正确的是| A.氧化剂与还原剂的总物质的量之比为2∶3 |
B.每转移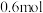 电子,生成 电子,生成 的体积为 的体积为 |
C.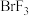 分子中溴原子的化合价为 分子中溴原子的化合价为 价 价 |
D. 和 和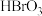 均为氧化产物 均为氧化产物 |
您最近一年使用:0次
2022-01-27更新
|
126次组卷
|
2卷引用:湖北省十堰市2021-2022学年高二上学期元月期末调研考试化学试题
名校
7 . 下列相关说法正确的是
| 化学反应方程式 | 相关说法 | |
| A | 2KClO3 2KCl +3O2↑ 2KCl +3O2↑ | 双线桥: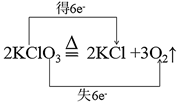 |
| B | 2Fe3+ +Cu=2Fe2+ + Cu2+ | 氧化性: Cu > Fe2+ |
| C | 4CuO 2Cu2O+O2↑ 2Cu2O+O2↑ | 每生成1 mol O2,转移2NA个电子 |
| D | ________ClO-+________Fe3+ + _______OH-=________FeO +______Cl- +_____ H2O +______Cl- +_____ H2O | 化学计量数依次为:3,2,10,2,3,5 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-01-19更新
|
313次组卷
|
4卷引用:湖北省2021-2022学年高一上学期期末调考化学试题
名校
8 . 关于下列氧化还原反应说法正确的是
| A.对于11PH3+24CuSO4+12H2O=3H3PO4+24H2SO4+8Cu3P↓反应中每24molCuSO4氧化11molPH3 |
B.在淀粉和 的混合溶液中滴加 的混合溶液中滴加 溶液。[已知: 溶液。[已知: 、 、 分别与卤素单质、卤素离子性质相似],溶液仍为蓝色,证明氧化性: 分别与卤素单质、卤素离子性质相似],溶液仍为蓝色,证明氧化性: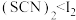 |
| C.K2H3IO6+9HI=2KI+4I2+6H2O,还原剂与氧化剂的物质的量之比为7:1 |
D. ,产生22.4L(标准状况) ,产生22.4L(标准状况) 时,反应中转移 时,反应中转移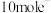 |
您最近一年使用:0次
2022-01-13更新
|
1110次组卷
|
4卷引用:湖北省武汉市汉阳、江夏2021-2022学年高一上学期12月联考化学试题
9 . 关于下列三个反应说法正确的是
①Cl2+2KBr=2KCl+Br2;②KClO3+6HCl=3Cl2↑+KCl+3H2O;③2KBrO3+Cl2=Br2+2KClO3
①Cl2+2KBr=2KCl+Br2;②KClO3+6HCl=3Cl2↑+KCl+3H2O;③2KBrO3+Cl2=Br2+2KClO3
| A.上述三个反应都有单质生成,所以都是置换反应 |
| B.反应②中还原剂与氧化剂的个数之比为5∶1 |
| C.氧化性由强到弱顺序为KClO3>KBrO3>Cl2>Br2 |
| D.③中1个氧化剂反应则失去电子为10个 |
您最近一年使用:0次
2022-01-10更新
|
148次组卷
|
3卷引用:湖北省荆门市龙泉中学2021-2022学年高一上学期11月月考(实验班)化学试题
名校
10 . 捕获二氧化碳是碳中和技术之一,如图是捕获二氧化碳生成甲酸的过程,N(C2H5)3性质与NH3类似。若NA为阿伏加德罗常数的值,下列说法正确的是


| A.若有22.4LCO2参与反应,则拆开CO2分子中共用电子对的数目为4NA |
| B.0.1molN(C2H5)3与盐酸恰好完全反应所得盐溶液中[N(C2H5)3H]+的数目为0.1NA |
| C.每生成1mol甲酸,该捕获过程中转移的电子数为2NA |
| D.1mol甲酸和足量乙醇充分反应后,生成甲酸乙酯的数目为NA |
您最近一年使用:0次
2022-01-03更新
|
1017次组卷
|
6卷引用:湖北省蕲春县第一高级中学2022届高三5月第三次模拟考试化学试题
湖北省蕲春县第一高级中学2022届高三5月第三次模拟考试化学试题云南省2021-2022学年高三上学期“3+3+3”高考备考诊断性联考(一)理科综合化学试题湖南省长沙市雅礼中学2021-2022学年高三下学期月考(七)化学试题(已下线)专题07化学反应中的能量变化及反应机理-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题07化学反应中的能量变化及反应机理-五年(2018~2022)高考真题汇编(全国卷)宁夏石嘴山市2023届高三适应性测试理科综合化学试题



