名校
解题方法
1 . LiBH4是有机合成中常用的试剂,与水反应:LiBH4+2H2O=LiBO2+4H2↑(LiBH4中B为+ 3价),下列说法中正确的是
| A.LiBH4被氧化,LiBO2是氧化产物 |
| B.生成lmolH2,反应转移2mol电子 |
| C.LiBH4与D2O反应,生成的气体相对分子质量为3 |
| D.与LiBH4中Li、H化合价相同的两种离子的半径Li>H |
您最近一年使用:0次
2017-10-10更新
|
405次组卷
|
2卷引用:湖北省黄冈市2018届高三9月质量检测化学试题
10-11高三上·湖北·期中
名校
2 . 一定条件下用甲烷可以消除氮氧化物(NOx)的污染。已知:
①CH4(g)+4NO2(g)==4NO(g)+CO2(g)+2H2O(g);ΔH=-574 kJ·mol-1
②CH4(g)+4NO(g)==2N2(g)+CO2(g)+2H2O(g);ΔH=-1160 kJ·mol-1
下列正确的选项是
①CH4(g)+4NO2(g)==4NO(g)+CO2(g)+2H2O(g);ΔH=-574 kJ·mol-1
②CH4(g)+4NO(g)==2N2(g)+CO2(g)+2H2O(g);ΔH=-1160 kJ·mol-1
下列正确的选项是
| A.CH4(g)+2NO2(g)==N2(g)+CO2(g)+2H2O(l);ΔH=-867 kJ·mol-1 |
| B.CH4催化还原NOx为N2的过程中,若x=1.6,则转移的电子总数为3.2 mol |
| C.若0.2 mol CH4还原NO2至N2,在上述条件下放出的热量为173.4 kJ |
| D.若用标准状况下4.48 L CH4还原NO2至N2,整个过程中转移的电子总数为3.2 mol. |
您最近一年使用:0次
2016-12-09更新
|
843次组卷
|
8卷引用:2010年湖北襄樊四校高三上学期期中联考化学卷
(已下线)2010年湖北襄樊四校高三上学期期中联考化学卷2016-2017学年湖北省咸宁市高二上学期第一次月考化学试卷2015-2016学年山东省武城县第二中学高二上学期第一次月考化学试卷山东省滕州市第一中学2020-2021学年高二一部9月小测试化学试题安徽省怀宁中学2020-2021学年高一下学期第一次月考化学试题江西省景德镇一中2020-2021学年高一下学期期中考试化学(1班)试题(已下线)期中考试模拟试题(二)-2023-2024学年高二化学期中考点大串讲(人教版2019选择性必修1)新疆克孜勒苏柯尔克孜自治州第一中学2022-2023学年高一上学期11月期中考试化学试题
3 . 如图所示,两圆圈相交的部分表示圆圈内的物质相互发生的反应。已知钠及其氧化物的物质的量均为0.1 mol,水的质量为100 g。下列说法正确的是( )
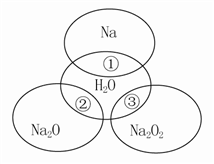

| A.Na2O2中阴阳离子数目之比为1∶1 |
| B.反应①的离子方程式为Na+2H2O===Na++2OH-+H2↑ |
| C.①、②、③充分反应后所得溶液中溶质的质量分数:①>②>③ |
| D.反应③转移电子的物质的量为0.1mol |
您最近一年使用:0次
2016-12-09更新
|
2087次组卷
|
12卷引用:2014-2015学年湖北省襄阳五中高一12月月考化学试卷
2014-2015学年湖北省襄阳五中高一12月月考化学试卷黑龙江省哈尔滨市第六中学2017-2018学年高一12月月考化学试题黑龙江省哈尔滨六中2017-2018学年高一12月月考化学试卷【全国百强校】黑龙江省哈尔滨市第三中学校2018-2019学年高一上学期第二次月考化学试题【全国百强校】黑龙江省大庆实验中学2018-2019学年高一上学期期末考试化学试题苏教版(2020)高一必修第一册专题3 总结检测人教版(2019)高一必修第一册 第二章素养检测人教版(2019)高一必修第一册 第二章 海水中的重要元素 第二章 章末综合检测卷(已下线)第三章 金属及其化合物(能力提升)-2020-2021学年高一化学单元测试定心卷(人教版必修1)高一必修第一册(苏教2019)专题3 专题综合检测卷(已下线)易错专题10 Na2O和Na2O2的性质与比较-【突破易错·冲刺满分】2021-2022学年高一上学期化学期中期末易错专题(人教版2019)重庆市万州第二高级中学2022-2023学年高一上学期12月线上考试化学试题
10-11高二上·湖南长沙·期中
名校
4 . 有Fe2+、 、Fe3+、
、Fe3+、 、H+和H2O六种粒子,属于同一氧化还原反应中的反应物和生成物,下列叙述不正确的是
、H+和H2O六种粒子,属于同一氧化还原反应中的反应物和生成物,下列叙述不正确的是
 、Fe3+、
、Fe3+、 、H+和H2O六种粒子,属于同一氧化还原反应中的反应物和生成物,下列叙述不正确的是
、H+和H2O六种粒子,属于同一氧化还原反应中的反应物和生成物,下列叙述不正确的是| A.氧化剂和还原剂的物质的量之比为1:8 |
| B.该过程说明Fe(NO3)2溶液不宜加酸酸化 |
C.若有1mol 发生还原反应,则转移8mol e- 发生还原反应,则转移8mol e- |
| D.若把该反应设计为原电池,则正极反应为Fe2+-e-=Fe3+ |
您最近一年使用:0次
2016-12-09更新
|
296次组卷
|
11卷引用:2015届湖北省四校高三上学期期中联考化学试卷
(已下线)2015届湖北省四校高三上学期期中联考化学试卷(已下线)2010年湖南省浏阳一中高二上学期期中考试化学试题(已下线)2014届浙江省浙北名校联盟高三上学期期中联考化学试卷(已下线)2014高考名师推荐化学氧化还原反应方程式的配平及相关计算2014-2015山西省忻州市第一中学高一下学期期中考试化学试卷2016届湖南省石门县一中高三第一次月考化学试卷2016届湖南省常德市石门一中高三上学期10月月考化学试卷2017届黑龙江大庆一中高三上第二次月考化学试卷湖南省师范大学附属中学2018届高三上学期10月月考试卷(二)化学试题(已下线)考点05 氧化还原反应-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)考点05 氧化还原反应(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
名校
解题方法
5 . Mg、Al两种金属分别跟相同体积、相同浓度的稀H2SO4反应,同温同压下生成氢气的体积相同,则Mg、Al两种金属之间的量的关系一定正确的是
| A.两个反应转移的电子数目相等 |
| B.加入镁、铝的质量比为4:3 |
| C.金属溶解的物质的量相等 |
| D.加入的两种金属的质量不等 |
您最近一年使用:0次
2016-12-09更新
|
1072次组卷
|
5卷引用:湖北省华中师范大学第一附属中学2016-2017学年高一下学期期中考试(文)化学试题
湖北省华中师范大学第一附属中学2016-2017学年高一下学期期中考试(文)化学试题【全国百强校】湖北省孝感市高级中学2018-2019学年高一上学期期中考试化学试题(已下线)2013-2014学年重庆市重庆一中高一上学期期中考试化学试卷2015-2016学年黑龙江省哈尔滨六中高一上期末化学试卷(已下线)练习10 镁及其化合物-2020-2021学年【补习教材·寒假作业】高一化学(苏教版)
12-13高三上·湖北孝感·阶段练习
6 . 把图2中的物质补充到图1中,可得到一个完整的氧化还原反应离子方程式(未配平)。对该氧化还原反应离子方程式的说法不正确的是


A.IO 作氧化剂 作氧化剂 |
| B.氧化剂和还原剂的物质的量之比为5∶2 |
| C.若有2mol Mn2+参加反应,则转移10 mol电子 |
| D.配平后Mn2+、H+的化学计量数分别为2、3 |
您最近一年使用:0次
11-12高一上·湖北黄冈·期中
7 . 氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:NO3+4H++3e-===NO+2H2O。
KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
(1)配平上述总反应方程式并标出电子转移的方向和总数__________________
(2)反应中硝酸体现了________ 、________ 性质。
(3)反应中若产生了0.2 mol气体,则转移电子的物质的量是________ mol。
(4)被1mol Cu2S中+1价亚铜离子还原的HNO3的物质的量是____ mol
KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
(1)配平上述总反应方程式并标出电子转移的方向和总数
(2)反应中硝酸体现了
(3)反应中若产生了0.2 mol气体,则转移电子的物质的量是
(4)被1mol Cu2S中+1价亚铜离子还原的HNO3的物质的量是
您最近一年使用:0次



