1 . 某小组实验探究不同条件下 溶液与
溶液与 溶液的反应。
溶液的反应。
已知:
i. 在一定条件下可被还原为:
在一定条件下可被还原为: (绿色)、
(绿色)、 (无色)、
(无色)、 (棕黑色)。
(棕黑色)。
ii. 在中性、酸性溶液中不稳定,易发生歧化反应,产生棕黑色沉淀,溶液变为紫色。
在中性、酸性溶液中不稳定,易发生歧化反应,产生棕黑色沉淀,溶液变为紫色。
(1)实验I~III的操作过程中,加⼊ 溶液和物质a时,应先加
溶液和物质a时,应先加___________ 。
(2)实验I中, 的还原产物为
的还原产物为___________ 。
(3)实验II中发生反应的离子方程式为___________ 。
(4)已知:可从电极反应⻆度分析物质氧化性和还原性的变化。用电极反应式表示实验III中溶液变绿时发⽣的氧化反应___________ 。
(5)解释实验III中“⼀段时间后绿色消失,产生棕黑色沉淀”的原因___________ 。
(6)若想观察 溶液与
溶液与 溶液反应后溶液为持续稳定的绿色,设计实验方案
溶液反应后溶液为持续稳定的绿色,设计实验方案___________ 。
(7)改用0.1
 溶液重复实验I,发现紫色溶液变浅并产生棕黑沉淀,写出产生棕黑色沉淀的离子方程式
溶液重复实验I,发现紫色溶液变浅并产生棕黑沉淀,写出产生棕黑色沉淀的离子方程式___________ 。
 溶液与
溶液与 溶液的反应。
溶液的反应。已知:
i.
 在一定条件下可被还原为:
在一定条件下可被还原为: (绿色)、
(绿色)、 (无色)、
(无色)、 (棕黑色)。
(棕黑色)。ii.
 在中性、酸性溶液中不稳定,易发生歧化反应,产生棕黑色沉淀,溶液变为紫色。
在中性、酸性溶液中不稳定,易发生歧化反应,产生棕黑色沉淀,溶液变为紫色。| 实验 | 序号 | 物质a | 实验现象 |
| 4滴物质a 6滴(约0.3mL)0.1   溶液 溶液
  溶液 溶液 | I | 3  溶液 溶液 | 紫色溶液变浅至几乎无色 |
| II |  | 紫色褪去,产生棕黑色沉淀 | |
| III | 6 NaOH溶液 NaOH溶液 | 溶液变绿,⼀段时间后绿色消失,产生棕黑色沉淀 |
 溶液和物质a时,应先加
溶液和物质a时,应先加(2)实验I中,
 的还原产物为
的还原产物为(3)实验II中发生反应的离子方程式为
(4)已知:可从电极反应⻆度分析物质氧化性和还原性的变化。用电极反应式表示实验III中溶液变绿时发⽣的氧化反应
(5)解释实验III中“⼀段时间后绿色消失,产生棕黑色沉淀”的原因
(6)若想观察
 溶液与
溶液与 溶液反应后溶液为持续稳定的绿色,设计实验方案
溶液反应后溶液为持续稳定的绿色,设计实验方案(7)改用0.1

 溶液重复实验I,发现紫色溶液变浅并产生棕黑沉淀,写出产生棕黑色沉淀的离子方程式
溶液重复实验I,发现紫色溶液变浅并产生棕黑沉淀,写出产生棕黑色沉淀的离子方程式
您最近一年使用:0次
2023-03-24更新
|
498次组卷
|
3卷引用:专题21 实验探究题
2023高三·全国·专题练习
解题方法
2 . 完成下列实验设计题:
(1)证明CO2中含有CO___________
(2)证明SO2中含有CO2___________
(3)证明SO 中含有SO
中含有SO
___________
(4)①证明H2C2O4是弱酸;②证明草酸的酸性强于碳酸;③证明草酸是二元酸___________ (提供的试剂:0.1 mol·L-1 NaHCO3溶液、0.1 mol·L-1草酸溶液、0.1 mol·L-1 NaOH溶液、Na2C2O4晶体、甲基橙、酚酞、pH试纸)
(5)设计一个实验方案证明酸性条件下NaNO2具有氧化性___________ (提供的试剂:0.10 mol·L-1 NaNO2溶液、KMnO4溶液、0.10 mol·L-1 KI溶液、淀粉溶液、稀硝酸、稀硫酸)
(1)证明CO2中含有CO
(2)证明SO2中含有CO2
(3)证明SO
 中含有SO
中含有SO
(4)①证明H2C2O4是弱酸;②证明草酸的酸性强于碳酸;③证明草酸是二元酸
(5)设计一个实验方案证明酸性条件下NaNO2具有氧化性
您最近一年使用:0次
3 . 根据下列实验操作和现象所得到的结论错误的是( )
| 选项 | 实验操作和现象 | 实验结论 |
| A | 向2mL0.1FeCl3的溶液中加足量铁粉,振荡,加1滴KSCN溶液,黄色逐渐消失,加KSCN溶液颜色不变 | 还原性:Fe>Fe2+ |
| B | 向久置的Na2SO3溶液中加入足量BaCl2溶液,出现白色沉淀;再加入足量稀盐酸,部分沉淀溶解 | 部分Na2SO3被氧化 |
| C | 向含I-的无色溶液中滴加少量新制氯水,再滴加淀粉溶液加入淀粉后溶液变成蓝色 | 氧化性:Cl2>I2 |
| D | 向某黄色溶液中加入淀粉KI溶液,溶液呈蓝色 | 溶液中含Br2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-07-03更新
|
275次组卷
|
3卷引用:第二单元 化学物质的变化测试题-2021年高考化学一轮复习名师精讲练
(已下线)第二单元 化学物质的变化测试题-2021年高考化学一轮复习名师精讲练黑龙江省哈尔滨市第三中学2019-2020学年高二下学期6月阶段性测试化学试题A山东省临沂市莒南第二中学2021届高三10月月考化学试题
4 . 某小组进行如下实验:向0.1mol·L-1 FeCl3溶液中通入SO2或加入Na2SO3溶液,均得到红色溶液。
已知:溶液中+4价含硫微粒物质的量分数随pH变化的曲线如下图所示。
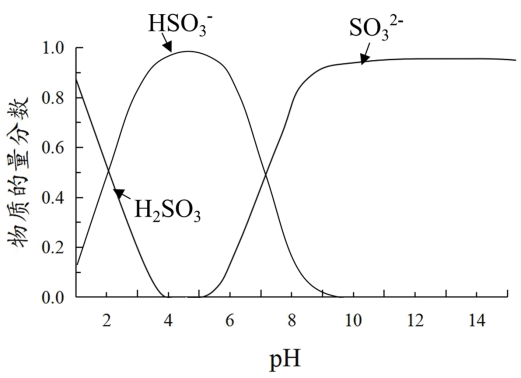
I.推测Fe3+与溶液中的某种+4价含硫微粒形成了红色的配离子。设计如下实验(均在常温下进行):
(1)将上述实验补充完整________ 。
(2)配离子的配体为 的实验证据是
的实验证据是_______ 。
II.探究pH对FeCl3和Na2SO3反应的影响。设计如下实验:
(3)探究实验b中溶液褪色更快的原因:
i.甲认为pH降低,有利于Fe3+氧化 ,导致实验b中溶液褪色更快。
,导致实验b中溶液褪色更快。
①从电极反应的角度,进行理论分析:
还原反应为:Fe3++e-=Fe2+氧化反应为:_______ 。
②已知上述实验条件下pH对Fe3+的氧化性几乎没有影响。从平衡移动的角度判断pH对 还原性的影响是
还原性的影响是_______ (填“增强”或“减弱”)。
③通过理论分析,甲认为其猜测_______ (填“成立”或“不成立”),并进一步实验,获得了证据。实验方案为:反应相同时间,分别取实验a和b中的溶液,检测_______ 浓度(填离子符号),比较其大小关系。
ii.乙猜测pH降低,有利于_______氧化 ,导致实验b中溶液褪色更快。
,导致实验b中溶液褪色更快。
④将乙的假设补充完整_______ (填化学式)。
⑤乙设计实验进行验证:
取10mL 0.1mol·L-1 Na2SO3溶液加硫酸调pH=1.7,用KMnO4溶液滴定,消耗体积为V1。另取一份相同的溶液放置10分钟后,再用KMnO4溶液滴定,消耗体积为V2.前后差值(V1-V2)为ΔVa。用同样的方法对10mL 0.1mol·L-1 Na2SO3(含H2SO4)pH=1.3进行滴定,消耗KMnO4溶液前后体积差值为ΔVb。
经对比可知,ΔVa>△Vb,由此得出的实验结论是_______ 。
(4)综合上述分析,pH降低,有利于_______ 反应的发生,导致实验b中溶液褪色更快。
已知:溶液中+4价含硫微粒物质的量分数随pH变化的曲线如下图所示。

I.推测Fe3+与溶液中的某种+4价含硫微粒形成了红色的配离子。设计如下实验(均在常温下进行):
| 实验 | 溶液1(1mL) | 溶液2(10mL) | 现象 |
| A | 0.1mol·L-1 FeCl3溶液 | SO2的饱和溶液 | 溶液1与溶液2混合后,实验A、B、C所得溶液红色依次加深 |
| B | 0.1mol·L-1 FeCl3溶液 | SO2的饱和溶液,用NaOH固体调 pH=5.0 | |
| C | 0.1mol·L-1 FeCl3溶液 | _______ |
(2)配离子的配体为
 的实验证据是
的实验证据是II.探究pH对FeCl3和Na2SO3反应的影响。设计如下实验:
| 序号 | 实验a | 实验b |
| 方案 | 5mL酸化的0.1mol·L-1 FeCl3与2mL 0.1mol·L-1 Na2SO3混合得红色溶液,测得pH=1.7 | 5mL酸化的0.1mol·L-1 FeCl3与2mL 0.1mol·L-1 Na2SO3混合得红色溶液,加几滴浓盐酸,调pH=1.3 |
| 现象 | 放置10分钟后,溶液红色均褪去,实验b中溶液褪色更快。经检验,褪色后的溶液中均存在Fe2+。 | |
i.甲认为pH降低,有利于Fe3+氧化
 ,导致实验b中溶液褪色更快。
,导致实验b中溶液褪色更快。①从电极反应的角度,进行理论分析:
还原反应为:Fe3++e-=Fe2+氧化反应为:
②已知上述实验条件下pH对Fe3+的氧化性几乎没有影响。从平衡移动的角度判断pH对
 还原性的影响是
还原性的影响是③通过理论分析,甲认为其猜测
ii.乙猜测pH降低,有利于_______氧化
 ,导致实验b中溶液褪色更快。
,导致实验b中溶液褪色更快。④将乙的假设补充完整
⑤乙设计实验进行验证:
取10mL 0.1mol·L-1 Na2SO3溶液加硫酸调pH=1.7,用KMnO4溶液滴定,消耗体积为V1。另取一份相同的溶液放置10分钟后,再用KMnO4溶液滴定,消耗体积为V2.前后差值(V1-V2)为ΔVa。用同样的方法对10mL 0.1mol·L-1 Na2SO3(含H2SO4)pH=1.3进行滴定,消耗KMnO4溶液前后体积差值为ΔVb。
经对比可知,ΔVa>△Vb,由此得出的实验结论是
(4)综合上述分析,pH降低,有利于
您最近一年使用:0次
2022-04-29更新
|
1807次组卷
|
6卷引用:专项14 化学实验综合题-备战2022年高考化学阶段性新题精选专项特训(全国卷)(5月期)
(已下线)专项14 化学实验综合题-备战2022年高考化学阶段性新题精选专项特训(全国卷)(5月期)天天练6-10北京市丰台区2022届高三二模化学试题(已下线)化学-2022年高考押题预测卷03(北京卷)北京市顺义区第一中学2022届高三下学期三模化学试题湖北省华中师范大学第一附属中学2022-2023学年高一上学期竞赛生10月测试化学试题
名校
解题方法
5 . 连二亚硫酸钠(Na2S2O4)俗称保险粉,有强还原性,在空气中极易被氧化。用NaHSO3还原法制备保险粉的流程如下:
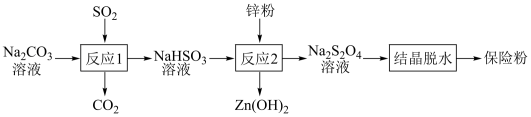
下列说法错误的是

下列说法错误的是
| A.反应1说明酸性:H2SO3>H2CO3 |
| B.反应2中消耗的氧化剂和还原剂的物质的量之比为1∶2 |
| C.反应2最好在无氧条件下进行 |
| D.反应1结束后,可用盐酸酸化的BaCl2溶液检验NaHSO3是否被氧化 |
您最近一年使用:0次
2021-11-04更新
|
803次组卷
|
5卷引用:专题40 硫的含氧酸盐-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)
(已下线)专题40 硫的含氧酸盐-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)江西省奉新县第一中学2021-2022学年上学期高三第一次月考化学试题(已下线)3.2.2 硫酸 不同价态硫元素间的转化-2021-2022学年高一化学课后培优练(鲁科版2019必修第一册)陕西省安康市2022-2023学年高二上学期11月期中化学试题陕西省安康市2022-2023学年高二下学期开学摸底考试化学试题
解题方法
6 . 室温下,下列实验方案能得出相应结论的是
| 选项 | 方案 | 结论 |
| A | 将灼热的木炭加入到浓硝酸中,有红棕色气体产生 | 木炭在加热条件下能与浓硝酸反应 |
| B | 用pH计分别测定0.1 mol·L-1NaClO溶液和0.1mol·L-1CH3COONa溶液的pH,前者pH大于后者 | HClO酸性强于CH3COOH |
| C | 向Fe(NO3)2和KSCN的混合溶液中滴入酸化的AgNO3溶液振荡,溶液颜色变红 | 氧化性: Ag+>Fe3+ |
| D | 向Na2SO3溶液中滴入酚酞试液,溶液变红,再加入BaCl2溶液后产生白色沉淀且红色褪去 | Na2SO3溶液中存在水解平衡 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7 . 已知NH4CuSO3与足量的1mol/L硫酸溶液混合微热,产生下列现象:①有红色金属生成;②有刺激性气味气体产生;③溶液呈蓝色。据此判断下列说法合理的是
| A.NH4CuSO3中硫元素被还原 |
| B.刺激性气味的气体是二氧化硫或氨气 |
| C.该反应中硫酸既体现了酸性又体现了氧化性 |
| D.反应中每消耗1molNH4CuSO3,转移的电子数约为3.01×1023 |
您最近一年使用:0次
8 . 下列由实验现象所得结论错误的是
A.向NaHSO3溶液中滴加氢硫酸,产生淡黄色沉淀,证明HSO 具有氧化性 具有氧化性 |
| B.向酸性KMnO4溶液中加入Fe3O4粉末,紫色褪去,证明Fe3O4中含Fe(Ⅱ) |
| C.向浓HNO3中插入红热的炭,产生红棕色气体,证明炭可与浓HNO3反应生成NO2 |
| D.向NaClO溶液中滴加酚酞试剂,先变红后褪色,证明NaClO在溶液中发生了水解反应 |
您最近一年使用:0次
2021-06-29更新
|
9774次组卷
|
21卷引用:课时23 氮及其化合物-2022年高考化学一轮复习小题多维练(全国通用)
(已下线)课时23 氮及其化合物-2022年高考化学一轮复习小题多维练(全国通用)(已下线)专题05 元素及其化合物-备战2022年高考化学真题及地市好题专项集训【山东专用】(已下线)专题07 非金属及其化合物-2022年高考化学二轮复习重点专题常考点突破练(已下线)解密07 非金属及其化合物(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)解密07 非金属及其化合物(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)秘籍05 微型实验方案设计与评价-备战2022年高考化学抢分秘籍(全国通用)(已下线)押新高考卷05题 化学实验基础-备战2022年高考化学临考题号押题(新高考通版)(已下线)专题24 实验分析设计型选择题-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)题型182 综合实验突破(已下线)专题07 无机物的转化 微型工艺流程-2023年高考化学真题题源解密(全国通用)2021年新高考山东化学高考真题山东省临沂市兰山区2020-2021学年高一下学期期末考试化学试题吉林省松原市实验高级中学2020-2021学年高一下学期期末考试化学试题内蒙古北京八中乌兰察布分校2021-2022学年高三上学期学科素养评估一化学试题2021年山东高考化学试题变式题1-10天津市第一中学2021-2022学年高三下学期4月月考化学试题山东省威海乳山市银滩高级中学2022-2023学年高三9月月考化学试题新疆乌鲁木齐市第八中学2022-2023学年高三上学期第一次月考化学试题河北省石家庄市第十五中学2022-2023学年高三上学期阶段性考试化学试题山东省济宁市邹城市孟子湖中学2021-2022学年高三下学期开学考试化学试题河北省唐山市第一中学2022-2023学年高三上学期11月期中考试化学试题
9 . 亚硫酸钠(Na2SO3)是印染工业中常用的脱氧剂和漂白剂。回答下列问题:
(1)实验室用H2SO4和NaHSO3制取SO2的化学方程式为:___________
(2)SO2可以与H2S反应,请写出其化学方程式:___________ 。
(3)亚硫酸钠易被氧化而变质为Na2SO4,选用下列试剂设计实验方案,检验亚硫酸钠样品氧化变质的程度。仅供选择的试剂:稀盐酸、稀H2SO4、稀HNO3、BaCl2溶液、酸性KMnO4溶液、H2O2溶液
(4)(Ga)与A1同主族,化学性质相似,是制造半导体材料氮化镓的重要原料,其中电解NaGaO2是获得Ga单质的重要方法,如图所示,则阴极的电极反应为:___________ 。若电解获得1molGa,则阳极产生的气体在标准状况下的体积至少为 ___________ L。

(1)实验室用H2SO4和NaHSO3制取SO2的化学方程式为:
(2)SO2可以与H2S反应,请写出其化学方程式:
(3)亚硫酸钠易被氧化而变质为Na2SO4,选用下列试剂设计实验方案,检验亚硫酸钠样品氧化变质的程度。仅供选择的试剂:稀盐酸、稀H2SO4、稀HNO3、BaCl2溶液、酸性KMnO4溶液、H2O2溶液
| 实验编号 | 实验步骤 | 现象 | 结论 |
| I | 取少量样品,加入除氧蒸馏水 | 固体完全溶解,得到无色溶液 | / |
| II | 取实验I的溶液, | 样品存在氧化变质 | |
| III | 另取实验I的溶液, | 样品并未完全氧化变质 |

您最近一年使用:0次
10 . 某研究性学习小组查阅资料得知,漂白粉与硫酸溶液反应可制取氯气,化学方程式为 ,他们设计如图实验装置制取氯气并验证其性质。请回答下列问题:
,他们设计如图实验装置制取氯气并验证其性质。请回答下列问题:
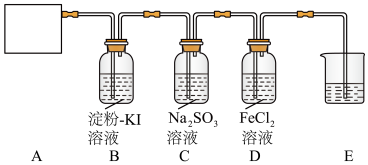
(1)该实验中A部分的装置是_______ (填字母)。
a.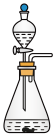 b.
b. 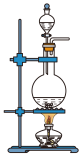 c.
c. 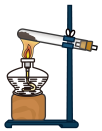 d.
d. 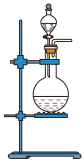
(2)装置B中的现象是_______ 。
(3)请写出装置D中发生反应的离子方程式:_______ ,装置E的作用是_______ 。
(4)请帮助他们设计一个实验,证明洗气瓶C中的亚硫酸钠已被氧化(简述实验步骤):_______ 。
(5)制取 的方法有多种,若A部分的装置是a,请再写出一种制备方法:
的方法有多种,若A部分的装置是a,请再写出一种制备方法:_______ (用化学方程式表示)。
 ,他们设计如图实验装置制取氯气并验证其性质。请回答下列问题:
,他们设计如图实验装置制取氯气并验证其性质。请回答下列问题:
(1)该实验中A部分的装置是
a.
 b.
b.  c.
c.  d.
d. 
(2)装置B中的现象是
(3)请写出装置D中发生反应的离子方程式:
(4)请帮助他们设计一个实验,证明洗气瓶C中的亚硫酸钠已被氧化(简述实验步骤):
(5)制取
 的方法有多种,若A部分的装置是a,请再写出一种制备方法:
的方法有多种,若A部分的装置是a,请再写出一种制备方法:
您最近一年使用:0次