名校
解题方法
1 . 钠碱法的启动吸收剂为 溶液,捕捉
溶液,捕捉 后生成
后生成 和
和 的混合液。
的混合液。
(1)工业上先用 溶液吸收
溶液吸收 ,再用
,再用 使
使 再生:NaOH溶液
再生:NaOH溶液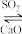 Na2SO3。使
Na2SO3。使 再生的原理是
再生的原理是___________ 。(用化学方程式表示)
(2)常温下进行“钠碱法”的模拟实验。用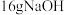 固体配成一定浓度的溶液,这些
固体配成一定浓度的溶液,这些 理论上最多可吸收
理论上最多可吸收 的体积约为
的体积约为___________  (折算成标准状况)。若实验时只吸收了
(折算成标准状况)。若实验时只吸收了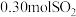 ,则反应后的吸收液中,溶质的组成为:
,则反应后的吸收液中,溶质的组成为:___________ 。(写出溶质组成和每种溶质的物质的量)
(3)若用碱液吸收工业尾气中的 后,得到等物质的量浓度的
后,得到等物质的量浓度的 和
和 溶液。继续向溶液中滴入几滴
溶液。继续向溶液中滴入几滴 溶液变浑浊,请写出发生反应的离子方程式
溶液变浑浊,请写出发生反应的离子方程式___________ 。
 溶液,捕捉
溶液,捕捉 后生成
后生成 和
和 的混合液。
的混合液。(1)工业上先用
 溶液吸收
溶液吸收 ,再用
,再用 使
使 再生:NaOH溶液
再生:NaOH溶液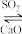 Na2SO3。使
Na2SO3。使 再生的原理是
再生的原理是(2)常温下进行“钠碱法”的模拟实验。用
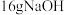 固体配成一定浓度的溶液,这些
固体配成一定浓度的溶液,这些 理论上最多可吸收
理论上最多可吸收 的体积约为
的体积约为 (折算成标准状况)。若实验时只吸收了
(折算成标准状况)。若实验时只吸收了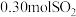 ,则反应后的吸收液中,溶质的组成为:
,则反应后的吸收液中,溶质的组成为:(3)若用碱液吸收工业尾气中的
 后,得到等物质的量浓度的
后,得到等物质的量浓度的 和
和 溶液。继续向溶液中滴入几滴
溶液。继续向溶液中滴入几滴 溶液变浑浊,请写出发生反应的离子方程式
溶液变浑浊,请写出发生反应的离子方程式
您最近半年使用:0次
名校
解题方法
2 . 某同学从物质类别、元素价态的角度,预测 和
和 部分化学性质。
部分化学性质。
(1)从物质类别角度, 属于酸性氧化物,预测
属于酸性氧化物,预测 可以和强碱反应,将少量
可以和强碱反应,将少量 通入NaOH溶液中,反应的离子方程式为
通入NaOH溶液中,反应的离子方程式为___________ 。
(2)从硫元素的价态角度分析, 既有氧化性又有还原性,
既有氧化性又有还原性,___________ 。
①将 通入酸性
通入酸性 溶液中,溶液紫色褪去,生成
溶液中,溶液紫色褪去,生成 。反应结束后,硫元素存在形式应该是
。反应结束后,硫元素存在形式应该是___________ 。
A. B.S C.
B.S C. D.
D.
② 还能和
还能和 反应,生成硫单质和水,反应的化学方程式为
反应,生成硫单质和水,反应的化学方程式为___________ 。
(3)查阅资料后发现, 的部分化学性质与
的部分化学性质与 类似。该同学向
类似。该同学向 溶液中加入稀硝酸,预测能产生一种刺激性气味的气体,该气体是
溶液中加入稀硝酸,预测能产生一种刺激性气味的气体,该气体是___________ 。但在实验过程中,他并没有检测到该气体生成,可能的原因是___________ 。
 和
和 部分化学性质。
部分化学性质。(1)从物质类别角度,
 属于酸性氧化物,预测
属于酸性氧化物,预测 可以和强碱反应,将少量
可以和强碱反应,将少量 通入NaOH溶液中,反应的离子方程式为
通入NaOH溶液中,反应的离子方程式为(2)从硫元素的价态角度分析,
 既有氧化性又有还原性,
既有氧化性又有还原性,①将
 通入酸性
通入酸性 溶液中,溶液紫色褪去,生成
溶液中,溶液紫色褪去,生成 。反应结束后,硫元素存在形式应该是
。反应结束后,硫元素存在形式应该是A.
 B.S C.
B.S C. D.
D.
②
 还能和
还能和 反应,生成硫单质和水,反应的化学方程式为
反应,生成硫单质和水,反应的化学方程式为(3)查阅资料后发现,
 的部分化学性质与
的部分化学性质与 类似。该同学向
类似。该同学向 溶液中加入稀硝酸,预测能产生一种刺激性气味的气体,该气体是
溶液中加入稀硝酸,预测能产生一种刺激性气味的气体,该气体是
您最近半年使用:0次
解题方法
3 . 如图所示是对煤燃烧产生的废气进行常温脱硫处理的基本流程示意图。
(1)试写出在废气脱硫并形成副产物的过程中所发生的主要反应的化学方程式:__________ 。
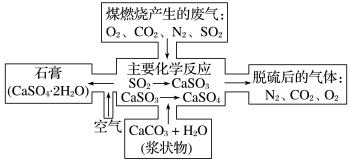
(2)废气脱硫以后含量明显增加的气体是________ (写物质名称),它对环境的负面影响是_________ 。
(3)检验脱硫后的气体中是否含有SO2的简单方法是___________________ 。
(1)试写出在废气脱硫并形成副产物的过程中所发生的主要反应的化学方程式:

(2)废气脱硫以后含量明显增加的气体是
(3)检验脱硫后的气体中是否含有SO2的简单方法是
您最近半年使用:0次
名校
解题方法
4 . 回答下列问题:
(1)写出下列物质的化学式:①钡餐:_____ ;②漂白液的有效成分:_____ 。
(2)写出木炭与浓硫酸共热时发生反应的化学方程式:_____ 。
(3)Na2SO3溶液易变质,实验室检验Na2SO3溶液是否变质的基本操作是_____ 。
(1)写出下列物质的化学式:①钡餐:
(2)写出木炭与浓硫酸共热时发生反应的化学方程式:
(3)Na2SO3溶液易变质,实验室检验Na2SO3溶液是否变质的基本操作是
您最近半年使用:0次
解题方法
5 . 人体吸入 会破坏某些酶的活性,使人体的代谢发生紊乱。为了减少危害,人们进行了许多探索和研究,并且在实际应用中取得了一定的成果。回答下列问题:
会破坏某些酶的活性,使人体的代谢发生紊乱。为了减少危害,人们进行了许多探索和研究,并且在实际应用中取得了一定的成果。回答下列问题:
(1) 具有氧化性,
具有氧化性, 与
与 反应会生成淡黄色沉淀,写出反应的化学方程式:
反应会生成淡黄色沉淀,写出反应的化学方程式:_______ 。
(2) 可以使品红溶液褪色,说明二氧化硫具有
可以使品红溶液褪色,说明二氧化硫具有_______ 性。
(3)石灰石——石膏法。该工艺原理利用石灰石加水制成的浆液( )作为吸收剂,吸收二氧化硫,并生成
)作为吸收剂,吸收二氧化硫,并生成 。再向其中通入烟气氧化生成
。再向其中通入烟气氧化生成 ,写出该工艺中生成
,写出该工艺中生成 的化学方程式:
的化学方程式:_______ 。
(4)近年来,有人提出了一种利用电解饱和氯化钠溶液循环治理含二氧化硫的废气并回收二氧化硫的方法。该方法的流程如下:
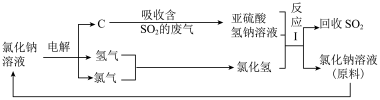
①此种方法中,可以循环利用的物质是_______ (填化学式)。
②写出电解饱和氯化钠溶液的化学方程式:_______ 。
③写出反应I的离子方程式:_______ 。
 会破坏某些酶的活性,使人体的代谢发生紊乱。为了减少危害,人们进行了许多探索和研究,并且在实际应用中取得了一定的成果。回答下列问题:
会破坏某些酶的活性,使人体的代谢发生紊乱。为了减少危害,人们进行了许多探索和研究,并且在实际应用中取得了一定的成果。回答下列问题:(1)
 具有氧化性,
具有氧化性, 与
与 反应会生成淡黄色沉淀,写出反应的化学方程式:
反应会生成淡黄色沉淀,写出反应的化学方程式:(2)
 可以使品红溶液褪色,说明二氧化硫具有
可以使品红溶液褪色,说明二氧化硫具有(3)石灰石——石膏法。该工艺原理利用石灰石加水制成的浆液(
 )作为吸收剂,吸收二氧化硫,并生成
)作为吸收剂,吸收二氧化硫,并生成 。再向其中通入烟气氧化生成
。再向其中通入烟气氧化生成 ,写出该工艺中生成
,写出该工艺中生成 的化学方程式:
的化学方程式:(4)近年来,有人提出了一种利用电解饱和氯化钠溶液循环治理含二氧化硫的废气并回收二氧化硫的方法。该方法的流程如下:

①此种方法中,可以循环利用的物质是
②写出电解饱和氯化钠溶液的化学方程式:
③写出反应I的离子方程式:
您最近半年使用:0次
6 . I.硫元素是动植物生长不可缺少的元素,硫酸是用途广泛的化工原料,可作脱水剂、吸水剂、氧化剂和催化剂等。
(1)Na2SO3溶液易变质,实验室检验Na2SO3溶液是否变质的试剂是_______ 。
(2)甲、乙两位同学用铜和硫酸做原料,设计了两种制取硫酸铜的方案。
方案甲:铜与浓硫酸加热直接反应,即Cu→CuSO4,方案乙:由Cu→CuO→CuSO4
①方案甲中,铜和浓硫酸反应的化学方程式是_______ 。
②这两种方案,你认为哪一种方案更合理?_______ 。理由是_______ 。
II.氨和硝酸是重要的工业产品,如图是工业合成氨及制备硝酸的流程示意图:
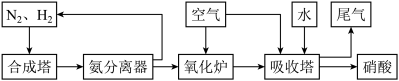
(3)合成塔中发生反应的化学方程式为_______ 。
(4)氨分离器中压强约为15MPa,温度约为-20℃,分离氨应用了氨的_______ 性质。
(5)氧化炉中,NH3转化为NO的化学方程式为_______ 。
(1)Na2SO3溶液易变质,实验室检验Na2SO3溶液是否变质的试剂是
(2)甲、乙两位同学用铜和硫酸做原料,设计了两种制取硫酸铜的方案。
方案甲:铜与浓硫酸加热直接反应,即Cu→CuSO4,方案乙:由Cu→CuO→CuSO4
①方案甲中,铜和浓硫酸反应的化学方程式是
②这两种方案,你认为哪一种方案更合理?
II.氨和硝酸是重要的工业产品,如图是工业合成氨及制备硝酸的流程示意图:

(3)合成塔中发生反应的化学方程式为
(4)氨分离器中压强约为15MPa,温度约为-20℃,分离氨应用了氨的
(5)氧化炉中,NH3转化为NO的化学方程式为
您最近半年使用:0次
名校
解题方法
7 . 请根据硫元素的价类二维图,回答下列问题:___________ ,Z转化为X所加试剂为___________ (填“氧化剂”或“还原剂”)。
(2)W的浓溶液与铜反应的化学方程式___________ 。
(3)欲制备 ,从氧化还原角度分析,合理的是___________(填字母)。
,从氧化还原角度分析,合理的是___________(填字母)。
(4)Y转化为W可以选择下列试剂___________ 。
A.酸性 溶液B.
溶液B. 溶液C.
溶液C. 溶液D.X的水溶液
溶液D.X的水溶液
写出你所选试剂将Y转化为W的离子方程式___________ 。
(5)将X与Z、W的稀溶液混合,可生成淡黄色固体,则在该反应中还原产物与氧化产物的质量之比为___________ 。

(2)W的浓溶液与铜反应的化学方程式
(3)欲制备
 ,从氧化还原角度分析,合理的是___________(填字母)。
,从氧化还原角度分析,合理的是___________(填字母)。A. | B. | C. | D. |
A.酸性
 溶液B.
溶液B. 溶液C.
溶液C. 溶液D.X的水溶液
溶液D.X的水溶液写出你所选试剂将Y转化为W的离子方程式
(5)将X与Z、W的稀溶液混合,可生成淡黄色固体,则在该反应中还原产物与氧化产物的质量之比为
您最近半年使用:0次
2023-03-21更新
|
541次组卷
|
3卷引用:四川省成都市第七中学2022-2023学年高一下学期3月月考化学试题
8 . 化学在治理空气污染方面发挥着重要的作用。
I、化石燃料的过度使用是导致酸雨的主要原因。研究表明,NOx、SO2形成酸雨时的转化关系如图所示:
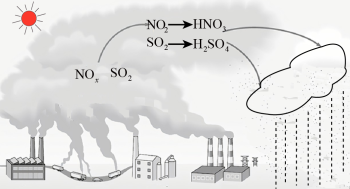
(1)HNO3的电离方程式为_______ 。
(2)SO2会被雨水吸收形成酸雨,这种酸雨在空气中久置酸性增强的原因是_______ (用化学方程式表示)。
Ⅱ、NOx、SO2等均为大气污染物,需处理后才能排放。
(3)用NaOH溶液可以吸收NOx,反应的化学方程式如下:
i.
ii.
①反应i中,每消耗0.3molNO2,转移电子数为_______ 。
②反应ii中,氧化剂和还原剂的物质的量之比为_______ 。
(4)用氨水可以吸收SO2制取铵盐。
①实验室用NH4Cl和Ca(OH)2制取NH3的化学方程式为_______ 。
②用足量氨水吸收SO2的化学方程式为_______ 。
(5)利用NaClO吸收液可在脱除烟气中NOx的同时脱除SO2。研究发现在不同的初始pH条件下,吸收液对流动烟气的脱硫效率都接近100%,而对NO的脱除率如下图所示。
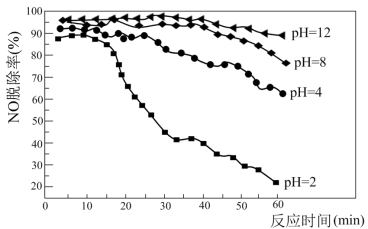
pH=2时,脱除SO2的离子方程式为_______ ;脱硝效率随反应时间的延长而逐渐降低的可能原因是_______ 。
I、化石燃料的过度使用是导致酸雨的主要原因。研究表明,NOx、SO2形成酸雨时的转化关系如图所示:

(1)HNO3的电离方程式为
(2)SO2会被雨水吸收形成酸雨,这种酸雨在空气中久置酸性增强的原因是
Ⅱ、NOx、SO2等均为大气污染物,需处理后才能排放。
(3)用NaOH溶液可以吸收NOx,反应的化学方程式如下:
i.

ii.

①反应i中,每消耗0.3molNO2,转移电子数为
②反应ii中,氧化剂和还原剂的物质的量之比为
(4)用氨水可以吸收SO2制取铵盐。
①实验室用NH4Cl和Ca(OH)2制取NH3的化学方程式为
②用足量氨水吸收SO2的化学方程式为
(5)利用NaClO吸收液可在脱除烟气中NOx的同时脱除SO2。研究发现在不同的初始pH条件下,吸收液对流动烟气的脱硫效率都接近100%,而对NO的脱除率如下图所示。

pH=2时,脱除SO2的离子方程式为
您最近半年使用:0次
9 . SO2、Na2SO3、Na2S2O5(焦亚硫酸钠)中都含有+4价的S,具有还原性。
(1)Na2SO3是实验室常用试剂。
①Na2SO3固体需密封保存,其原因是______ 。
②实验室用Na2SO3固体与浓硫酸制备SO2,该反应的化学方程式为______ 。
③在Br2水中加入Na2SO3溶液反应的离子方程式为______ 。
(2)一定条件下,将SO2通入TeOSO4溶液中,反应一段时间后过滤、洗涤得到粗Te。
①SO2还原TeOSO4溶液得到Te的反应中,n(SO2):n(TeOSO4)=______ 。
②“洗涤”的具体操作为______ 。
③过程中须控制反应温度为80℃,温度不能过高的原因是______ 。
(3)焦亚硫酸钠(Na2S2O5)空气法处理含氰废水的部分机理如下,其中[O]代表活性氧原子,具有强氧化性:S2O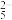 +H2O=2SO
+H2O=2SO +2H+、SO
+2H+、SO +O2=SO
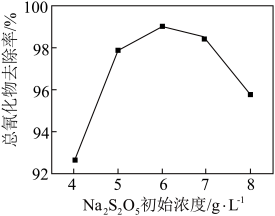
+O2=SO +[O]、CN-+[O]=CNO-。其他条件相同时,废水中氰化物去除率随Na2S2O5初始浓度的变化如图所示。当Na2S2O5初始浓度大于6g•L-1时,总氰化物去除率下降的原因可能是
+[O]、CN-+[O]=CNO-。其他条件相同时,废水中氰化物去除率随Na2S2O5初始浓度的变化如图所示。当Na2S2O5初始浓度大于6g•L-1时,总氰化物去除率下降的原因可能是______ 。
(1)Na2SO3是实验室常用试剂。
①Na2SO3固体需密封保存,其原因是
②实验室用Na2SO3固体与浓硫酸制备SO2,该反应的化学方程式为
③在Br2水中加入Na2SO3溶液反应的离子方程式为
(2)一定条件下,将SO2通入TeOSO4溶液中,反应一段时间后过滤、洗涤得到粗Te。
①SO2还原TeOSO4溶液得到Te的反应中,n(SO2):n(TeOSO4)=
②“洗涤”的具体操作为
③过程中须控制反应温度为80℃,温度不能过高的原因是
(3)焦亚硫酸钠(Na2S2O5)空气法处理含氰废水的部分机理如下,其中[O]代表活性氧原子,具有强氧化性:S2O
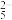 +H2O=2SO
+H2O=2SO +2H+、SO
+2H+、SO +O2=SO
+O2=SO +[O]、CN-+[O]=CNO-。其他条件相同时,废水中氰化物去除率随Na2S2O5初始浓度的变化如图所示。当Na2S2O5初始浓度大于6g•L-1时,总氰化物去除率下降的原因可能是
+[O]、CN-+[O]=CNO-。其他条件相同时,废水中氰化物去除率随Na2S2O5初始浓度的变化如图所示。当Na2S2O5初始浓度大于6g•L-1时,总氰化物去除率下降的原因可能是
您最近半年使用:0次
解题方法
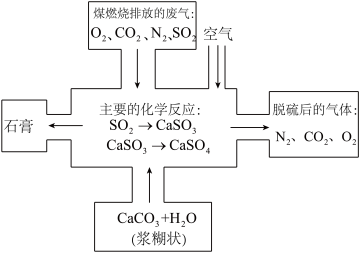
10 . 煤是一种常用的燃料。煤燃烧产生的废气中含有的二氧化硫等有害气体会对环境造成污染,因此需要将废气净化后再排放。
(1)这些废气会对环境造成怎样的影响?__________
(2)如果废气中的二氧化硫进入大气,会发生哪些化学变化?写出相关反应的化学方程式。__________
(3)如图是对煤燃烧产生的废气进行脱硫处理的基本流程图,试写出废气脱硫过程中发生的主要反应的化学方程式。__________

(1)这些废气会对环境造成怎样的影响?
(2)如果废气中的二氧化硫进入大气,会发生哪些化学变化?写出相关反应的化学方程式。
(3)如图是对煤燃烧产生的废气进行脱硫处理的基本流程图,试写出废气脱硫过程中发生的主要反应的化学方程式。
您最近半年使用:0次



