解题方法
1 . 苯甲酸可用作食品防腐剂。实验室可通过甲苯(密度为0.87g·mL-1) 氧化制苯甲酸,其反应原理、制备装置如下:
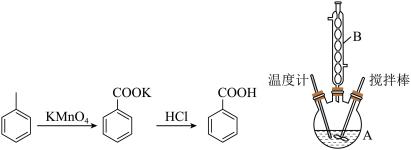
实验步骤:
I.向仪器A 中加入1.5mL甲苯、100mL水和4.8g(约0.03mol)高锰酸钾(被还原为MnO2),慢慢搅拌,并加热回流约30min后停止加热并继续搅拌1 min。
Ⅱ.将反应液与适量饱和亚硫酸氢钠溶液混合振荡,过滤、洗涤,将滤液、洗涤液合并放在置于冰水浴中的烧杯内,再用浓盐酸酸化至苯甲酸完全析出。将析出的苯甲酸过滤,用适量X洗涤、然后干燥,称量,得到1.0g粗产品。
Ⅲ.纯度测定:称取0.150g 粗产品(杂质不与NaOH反应),配成乙醇溶液并置于100 mL容量瓶中定容。每次移取25.00mL溶液,用0.01000mol·L-¹的NaOH标准溶液滴定,三次滴定平均消耗22.50mL的NaOH标准溶液。
回答下列问题:
(1)仪器 A 的名称是___________ ,其最适宜规格为___________ (填字母)。
a.100mL b.250mL c.500mL d.1000mL
(2)步骤Ⅱ中的适量饱和亚硫酸氢钠溶液的作用是___________ 。使用冰水浴的目的是___________ ,X是___________ 。
(3)装置中仪器B的作用是___________
(4)本实验制备的苯甲酸的纯度为___________ %(保留1位小数)。
(5)若要得到纯度更高的苯甲酸,可通过___________ 的方法提纯。

| 名称 | 相对分子质量 | 熔点/℃ | 沸点/℃ | 溶解性 |
| 甲苯 | 92 | -95 | 110.6 | 不溶于水,易溶于乙醇 |
| 苯甲酸 | 122 | 122.4 | 248 | 微溶于冷水,易溶于乙醇、热水 |
I.向仪器A 中加入1.5mL甲苯、100mL水和4.8g(约0.03mol)高锰酸钾(被还原为MnO2),慢慢搅拌,并加热回流约30min后停止加热并继续搅拌1 min。
Ⅱ.将反应液与适量饱和亚硫酸氢钠溶液混合振荡,过滤、洗涤,将滤液、洗涤液合并放在置于冰水浴中的烧杯内,再用浓盐酸酸化至苯甲酸完全析出。将析出的苯甲酸过滤,用适量X洗涤、然后干燥,称量,得到1.0g粗产品。
Ⅲ.纯度测定:称取0.150g 粗产品(杂质不与NaOH反应),配成乙醇溶液并置于100 mL容量瓶中定容。每次移取25.00mL溶液,用0.01000mol·L-¹的NaOH标准溶液滴定,三次滴定平均消耗22.50mL的NaOH标准溶液。
回答下列问题:
(1)仪器 A 的名称是
a.100mL b.250mL c.500mL d.1000mL
(2)步骤Ⅱ中的适量饱和亚硫酸氢钠溶液的作用是
(3)装置中仪器B的作用是
(4)本实验制备的苯甲酸的纯度为
(5)若要得到纯度更高的苯甲酸,可通过
您最近一年使用:0次
2 . 某同学通过如下流程制备Cu2O,已知CuCl难溶于水和稀硫酸。

下列说法错误的是

下列说法错误的是
| A.步骤②中氧化剂和还原剂物质的量之比为1:2 |
| B.步骤③中为防止CuCl被氧化,可用Na2SO3溶液洗涤 |
C.步骤④发生反应的离子方程式为 |
| D.步骤⑤可以用HNO3酸化的AgNO3溶液检验沉淀是否洗涤干净 |
您最近一年使用:0次
2023-07-11更新
|
172次组卷
|
2卷引用:福建省漳州市2022-2023学年高一下学期期末教学质量检测化学试题
3 . 宏观辨识与微观探析是化学学科核心素养之一、下列离子方程式书写正确的是
A. 溶于水: 溶于水: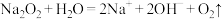 |
B.铜与氯化铁溶液反应: |
C. 溶液与过量的 溶液与过量的 溶液混合: 溶液混合: |
D.向 溶液中通入氯气: 溶液中通入氯气: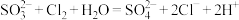 |
您最近一年使用:0次
名校
解题方法
4 . 氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业。工业以硫化铜精矿为原料,设计符合绿色化学理念的制备CuCl的流程如图:

已知:CuCl难溶于水和乙醇,潮湿时易水解氧化。
下列说法正确的是

已知:CuCl难溶于水和乙醇,潮湿时易水解氧化。
下列说法正确的是
| A.步骤①焙烧产生的有毒气体,可以使紫色石蕊溶液先变红后褪色,体现了漂白性 |
| B.步骤②中可以用硝酸代替硫酸,不影响后续处理 |
C.步骤③离子方程式: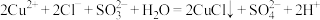 |
| D.步骤④用的乙醇洗涤,也可以使用蒸馏水洗涤 |
您最近一年使用:0次
2023-06-29更新
|
158次组卷
|
2卷引用:湖北省咸宁市2022-2023学年高一下学期期末考试化学试题
名校
解题方法
5 . 元素周期表中第ⅥA族元素单质及其化合物有着广泛应用。 、
、 具有杀菌、消毒、漂白等作用。硫磺、黄铁矿(
具有杀菌、消毒、漂白等作用。硫磺、黄铁矿( )可作为工业制硫酸的原料,辉铜矿(
)可作为工业制硫酸的原料,辉铜矿( )煅烧时可发生反应:
)煅烧时可发生反应: 。
。 直接排放会造成环境污染,可将其转化或用石灰乳、
直接排放会造成环境污染,可将其转化或用石灰乳、 等物质进行回收再利用。
等物质进行回收再利用。 与
与 的水溶液反应可制备硒。下列物质性质与应用对应关系正确的是
的水溶液反应可制备硒。下列物质性质与应用对应关系正确的是
 、
、 具有杀菌、消毒、漂白等作用。硫磺、黄铁矿(
具有杀菌、消毒、漂白等作用。硫磺、黄铁矿( )可作为工业制硫酸的原料,辉铜矿(
)可作为工业制硫酸的原料,辉铜矿( )煅烧时可发生反应:
)煅烧时可发生反应: 。
。 直接排放会造成环境污染,可将其转化或用石灰乳、
直接排放会造成环境污染,可将其转化或用石灰乳、 等物质进行回收再利用。
等物质进行回收再利用。 与
与 的水溶液反应可制备硒。下列物质性质与应用对应关系正确的是
的水溶液反应可制备硒。下列物质性质与应用对应关系正确的是A. 有还原性,可用于吸收尾气 有还原性,可用于吸收尾气 | B. 有强氧化性,可用作食品的漂白剂 有强氧化性,可用作食品的漂白剂 |
| C.浓硫酸具有脱水性,可用作酯化反应的催化剂 | D.乙醇是有机溶剂,可用于萃取碘水中的碘单质 |
您最近一年使用:0次
6 . 宏观辨识与微观探析是化学学科核心素养之一、下列方程式符合题意的是
A.向 溶液中滴加少量NaClO溶液: 溶液中滴加少量NaClO溶液: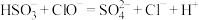 |
B.向溴的四氯化碳溶液中通入丙烯,溶液褪色并分层: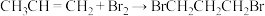 |
C.在 溶液中滴加稀盐酸,溶液变黄色: 溶液中滴加稀盐酸,溶液变黄色: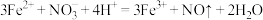 |
D.甲醇( )和乙酸、浓硫酸混合并共热制备乙酸甲酯: )和乙酸、浓硫酸混合并共热制备乙酸甲酯: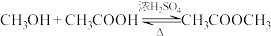 |
您最近一年使用:0次
2023-06-28更新
|
125次组卷
|
3卷引用:江西省重点中学九江六校2022-2023学年高一下学期期末联考化学试题
名校
7 . 如图所示装置,将 、
、 通入
通入 中制备氯化亚砜(
中制备氯化亚砜( )。已知:①
)。已知:① 是一种液态化合物,沸点为77℃;②
是一种液态化合物,沸点为77℃;② 遇水剧烈反应,液面上产生白雾,并有刺激性气味的气体产生。请回答以下问题:
遇水剧烈反应,液面上产生白雾,并有刺激性气味的气体产生。请回答以下问题:

(1)下列固体药品均可与 反应制备
反应制备 ,最不适合的是
,最不适合的是_____ 。
A. B.
B.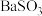 C.
C.
(2)装置e中的试剂为_____ 。
(3)写出制备 的化学方程式
的化学方程式_____ 。
(4)若反应中向过量 中共计通入
中共计通入 的体积为925mL(S.T.P.),
的体积为925mL(S.T.P.), 的体积为896mL(S.T.P.),最后得到产品4.76g
的体积为896mL(S.T.P.),最后得到产品4.76g ,则
,则 的产率(实际产量与理论产量之比)为
的产率(实际产量与理论产量之比)为_____ 。
(5)若用碱液吸收工业尾气中的 后,得到等物质的量浓度的
后,得到等物质的量浓度的 和
和 溶液。继续向溶液中滴入几滴
溶液。继续向溶液中滴入几滴 溶液变浑浊,请写出发生反应的离子方程式
溶液变浑浊,请写出发生反应的离子方程式_____ 。
 、
、 通入
通入 中制备氯化亚砜(
中制备氯化亚砜( )。已知:①
)。已知:① 是一种液态化合物,沸点为77℃;②
是一种液态化合物,沸点为77℃;② 遇水剧烈反应,液面上产生白雾,并有刺激性气味的气体产生。请回答以下问题:
遇水剧烈反应,液面上产生白雾,并有刺激性气味的气体产生。请回答以下问题:
(1)下列固体药品均可与
 反应制备
反应制备 ,最不适合的是
,最不适合的是A.
 B.
B.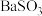 C.
C.
(2)装置e中的试剂为
(3)写出制备
 的化学方程式
的化学方程式(4)若反应中向过量
 中共计通入
中共计通入 的体积为925mL(S.T.P.),
的体积为925mL(S.T.P.), 的体积为896mL(S.T.P.),最后得到产品4.76g
的体积为896mL(S.T.P.),最后得到产品4.76g ,则
,则 的产率(实际产量与理论产量之比)为
的产率(实际产量与理论产量之比)为(5)若用碱液吸收工业尾气中的
 后,得到等物质的量浓度的
后,得到等物质的量浓度的 和
和 溶液。继续向溶液中滴入几滴
溶液。继续向溶液中滴入几滴 溶液变浑浊,请写出发生反应的离子方程式
溶液变浑浊,请写出发生反应的离子方程式
您最近一年使用:0次
8 . 下列操作不会引起化学反应的是
| A.硝酸亚铁溶液中加入稀硫酸 | B.室温下将氧气和氢气以1∶2体积比混和 |
| C.常温下铝片伸入浓硫酸 | D.将亚硫酸溶液与氢硫酸混和 |
您最近一年使用:0次
名校
解题方法
9 . 亚硫酸具有酸性,且
| A.无氧化性,无还原性 | B.有氧化性,无还原性 | C.有氧化性,有还原性 | D.无氧化性,有还原性 |
您最近一年使用:0次
2023-06-25更新
|
166次组卷
|
2卷引用:上海市进才中学2022-2023学年高一下学期期末考试化学试题
名校
解题方法
10 . 某同学为了验证Fe2+是否能将H2SO3氧化成 ,用50mL,0.1mol/LFeCl3溶液吸收一定量的
,用50mL,0.1mol/LFeCl3溶液吸收一定量的 气体后,进行以下实验:
气体后,进行以下实验:
(1)检验吸收液中是否含有 的操作为
的操作为_____________ 。
(2)请写出FeCl3吸收SO2的离子方程式:___________ ,反应中的氧化产物是__________ 。
(3)吸收液中除了含有H+、Cl-、 以外,该同学对其他成分(Fe3+、Fe2+、H2SO3)的可能组合进行了猜想和探究:
以外,该同学对其他成分(Fe3+、Fe2+、H2SO3)的可能组合进行了猜想和探究:
①提出假设。
假设1:溶液中存在Fe2+
假设2:溶液中存在Fe3+、Fe2+
假设3:溶液中存在__________ 。
②设计方案,进行实验,验证假设。
请写出实验步骤以及预期现象和结论(可不填满)。限选实验试剂和仪器:试管、滴管、0.1mol/LKMnO4溶液、0.1mol/LKSCN溶液、品红溶液。
 ,用50mL,0.1mol/LFeCl3溶液吸收一定量的
,用50mL,0.1mol/LFeCl3溶液吸收一定量的 气体后,进行以下实验:
气体后,进行以下实验:(1)检验吸收液中是否含有
 的操作为
的操作为(2)请写出FeCl3吸收SO2的离子方程式:
(3)吸收液中除了含有H+、Cl-、
 以外,该同学对其他成分(Fe3+、Fe2+、H2SO3)的可能组合进行了猜想和探究:
以外,该同学对其他成分(Fe3+、Fe2+、H2SO3)的可能组合进行了猜想和探究:①提出假设。
假设1:溶液中存在Fe2+
假设2:溶液中存在Fe3+、Fe2+
假设3:溶液中存在
②设计方案,进行实验,验证假设。
请写出实验步骤以及预期现象和结论(可不填满)。限选实验试剂和仪器:试管、滴管、0.1mol/LKMnO4溶液、0.1mol/LKSCN溶液、品红溶液。
| 实验步骤 | 预期现象和结论 |
| 步骤1:用试管取样品溶液2~3mL,滴入 | 若 |
| 步骤2: | 若 |
| 步骤3(可补充): |
您最近一年使用:0次



