1 . 能正确表示下列反应的离子方程式为
A.过量铁粉加入稀硝酸中:Fe+4H++NO =Fe3++NO↑+2H2O =Fe3++NO↑+2H2O |
| B.氯化铜溶液中通入硫化氢:Cu2++S2-=CuS↓ |
C.用Na2SO3溶液吸收少量Cl2:3SO +Cl2+H2O=2HSO +Cl2+H2O=2HSO +2Cl-+SO +2Cl-+SO |
D.同浓度同体积NH4HSO4溶液与NaOH溶液混合:NH +OH-=NH3•H2O +OH-=NH3•H2O |
您最近半年使用:0次
2 . Ⅰ.某小组利用数字化实验模拟制备Fe(OH)2并探究其相关性质。
(1)模拟制备Fe(OH)2装置如图:打开右瓶上方空气过滤器的气阀(平衡压强,便于FeSO4溶液能够进入右瓶);然后,依次打开鲁尔阀、推动注射器,将注射器中的FeSO4溶液加入左瓶的溶液中,促使左瓶中的FeSO4溶液流入右瓶;当右瓶中明显有白色沉淀生成时,停止加液,依次关闭鲁尔阀、关闭右瓶上方的空气过滤器的气阀、打开左瓶上方的空气过滤器的气阀。实验证明制备Fe(OH)2最佳pH是6~8,氨水代替NaOH溶液效果更好的原因是_____ ,Na2SO3的作用是_____ 。
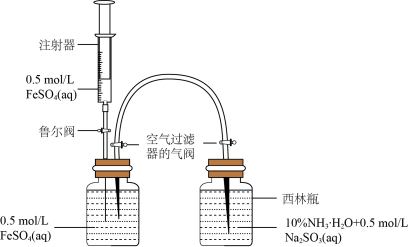
(2)探究原材料FeSO4的相关性质。向50mL蒸馏水中加入FeSO4·7H2O晶体搅拌以加快溶解,用溶解氧传感器测定液体中溶解氧浓度随时间的变化, 点时加入NaOH溶液所得曲线如图。
点时加入NaOH溶液所得曲线如图。

对比ab、bc段溶解氧的消耗速率,可以得出什么结论_____ 。
(3)已知:在 时溶液中,
时溶液中, 被氧化成
被氧化成 的过程中会产生
的过程中会产生 ,且
,且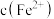 降低量大于
降低量大于 增加量,
增加量, 几乎不变,用总离子方程式说明原因
几乎不变,用总离子方程式说明原因_____ ,检验反应后的溶液中是否存在 ,可以选择的试剂是
,可以选择的试剂是_____ 。
A.NaOH溶液 B.K3[Fe(CN)6] C.KSCN D.KMnO4
Ⅱ.
(4)用氢氧化钠固体配制实验所需的NaOH溶液,下列图示对应的操作规范的是_____
(5)用NaOH固体配制实验所需的NaOH溶液时,下列操作会导致所配溶液浓度偏高的是_____ 。
A.未冷却至室温就定容
B.容量瓶用蒸馏水洗净后未干燥
C.定容时俯视读取刻度
D.定容时液面超过了刻度线,并将多余溶液吸出
E.称量NaOH时用了生锈的砝码
(1)模拟制备Fe(OH)2装置如图:打开右瓶上方空气过滤器的气阀(平衡压强,便于FeSO4溶液能够进入右瓶);然后,依次打开鲁尔阀、推动注射器,将注射器中的FeSO4溶液加入左瓶的溶液中,促使左瓶中的FeSO4溶液流入右瓶;当右瓶中明显有白色沉淀生成时,停止加液,依次关闭鲁尔阀、关闭右瓶上方的空气过滤器的气阀、打开左瓶上方的空气过滤器的气阀。实验证明制备Fe(OH)2最佳pH是6~8,氨水代替NaOH溶液效果更好的原因是

(2)探究原材料FeSO4的相关性质。向50mL蒸馏水中加入FeSO4·7H2O晶体搅拌以加快溶解,用溶解氧传感器测定液体中溶解氧浓度随时间的变化,
 点时加入NaOH溶液所得曲线如图。
点时加入NaOH溶液所得曲线如图。
对比ab、bc段溶解氧的消耗速率,可以得出什么结论
(3)已知:在
 时溶液中,
时溶液中, 被氧化成
被氧化成 的过程中会产生
的过程中会产生 ,且
,且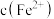 降低量大于
降低量大于 增加量,
增加量, 几乎不变,用总离子方程式说明原因
几乎不变,用总离子方程式说明原因 ,可以选择的试剂是
,可以选择的试剂是A.NaOH溶液 B.K3[Fe(CN)6] C.KSCN D.KMnO4
Ⅱ.
(4)用氢氧化钠固体配制实验所需的NaOH溶液,下列图示对应的操作规范的是_____
 |  | 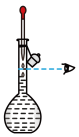 |  |
| A.称量 | B.转移 | C、定容 | D、摇匀 |
| A.A | B.B | C.C | D.D |
(5)用NaOH固体配制实验所需的NaOH溶液时,下列操作会导致所配溶液浓度偏高的是
A.未冷却至室温就定容
B.容量瓶用蒸馏水洗净后未干燥
C.定容时俯视读取刻度
D.定容时液面超过了刻度线,并将多余溶液吸出
E.称量NaOH时用了生锈的砝码
您最近半年使用:0次
解题方法
3 . 化合物X是一种蓝黑色(有时是粉红色)的固体,是一种由趋磁细菌制造的生物矿。某研究小组按如下流程探究该固体的组成:

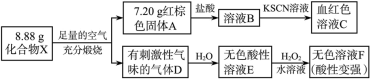
请回答:
(1)X的化学式为___________ 。
(2)请写出E反应生成F的化学方程式:___________ 。
(3)化合物X(只含两种元素)与盐酸反应,反应后得到浅绿色溶液,同时生成一种浅黄色不溶物和一种臭鸡蛋气味气体,请写出该反应的离子方程式:___________ 。


请回答:
(1)X的化学式为
(2)请写出E反应生成F的化学方程式:
(3)化合物X(只含两种元素)与盐酸反应,反应后得到浅绿色溶液,同时生成一种浅黄色不溶物和一种臭鸡蛋气味气体,请写出该反应的离子方程式:
您最近半年使用:0次
解题方法
4 . 下列除杂试剂或方法正确的是
| 选项 | 被提纯物质 | 杂质 | 除杂试剂或方法 |
| A |  溶液 溶液 |  | 加入过量 溶液并过滤、洗涤 溶液并过滤、洗涤再将沉淀溶于适量盐酸 |
| B | 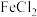 溶液 溶液 |  | 加入过量铜粉并过滤、洗涤 |
| C |  |  | 在空气中灼烧至质量不再变化 |
| D |  |  | 在空气中灼烧至质量不再变化 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
5 . 焦亚硫酸钠(Na2S2O5)常用作葡萄酒、果脯等食品的抗氧化剂。
I.焦亚硫酸钠的制备
已知:①Na2S2O5在空气中、受热时均易分解。
②生成Na2S2O5的化学方程式为2NaHSO3=Na2S2O5+H2O。
③水溶液中H2SO3、HSO 、SO
、SO 的物质的量分数随pH的分布如图1所示。
的物质的量分数随pH的分布如图1所示。
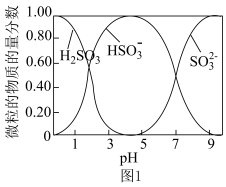
(1)SO2与Na2CO3过饱和溶液反应生成NaHSO3和CO2,其离子方程式为___________ 。
(2)实验室制备少量Na2S2O5的装置如图2所示,请补充完整相应实验方案:在不断搅拌下,控制反应温度在40℃左右,___________ ,20℃静置结晶,经减压抽滤、洗涤、25~30 ℃干燥,可获得Na2S2O5固体。
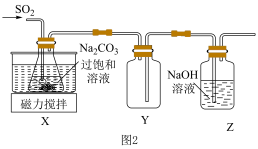
(3)实验制得的Na2S2O5固体中含有一定量的Na2SO4,其原因是___________ 。
Ⅱ.焦亚硫酸钠含量的测定
工业焦亚硫酸钠优质品要求质量分数≥96.5%。通过下列实验检测焦亚硫酸钠样品是否达到优质品标准。实验检测原理为:
Na2S2O5+CH3COOH+I2+H2O—H2SO4+HI+CH3COONa(未配平);
I2+2Na2S2O3=Na2S4O6+2NaI。
准确称取0.1950g样品,快速置于预先加入30.00 mL 0.100 0 mol·L-1碘标准液及20 mL水的250 mL碘量瓶中,加入5 mL乙酸溶液,立即盖上瓶塞,水封,缓缓摇动溶解后,置于暗处放置5 min;用0.1000 mol·L-1 Na2S2O3标准溶液滴定至溶液呈微黄色,加入淀粉指示剂,继续滴定至终点,消耗Na2S2O3溶液20.00 mL。
(4)滴定终点现象是___________ 。
(5)通过计算判断该样品是否为优质品是___________ (写出计算过程)。
I.焦亚硫酸钠的制备
已知:①Na2S2O5在空气中、受热时均易分解。
②生成Na2S2O5的化学方程式为2NaHSO3=Na2S2O5+H2O。
③水溶液中H2SO3、HSO
 、SO
、SO 的物质的量分数随pH的分布如图1所示。
的物质的量分数随pH的分布如图1所示。
(1)SO2与Na2CO3过饱和溶液反应生成NaHSO3和CO2,其离子方程式为
(2)实验室制备少量Na2S2O5的装置如图2所示,请补充完整相应实验方案:在不断搅拌下,控制反应温度在40℃左右,

(3)实验制得的Na2S2O5固体中含有一定量的Na2SO4,其原因是
Ⅱ.焦亚硫酸钠含量的测定
工业焦亚硫酸钠优质品要求质量分数≥96.5%。通过下列实验检测焦亚硫酸钠样品是否达到优质品标准。实验检测原理为:
Na2S2O5+CH3COOH+I2+H2O—H2SO4+HI+CH3COONa(未配平);
I2+2Na2S2O3=Na2S4O6+2NaI。
准确称取0.1950g样品,快速置于预先加入30.00 mL 0.100 0 mol·L-1碘标准液及20 mL水的250 mL碘量瓶中,加入5 mL乙酸溶液,立即盖上瓶塞,水封,缓缓摇动溶解后,置于暗处放置5 min;用0.1000 mol·L-1 Na2S2O3标准溶液滴定至溶液呈微黄色,加入淀粉指示剂,继续滴定至终点,消耗Na2S2O3溶液20.00 mL。
(4)滴定终点现象是
(5)通过计算判断该样品是否为优质品是
您最近半年使用:0次
名校
解题方法
6 . 硫及其化合物在生产、生活和科学研究中有着广泛的作用。对燃煤烟气脱硫能有效减少对大气的污染并实现资源化利用。方法1用氨水将  先转化为
先转化为 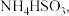 再氧化为
再氧化为 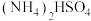 ;方法2用生物质热解气(主要成分为CO、CH4、H2)将
;方法2用生物质热解气(主要成分为CO、CH4、H2)将  在高温下还原为单质硫;方法3用
在高温下还原为单质硫;方法3用  溶液吸收
溶液吸收  生成
生成  ,再加热吸收液,使之重新生成亚硫酸钠;方法4用
,再加热吸收液,使之重新生成亚硫酸钠;方法4用  溶液吸收烟气中
溶液吸收烟气中  ,使用惰性电极电解吸收后的溶液,
,使用惰性电极电解吸收后的溶液, 在阴极被还原为硫单质。可以用
在阴极被还原为硫单质。可以用  溶液除去
溶液除去 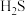 气体,生成黑色
气体,生成黑色  沉淀。下列化学反应表示不正确的是
沉淀。下列化学反应表示不正确的是
 先转化为
先转化为 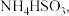 再氧化为
再氧化为 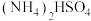 ;方法2用生物质热解气(主要成分为CO、CH4、H2)将
;方法2用生物质热解气(主要成分为CO、CH4、H2)将  在高温下还原为单质硫;方法3用
在高温下还原为单质硫;方法3用  溶液吸收
溶液吸收  生成
生成  ,再加热吸收液,使之重新生成亚硫酸钠;方法4用
,再加热吸收液,使之重新生成亚硫酸钠;方法4用  溶液吸收烟气中
溶液吸收烟气中  ,使用惰性电极电解吸收后的溶液,
,使用惰性电极电解吸收后的溶液, 在阴极被还原为硫单质。可以用
在阴极被还原为硫单质。可以用  溶液除去
溶液除去 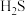 气体,生成黑色
气体,生成黑色  沉淀。下列化学反应表示不正确的是
沉淀。下列化学反应表示不正确的是A.氨水吸收  的反应: 的反应: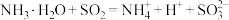 |
B. 还原 还原  的反应:2CO+SO2 的反应:2CO+SO2 S+2CO2 S+2CO2 |
C. 吸收液再生的反应: 吸收液再生的反应: |
D.电解吸收  后的溶液的总反应:3H2SO3 后的溶液的总反应:3H2SO3 S↓+2H2SO4+H2O S↓+2H2SO4+H2O |
您最近半年使用:0次
7 . 某研究小组同学为探究锌与硫酸反应生成 、
、 的临界浓度(浓硫酸能与锌反应生成
的临界浓度(浓硫酸能与锌反应生成 的最低浓度)设计了如图实验(加热和夹持装置已省略)。
的最低浓度)设计了如图实验(加热和夹持装置已省略)。
已知:锌与浓硫酸开始时反应缓慢,可以适当加热以加速其反应,当有大量气泡生成时,该反应速率会明显加快并伴有大量的热放出。
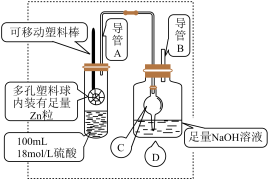
移动塑料棒,使锌浸没到硫酸中充分反应,反应结束后向D装置中加入足量的 溶液,再加入足量的
溶液,再加入足量的 溶液,充分反应后将所得沉淀过滤、洗涤、干燥、称量得到固体质量为a g。
溶液,充分反应后将所得沉淀过滤、洗涤、干燥、称量得到固体质量为a g。
(1)加入H₂O₂溶液发生反应的离子方程式是___________ 。
(2)浓硫酸与锌反应的临界浓度为___________ mol·L-1(用含a的计算式表示,忽略溶液体积变化)。
 、
、 的临界浓度(浓硫酸能与锌反应生成
的临界浓度(浓硫酸能与锌反应生成 的最低浓度)设计了如图实验(加热和夹持装置已省略)。
的最低浓度)设计了如图实验(加热和夹持装置已省略)。已知:锌与浓硫酸开始时反应缓慢,可以适当加热以加速其反应,当有大量气泡生成时,该反应速率会明显加快并伴有大量的热放出。

移动塑料棒,使锌浸没到硫酸中充分反应,反应结束后向D装置中加入足量的
 溶液,再加入足量的
溶液,再加入足量的 溶液,充分反应后将所得沉淀过滤、洗涤、干燥、称量得到固体质量为a g。
溶液,充分反应后将所得沉淀过滤、洗涤、干燥、称量得到固体质量为a g。(1)加入H₂O₂溶液发生反应的离子方程式是
(2)浓硫酸与锌反应的临界浓度为
您最近半年使用:0次
名校
8 . 书写下列反应的离子 方程式:
(1)以NaIO3为原料制备I2的方法是:先向NaIO3溶液中加入计量的NaHSO3,生成碘化物;再向混合溶液中加入NaIO3溶液,反应得到I2.上述制备I2的总反应___________ 。
(2)在酸性条件下,黄铁矿(FeS2,其中S为-1价)催化氧化的反应转化如图所示。
总反应:2FeS2+7O2+2H2O=2Fe2++4 +4H+
+4H+
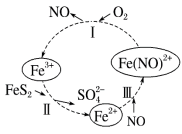
①反应I:___________ 。
②反应II:___________ 。
(3)红磷充分燃烧的产物与足量热的NaOH溶液反应,该反应的离子方程式是___________ 。
(4)取FeSO4溶液,调pH约为7,加入淀粉KI溶液和H2O2,溶液呈褐色并有红褐色沉淀生成。当消耗2molI-时,共转移3mol电子,该反应的离子方程式是___________ 。
(5)NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如图所示:
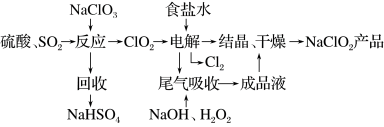
①写出“反应”步骤中生成ClO2的化学方程式:___________ 。
② “电解”过程阴极主反应的方程式:___________ 。
③“尾气吸收”是吸收“电解”过程排出的少量ClO2,写出此吸收反应的离子方程式:___________ 。
(1)以NaIO3为原料制备I2的方法是:先向NaIO3溶液中加入计量的NaHSO3,生成碘化物;再向混合溶液中加入NaIO3溶液,反应得到I2.上述制备I2的总反应
(2)在酸性条件下,黄铁矿(FeS2,其中S为-1价)催化氧化的反应转化如图所示。
总反应:2FeS2+7O2+2H2O=2Fe2++4
 +4H+
+4H+
①反应I:
②反应II:
(3)红磷充分燃烧的产物与足量热的NaOH溶液反应,该反应的离子方程式是
(4)取FeSO4溶液,调pH约为7,加入淀粉KI溶液和H2O2,溶液呈褐色并有红褐色沉淀生成。当消耗2molI-时,共转移3mol电子,该反应的离子方程式是
(5)NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如图所示:

①写出“反应”步骤中生成ClO2的化学方程式:
② “电解”过程阴极主反应的方程式:
③“尾气吸收”是吸收“电解”过程排出的少量ClO2,写出此吸收反应的离子方程式:
您最近半年使用:0次
9 . 室温下,探究向5mL0.50mol/LNa2SO3溶液中滴加2滴0.50mol/LFeCl3溶液后的产物,下列实验方案和结论不正确的是
| 选项 | 实验方案 | 实验结论 |
| A | 取反应后的上层清液,先加入盐酸,后加入BaCl2溶液,没有白色沉淀生成。 | 没有生成Na2SO4 |
| B | 滴加FeCl3溶液后,立即用激光灯照射,观察到一条光亮的通路。 | 生成了Fe(OH)3胶体 |
| C | 向反应后的溶液中滴加几滴酸性KMnO4溶液,紫红色褪去。 | 混合液含有Fe2+ |
| D | 将等体积的Na2SO3溶液和FeCl3溶液混合放置一小时后,溶液变为淡绿色。 | Na2SO3能还原FeCl3 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
10 . 下列离子方程式书写正确的是
A.磁性氧化铁可溶于稀硝酸: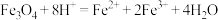 |
B. 溶液中滴加足量的溴水: 溶液中滴加足量的溴水: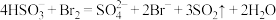 |
C.偏铝酸钠和盐酸2:3混合: |
D. 溶液与 溶液与 溶液等浓度等体积混合: 溶液等浓度等体积混合: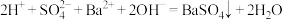 |
您最近半年使用:0次



