名校
1 . 下列说法中,可以证明醋酸是弱电解质的是
| A.醋酸溶液具有导电性 |
| B.醋酸能与水以任意比互溶 |
C.常温下, 的醋酸溶液中, 的醋酸溶液中,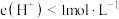 |
D.10mL 的醋酸溶液恰好能与10mL 的醋酸溶液恰好能与10mL 的NaOH溶液完全反应 的NaOH溶液完全反应 |
您最近一年使用:0次
2023-02-17更新
|
73次组卷
|
2卷引用:山西省阳泉市2022-2023学年高二上学期期末化学试题
名校
解题方法
2 . 下列说法中正确的是
A.某酸性溶液中:Cl-、CH3COO-、Mg2+、SO 能大量共存 能大量共存 |
B.含有大量 的溶液中:NH 的溶液中:NH 、K+、SO 、K+、SO 、OH-能大量共存 、OH-能大量共存 |
C.某透明溶液中:K+、 、 、 、Cl-可能大量共存 、Cl-可能大量共存 |
D.取少量某溶液,向其中加入盐酸酸化的BaCl2溶液,观察到有白色沉淀生成,证明该溶液中含有 |
您最近一年使用:0次
解题方法
3 . 化学小组同学通过实验探究某补铁药品中含亚铁盐,实验过程如下:
(1)甲同学取少量溶液,先加入2滴 溶液,溶液无明显变化;再加入几滴新制氯水,溶液变红。氯水与亚铁盐反应的离子方程式为
溶液,溶液无明显变化;再加入几滴新制氯水,溶液变红。氯水与亚铁盐反应的离子方程式为__________ 。
(2)乙同学也取少量溶液,滴加 溶液,有沉淀生成;将其露置于空气中可观察到的现象是
溶液,有沉淀生成;将其露置于空气中可观察到的现象是__________ ;产生该现象原因是__________ (用化学方程式解释)。
(3)丙同学取少量甲同学实验后的溶液,加入过量铁粉,溶液红色又消失。此实验能证明的是__________ 。
(1)甲同学取少量溶液,先加入2滴
 溶液,溶液无明显变化;再加入几滴新制氯水,溶液变红。氯水与亚铁盐反应的离子方程式为
溶液,溶液无明显变化;再加入几滴新制氯水,溶液变红。氯水与亚铁盐反应的离子方程式为(2)乙同学也取少量溶液,滴加
 溶液,有沉淀生成;将其露置于空气中可观察到的现象是
溶液,有沉淀生成;将其露置于空气中可观察到的现象是(3)丙同学取少量甲同学实验后的溶液,加入过量铁粉,溶液红色又消失。此实验能证明的是
您最近一年使用:0次
解题方法
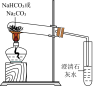
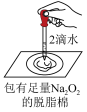
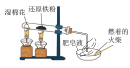
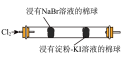
4 . 下列实验中,利用图中装置不能达到实验目的的是
选项 | A | B | C | D |
装置 |
|
|
|
|
目的 | 鉴别碳酸钠和碳酸氢钠 | 证明 与水反应放热 与水反应放热 | 验证铁粉与水蒸气的反应 | 证明氧化性: |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
5 . 下列实验事实不能证明醋酸是弱电解质的是
| A.用醋酸溶液做导电实验时,灯泡很暗 |
B.常温下,测得0.1 醋酸溶液的 醋酸溶液的 |
C.常温下,将 的醋酸溶液稀释1000倍测得 的醋酸溶液稀释1000倍测得 |
| D.等氢离子浓度、等体积的盐酸和醋酸溶液中和碱时,醋酸中和碱的量更多 |
您最近一年使用:0次
2023-11-09更新
|
312次组卷
|
3卷引用:山西省阳泉市第一中学校2023-2024学年高二上学期11月期中考试化学试题
名校
6 . 下列事实不能证明CH3COOH是弱酸的是
| A.CH3COOH溶液能使石蕊溶液变红 |
| B.0.1 mol∙L−1CH3COOH溶液中H+浓度小于0.1 mol∙L−1 |
| C.物质的量浓度相同的CH3COOH溶液的导电能力比盐酸弱 |
| D.0.01 mol∙L−1CH3COOH溶液中有两种分子存在 |
您最近一年使用:0次
2023-08-31更新
|
525次组卷
|
4卷引用:山西省阳泉市第一中学校2022-2023学年高二上学期11月期中考试化学试题
7 . 对下列实验操作和现象的解释或结论正确的是
| 实验操作 | 现象 | 解释或结论 | |
| A | 向盛有10mL0.01mol·L-1AgNO3溶液的试管中滴加1mL0.01mol·L-1NaCl溶液,再向其中滴加1mL0.01mol·L-1KI溶液 | 先产生白色沉淀,后产生黄色沉淀 | 常温下Ksp(AgCl)>Ksp(AgI) |
| B | 向浓盐酸中加入少量碳酸钠溶液,将产生的气体通入苯酚钠溶液 | 苯酚钠溶液中出现白色浑浊 | 可以证明酸性:盐酸>碳酸>苯酚 |
| C | 在酸性KMnO4溶液中通入SO2 | 溶液褪色 | SO2具有漂白性 |
| D | 压缩装有NO2和N2O4混合气体(已达平衡)的容器 | 气体颜色先变深后稍变浅 | 平衡向生成N2O4的方向移动 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
8 . 氮及其化合物是重要的化工原料。回答下列问题:
(1)利用如图所示装置及药品制取氨气。

①A中制取氨气的化学方程式为___________ 。
②C为方框内氨气的收集装置,则a应与___________ (填“b”或“c”)相连。
③证明氨气已集满的操作和现象是___________ 。
(2)若观察到装置D中的烧瓶内产生了红色喷泉。则说明氨气具有的性质是___________ 。
(3)氨经催化氧化可制备硝酸,氨催化氧化的化学方程式为___________ 。
(4) 可用碱液吸收:
可用碱液吸收: (未配平),已知M是一种盐,且在生
(未配平),已知M是一种盐,且在生
成物中M与 的物质的量比为1∶1.则M的化学式为
的物质的量比为1∶1.则M的化学式为___________ 。
(5)NO可在一定条件下,用氨气还原成可直接排入空气中的无毒气体,此反应中氧化剂和还原剂的物质的量之比___________
(1)利用如图所示装置及药品制取氨气。

①A中制取氨气的化学方程式为
②C为方框内氨气的收集装置,则a应与
③证明氨气已集满的操作和现象是
(2)若观察到装置D中的烧瓶内产生了红色喷泉。则说明氨气具有的性质是
(3)氨经催化氧化可制备硝酸,氨催化氧化的化学方程式为
(4)
 可用碱液吸收:
可用碱液吸收: (未配平),已知M是一种盐,且在生
(未配平),已知M是一种盐,且在生成物中M与
 的物质的量比为1∶1.则M的化学式为
的物质的量比为1∶1.则M的化学式为(5)NO可在一定条件下,用氨气还原成可直接排入空气中的无毒气体,此反应中氧化剂和还原剂的物质的量之比
您最近一年使用:0次
解题方法
9 . 下列实验能达到实验目的的是
选项 | 实验内容 | 实验目的 |
A | 将CuCl2·2H2O晶体置于坩埚中加热 | 制备CuCl2固体 |
B | 向FeCl2 溶液中滴加酸性高锰酸钾溶液 | 证明Fe2+具有还原性 |
C | 将Mg、Al分别加入浓NaOH溶液中,观察并比较实验现象 | 比较Mg和Al的金属活动性 |
D | 加热氯化铵和氢氧化钙的混合物,并将产生的气体通过装有碱石灰的干燥管 | 制取氨气并干燥 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
10 . 过氧化氢溶液俗称双氧水,有杀菌消毒的作用,医疗上常用它来清洗伤口,工业上有时也可作为矿业废液消毒剂,有“绿色氧化剂”的美称。某小组设计如下实验探究H2O2的性质:
(1)已知 H2O2的稳定性与溶液pH的关系如图所示(pH越小代表溶液酸性越强)。

①H2O2中氧元素的化合价为_______ ,请写出H2O2分解反应的化学方程式:_______ 。
②根据题中信息可知新配制好的H2O2溶液中需滴入几滴_______ 以保证溶液的稳定性(填“稀硫酸”或“氨水”)。
(2)向硫酸酸化的KMnO4溶液中滴加H2O2溶液,振荡,溶液紫红色褪去并产生大量无色气泡,把带火星的木条靠近试管口木条复燃。已知反应生成了无色的MnSO4溶液,则该反应的氧化产物为_______ ,证明H2O2具有性_______ 性(填“氧化”或“还原”)。
(3)向双氧水中通入H2S气体,有淡黄色S沉淀产生,该反应证明H2O2具有_______ 性(填“氧化”或“还原”)。
(4)下列反应中H2O2表现出来的性质与 中H2O2表现出来的性质相同的是
中H2O2表现出来的性质相同的是_______ 。
A.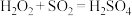
B.
C.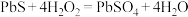
(5)已知I-、Fe2+、SO2、H2O2均有一定的还原性,它们在酸性溶液中还原性的强弱顺序为:SO2>I->H2O2>Fe2+,则下列反应不能发生的是_______。
(1)已知 H2O2的稳定性与溶液pH的关系如图所示(pH越小代表溶液酸性越强)。

①H2O2中氧元素的化合价为
②根据题中信息可知新配制好的H2O2溶液中需滴入几滴
(2)向硫酸酸化的KMnO4溶液中滴加H2O2溶液,振荡,溶液紫红色褪去并产生大量无色气泡,把带火星的木条靠近试管口木条复燃。已知反应生成了无色的MnSO4溶液,则该反应的氧化产物为
(3)向双氧水中通入H2S气体,有淡黄色S沉淀产生,该反应证明H2O2具有
(4)下列反应中H2O2表现出来的性质与
 中H2O2表现出来的性质相同的是
中H2O2表现出来的性质相同的是A.
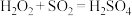
B.

C.
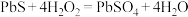
(5)已知I-、Fe2+、SO2、H2O2均有一定的还原性,它们在酸性溶液中还原性的强弱顺序为:SO2>I->H2O2>Fe2+,则下列反应不能发生的是_______。
A. | B. |
C.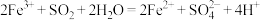 | D.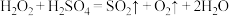 |
您最近一年使用:0次