1 . 下列实验设计、现象和结论都正确的是
| 选项 | 实验操作及现象 | 实验结论 |
| A | 取少量 样品溶于水,加入 样品溶于水,加入 溶液,再加入足量盐酸,产生白色沉淀 溶液,再加入足量盐酸,产生白色沉淀 | 原样品已变质 |
| B | 向某溶液中滴加浓盐酸,将产生气体通入石蕊试液,溶液先变红后褪色 | 溶液中含有 或 或 |
| C | 向溶有 的 的 溶液中通入气体X,出现白色沉淀 溶液中通入气体X,出现白色沉淀 | 气体X不一定是氧化性气体 |
| D | 在某固体试样加水后的溶液中,滴加 溶液,没有产生使湿润红色石蕊试纸变蓝的气体 溶液,没有产生使湿润红色石蕊试纸变蓝的气体 | 该固体试样中不可能存在 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-09-23更新
|
1948次组卷
|
10卷引用:吉林省长春市东北师范大学附属中学2023-2024学年高三上学期9月一模化学试题
吉林省长春市东北师范大学附属中学2023-2024学年高三上学期9月一模化学试题吉林省延边第一中学2023-2024学年高三上学期第二次模考化学试题吉林省通化市梅河口市第五中学2023-2024学年高三上学期1月期末化学试题河南省兰考县第一高级中学2023-2024学年高二上学期期中考试化学试题(已下线)题型03 离子方程式正误判断 离子共存、检验和推断-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)辽宁省沈阳市东北育才学校科学高中部2023-2024学年高三第三次模拟考试 化学试题(已下线)专题03 化学实验基础-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)(已下线)通关练03 常考化学实验基础知识-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)(已下线)压轴题01?离子方程式与离子共存的判断(5大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)(已下线)第03讲 离子共存、离子的检验与推断(讲义)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)
名校
解题方法
2 . 根据实验操作和现象,不能得出相应结论的是
A.等体积、 的两种酸 的两种酸 和 和 ,分别与足量的 ,分别与足量的 反应,酸 反应,酸 放出的氢气多,则酸性: 放出的氢气多,则酸性: |
B.将 样品溶于稀硫酸,滴加 样品溶于稀硫酸,滴加 溶液,溶液变红,则 溶液,溶液变红,则 样品溶于稀硫酸前已氧化变质 样品溶于稀硫酸前已氧化变质 |
C.将充满 的密闭玻璃球没泡在热水中,气体红棕色加深,则 的密闭玻璃球没泡在热水中,气体红棕色加深,则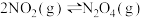 , , |
D.向含有酚酞的 溶液中加入少量 溶液中加入少量 固体,有白色沉淀生成,溶液红色变浅,则纯碱溶液呈碱性是由 固体,有白色沉淀生成,溶液红色变浅,则纯碱溶液呈碱性是由 水解引起的 水解引起的 |
您最近一年使用:0次
2021-11-17更新
|
321次组卷
|
3卷引用:吉林省乾安县第七中学2021-2022学年高二上学期第三次质量检测化学试题
解题方法
3 .  是一种黄色油状液体,熔点
是一种黄色油状液体,熔点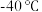 ,沸点
,沸点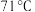 ,不溶于冷水,常温下密度为
,不溶于冷水,常温下密度为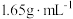 。
。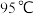 以上爆炸,弱酸性环境稳定,中性水中易发生水解。常用于面粉的漂白和杀菌。实验室可用
以上爆炸,弱酸性环境稳定,中性水中易发生水解。常用于面粉的漂白和杀菌。实验室可用 和
和 溶液在常温下反应制取,所用装置如下:
溶液在常温下反应制取,所用装置如下:
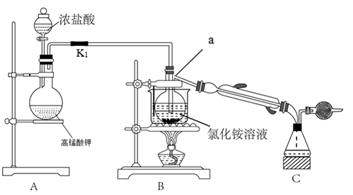
回答下列问题:
(1) 的分子构型为
的分子构型为___________ 。
(2)仪器a的名称为___________ ;实验室利用装置A还可以制备下列哪些物质___________ (填字母)。
a、乙炔b、硝基苯c、溴苯d、乙酸乙酯
(3)打开活塞 ,将浓盐酸滴入圆底烧瓶中,仪器a中制备
,将浓盐酸滴入圆底烧瓶中,仪器a中制备 的化学反应方程式为
的化学反应方程式为___________ ,待反应至仪器a中有大量油状液体生成,关闭活塞 。将产物分离并用无水
。将产物分离并用无水 干燥后,利用B、C装置将
干燥后,利用B、C装置将 提纯,提纯过程中水浴温度应控制在
提纯,提纯过程中水浴温度应控制在___________ 。
(4)将提纯后的 滴入含有紫色石蕊试剂的水中,溶液先变蓝后褪色,产生该现象的原因是
滴入含有紫色石蕊试剂的水中,溶液先变蓝后褪色,产生该现象的原因是___________ (使用化学用语结合文字解释)。
(5)液氯储罐中常混有 。为测定氯气中的
。为测定氯气中的 含量,将一定量样品先通入足量含有氧化汞的浓盐酸溶液中(反应为:
含量,将一定量样品先通入足量含有氧化汞的浓盐酸溶液中(反应为: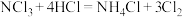 ),产生的气体通过饱和食盐水后再用足量
),产生的气体通过饱和食盐水后再用足量 溶液吸收,测得吸收后
溶液吸收,测得吸收后 溶液增重
溶液增重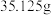 。经测定
。经测定 吸收管内
吸收管内 质量为
质量为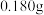 。该样品中
。该样品中 的质量分数为
的质量分数为___________ %(保留三位有效数字);若产生的气体未通过饱和食盐水,则测定结果___________ (填“偏高”“偏低”或“无影响”)。
 是一种黄色油状液体,熔点
是一种黄色油状液体,熔点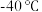 ,沸点
,沸点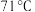 ,不溶于冷水,常温下密度为
,不溶于冷水,常温下密度为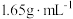 。
。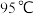 以上爆炸,弱酸性环境稳定,中性水中易发生水解。常用于面粉的漂白和杀菌。实验室可用
以上爆炸,弱酸性环境稳定,中性水中易发生水解。常用于面粉的漂白和杀菌。实验室可用 和
和 溶液在常温下反应制取,所用装置如下:
溶液在常温下反应制取,所用装置如下:
回答下列问题:
(1)
 的分子构型为
的分子构型为(2)仪器a的名称为
a、乙炔b、硝基苯c、溴苯d、乙酸乙酯
(3)打开活塞
 ,将浓盐酸滴入圆底烧瓶中,仪器a中制备
,将浓盐酸滴入圆底烧瓶中,仪器a中制备 的化学反应方程式为
的化学反应方程式为 。将产物分离并用无水
。将产物分离并用无水 干燥后,利用B、C装置将
干燥后,利用B、C装置将 提纯,提纯过程中水浴温度应控制在
提纯,提纯过程中水浴温度应控制在(4)将提纯后的
 滴入含有紫色石蕊试剂的水中,溶液先变蓝后褪色,产生该现象的原因是
滴入含有紫色石蕊试剂的水中,溶液先变蓝后褪色,产生该现象的原因是(5)液氯储罐中常混有
 。为测定氯气中的
。为测定氯气中的 含量,将一定量样品先通入足量含有氧化汞的浓盐酸溶液中(反应为:
含量,将一定量样品先通入足量含有氧化汞的浓盐酸溶液中(反应为: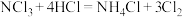 ),产生的气体通过饱和食盐水后再用足量
),产生的气体通过饱和食盐水后再用足量 溶液吸收,测得吸收后
溶液吸收,测得吸收后 溶液增重
溶液增重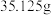 。经测定
。经测定 吸收管内
吸收管内 质量为
质量为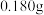 。该样品中
。该样品中 的质量分数为
的质量分数为
您最近一年使用:0次
名校
解题方法
4 . 某实验课题小组的同学在实验室利用新制备的硫酸亚铁溶液制备硫酸亚铁铵(俗名为莫尔盐)[(NH4)2SO4·FeSO4·6H2O](相对分子质量为392),该晶体比一般亚铁盐稳定,易溶于水,不溶于乙醇。
(一)制备硫酸亚铁溶液(实验步骤如图所示)
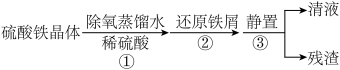
(1)步骤①,加入稀硫酸的目的是_____ 。
(2)步骤②,加入还原铁屑后观察到的现象是___ 。实验前,常用碱溶液洗涤铁屑,其目的是__ 。
(二)制备莫尔盐(硫酸亚铁铵)
(3)在FeSO4溶液中加入稍过量的硫酸铵饱和溶液。从溶液中提取(NH4)2SO4·FeSO4·6H2O的具体操作是____ 、用乙醇洗涤、干燥。
(三)检验莫尔盐加热时的分解产物
莫尔盐受热分解,甲同学认为分解产物可能有以下几种情况:
a. Fe2O3、SO3、NH3、H2O b. FeO、NH3、SO3、H2O
c. FeO、SO2、NH3、H2O d. Fe2O3、NH3、SO2、SO3、H2O
(4)经认真分析,推理即可确定猜想_______ (填序号)不成立。
(5)乙同学认为莫尔盐分解的产物中可能含有SO3(g)、SO2(g)及N2(g)。为验证产物的存在,乙同学用下列装置进行实验:

①乙同学的实验中,装置依次连接的合理顺序为A→H→_____ →G 。
②证明分解产物中含有SO3的实验现象是_____ 。
(四)测定实验(二)所得晶体中(NH4)2SO4·FeSO4·6H2O的纯度
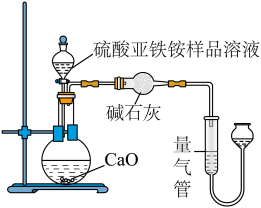
称取m g硫酸亚铁铵样品配制成500 mL溶液,取20.00 mL样品溶液进行实验,装置如图所示。
(6)若实验测得NH3的体积为V L(已折算为标准状况下),则该硫酸亚铁铵样品的纯度为____ (列出计算式即可)。
(一)制备硫酸亚铁溶液(实验步骤如图所示)

(1)步骤①,加入稀硫酸的目的是
(2)步骤②,加入还原铁屑后观察到的现象是
(二)制备莫尔盐(硫酸亚铁铵)
(3)在FeSO4溶液中加入稍过量的硫酸铵饱和溶液。从溶液中提取(NH4)2SO4·FeSO4·6H2O的具体操作是
(三)检验莫尔盐加热时的分解产物
莫尔盐受热分解,甲同学认为分解产物可能有以下几种情况:
a. Fe2O3、SO3、NH3、H2O b. FeO、NH3、SO3、H2O
c. FeO、SO2、NH3、H2O d. Fe2O3、NH3、SO2、SO3、H2O
(4)经认真分析,推理即可确定猜想
(5)乙同学认为莫尔盐分解的产物中可能含有SO3(g)、SO2(g)及N2(g)。为验证产物的存在,乙同学用下列装置进行实验:

①乙同学的实验中,装置依次连接的合理顺序为A→H→
②证明分解产物中含有SO3的实验现象是
(四)测定实验(二)所得晶体中(NH4)2SO4·FeSO4·6H2O的纯度
称取m g硫酸亚铁铵样品配制成500 mL溶液,取20.00 mL样品溶液进行实验,装置如图所示。
(6)若实验测得NH3的体积为V L(已折算为标准状况下),则该硫酸亚铁铵样品的纯度为

您最近一年使用:0次



