名校
解题方法
1 . 利用Heck反应合成一种药物中间体需要经历如图反应过程。下列有关说法错误的是
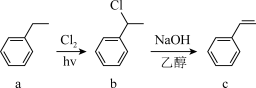

| A.a、b、c中只有a是苯的同系物 |
| B.c既可发生氧化反应,也可发生聚合反应 |
| C.a、b、c中所有碳原子均有可能共面 |
| D.向反应b→c所得混合物中滴入AgNO3溶液,可证明b中是否含有氯元素 |
您最近一年使用:0次
名校
解题方法
2 . 对于H2O2分解反应,Cu2+也有一定的催化作用。为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。下列说法不正确的是


| A.图甲可通过观察气泡产生快慢来比较反应速率的大小 |
| B.图甲所示实验中,若左边试管里的反应速率大于右边的,则证明Fe3+对H2O2分解的催化效果比Cu2+的好 |
| C.用图乙装置测定反应速率,可测定反应产生的气体体积及反应时间 |
| D.为检查乙装置的气密性,可关闭a处旋塞,将注射器活塞拉出一定距离,一段时间后松开活塞,观察活塞是否回到原位 |
您最近一年使用:0次
2021-10-10更新
|
282次组卷
|
7卷引用:河南省焦作市博爱县第一中学2023-2024学年高二上学期10月月考化学试题
3 . 某化学兴趣小组设计如下两个实验证明:①氧化性:Fe3+>I2,②反应2Fe3++2I-=2Fe2++I2为可逆反应,下列说法中错误的是
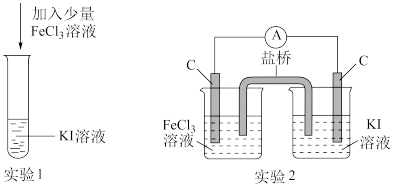

| A.实验1试管中加入淀粉后溶液变蓝,该条件下氧化性:Fe3+>I2 |
| B.实验2中最后电流表指针不再偏转可证明上述反应为可逆反应 |
| C.实验1反应结束后,向试管中加入KSCN能判断该反应是否为可逆反应 |
| D.实验2电流表指针不再偏转时,向右侧烧杯中加入单质碘可判断该反应是否为可逆反应 |
您最近一年使用:0次
2014高三·全国·专题练习
名校
解题方法
4 . 如图,在注射器中加入少量 晶体,并吸入少量浓硫酸(以不接触纸条为准)。则下列有关说法正确的是
晶体,并吸入少量浓硫酸(以不接触纸条为准)。则下列有关说法正确的是
 晶体,并吸入少量浓硫酸(以不接触纸条为准)。则下列有关说法正确的是
晶体,并吸入少量浓硫酸(以不接触纸条为准)。则下列有关说法正确的是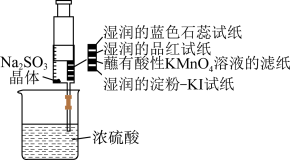
| A.蓝色石蕊试纸先变红后褪色 |
B.品红试纸、蘸有酸性 溶液的滤纸均褪色,证明 溶液的滤纸均褪色,证明 具有漂白性 具有漂白性 |
C.湿润的淀粉 试纸未变蓝说明 试纸未变蓝说明 的氧化性弱于 的氧化性弱于 |
D.饱和NaCl溶液可用于除去实验中多余的 |
您最近一年使用:0次
2020-10-07更新
|
909次组卷
|
36卷引用:河南省焦作市温县第一高级中学2022-2023学年高二上学期期末考试化学试题
河南省焦作市温县第一高级中学2022-2023学年高二上学期期末考试化学试题(已下线)2014年高考化学鲁科版3.3硫的转化练习卷山东省济南第一中学2017-2018学年高一上学期期末考试化学试题江西省南昌市第二中学2017-2018学年高一上学期期末考试化学试题湖南省石门县第一中学2016-2017学年高一下学期期末考试化学试题(已下线)2018年11月27日 《每日一题》人教必修1-二氧化硫和三氧化硫、二氧化碳的性质与比较【校级联考】天津市静海区2019届高三上学期三校联考化学试题(已下线)2019年11月26日 《每日一题》人教版(必修1)——二氧化硫和三氧化硫、二氧化碳的性质与比较2019-2020学年高一上学期期末复习《新题速递·化学》12月(考点15-20)安徽省淮北市第一中学2019-2020学年高一下学期《硫及其化合物的性质》 跟进作业 (第三课时)(已下线)【新东方】2020-80.(已下线)专题01 硫及其化合物(核心素养卷)-【新教材精创】2019-2020学年高一化学新教材知识讲学(必修第二册)福建省龙海市第二中学2019-2020学年高一下学期4月月考化学试题江西省南昌市八一中学2019-2020学年高一下学期期中考试化学试题(已下线)3.2.1 自然界中的硫 二氧化硫练习(1)——《高中新教材同步备课》(鲁科版 必修第一册)山东省山东师范大学附属中学2019-2020学年高一上学期12月份月考化学试题黑龙江省大兴安岭漠河县第一中学2019-2020学年高二下学期第二次月考化学试卷苏教版(2020)高一必修第一册专题4第一单元课时1 硫、二氧化硫和三氧化硫(已下线)第3章 总结与检测(1)——《高中新教材同步备课》(鲁科版 必修第一册)鲁科版(2019)高一必修第一册第3章 物质的性质与转化 第2节 硫的转化 课时1 硫、二氧化硫和三氧化硫河北省衡水市阜城中学2019-2020学年高一上学期期末考试化学试题高一必修第二册(人教2019版)第五章 第一节 硫及其化合物 课时1 硫和二氧化硫高一必修第一册(苏教2019版)专题4 B 素养拓展区 过素养 学科素养拓展训练(已下线)第三单元 物质的性质与转化(能力提升)-2020-2021学年高一化学必修第一册单元测试定心卷 (鲁科版2019)专题4 第二单元 综合拔高练-高中化学苏教2019版必修第一册安徽省六安市舒城育才学校2020-2021学年高一3月月考化学试题黑龙江省哈尔滨市阿城区龙涤中学2020-2021学年高一4月月考化学试题黑龙江省哈尔滨市第一六二中学校2020-2021学年高一下学期4月月考化学试题河北承德第一中学2020-2021学年高二下学期第三次月考化学试题山西省太原市第五中学2021-2022学年高一下学期4月阶段性检测化学试题安徽省滁州市定远县民族中学2021-2022学年高一下学期期中考试化学试题湖北省竹溪县第二高级中学2021-2022学年高一下学期第一次月考化学试题广东省肇庆市高要区第一中学2022-2023学年高三下学期模拟考试(二)化学试题四川省达州市万源中学2023-2024学年高二上学期10月月考化学试题北京市育英学校2023-2024学年高一上学期期末考试化学试题北京市第二十二中学2023-2024学年高一下学期阶段测试化学试题
5 . 某学习小组设计的蔗糖水解反应如图所示(夹持装置省略)。下列说法错误的是( )
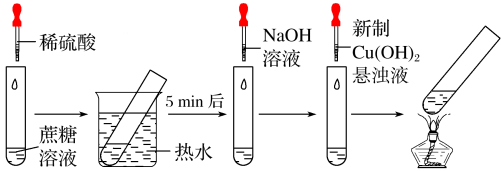

| A.稀硫酸和热水浴都能加快蔗糖水解速率 |
| B.滴加NaOH溶液的目的是调溶液的pH至碱性 |
| C.加热至沸腾后试管内生成黑色沉淀 |
| D.实验现象证明蔗糖水解有还原性物质生成 |
您最近一年使用:0次
2020-06-01更新
|
660次组卷
|
16卷引用:河南省焦作市博爱县第一中学2022-2023学年高三下学期5月月考化学试题
河南省焦作市博爱县第一中学2022-2023学年高三下学期5月月考化学试题四川省宜宾市普通高中2020届高三高考适应性考试(三诊)理综-化学试题四川省攀枝花市第十五中学校2019-2020学年高二期末模拟考试化学试卷湖南省长沙县第九中学2019-2020学年高二下学期期末检测化学试题(已下线)4.2 糖类(B级能力练)-2020-2021学年高二化学章节分层检测ABC(人教版选修5)江西省抚州市南城一中2020-2021学年高二下学期期中联考化学试题(已下线)考向31 生命中的的基础化学物质 有机合成高分子-备战2022年高考化学一轮复习考点微专题专题6 生命活动的物质基础——糖类、油脂、蛋白质 第一单元 糖类和油脂 第1课时 糖类第四章 本章复习提升山东省菏泽市单县第二中学2021-2022学年高二下学期四月月考化学试题(已下线)易错点30 大分子和高分子-备战2023年高考化学考试易错题(已下线)第一部分 二轮专题突破 专题19 有机选择题题型分析(已下线)第九章 有机化学基础 必做实验提升(七) 有机化合物中常见官能团的检验6.1.1糖类 课后黑龙江省双鸭山市第一中学2022-2023学年高二下学期期末考试化学试题(已下线)第四章 生物大分子(B卷)
名校
6 . 已知:Ag++SCN-=AgSCN↓(白色),某同学探究AgSCN的溶解平衡及转化,进行以下实验。不正确 的是

| A.①中现象能说明Ag+与SCN-生成AgSCN沉淀的反应有限度 |
| B.②中现象产生的原因是发生了反应Fe(SCN)3 +3Ag+ =3AgSCN↓+Fe3+ |
| C.③中产生黄色沉淀的现象能证明AgI的溶解度比AgSCN的溶解度小 |
| D.④中黄色沉淀溶解的原因可能是AgI与KI溶液中的I-进一步发生了反应 |
您最近一年使用:0次
2019-01-29更新
|
1123次组卷
|
12卷引用:河南省焦作市温县第一高级中学2021-2022学年高二下学期2月月考化学试题
河南省焦作市温县第一高级中学2021-2022学年高二下学期2月月考化学试题【市级联考】四川省攀枝花市2018-2019学年高二上学期期末教学质量监测化学试题【区级联考】北京市房山区2019届高三下学期二模考试化学试题【区级联考】北京市房山区2019届高三下学期高考第二次模拟测试理科综合化学试题(已下线)2019年11月17日《每日一题》人教版(选修4)—— 每周一测湖北省武汉市武昌区武汉中学2019-2020学年高二上学期化学(人教版选修4)期末复习试题:专题11 难溶电解质溶解平衡的应用复习题北京市朝阳区2020届高三4月(一模)适应性试卷练习安徽省太和第一中学2020-2021学年高二上学期期中考试化学(普通班)试题北京市海淀区中关村中学2022届高三下学期三模化学试题北京市顺义牛栏山第一中学2023-2024学年高二上学期期中考试化学试题北京市第八中学2023-2024学年高三上学期12月月考化学试题北京师范大学附属中学2023-2024学年高三下学期统练 化学试题
7 . 向胶体中加入电解质能使胶体发生聚沉。使一定量的胶体在一定时间内开始聚沉所需电解质的浓度称作“聚沉值”,电解质的“聚沉值”越小其凝聚力越大;实验证明,凝聚力主要取决于和胶粒带相反电荷的离子所带的电荷数。某胶体遇氯化镁溶液或石膏水易发生聚沉,而遇食盐水或Na2SO4溶液不易发生聚沉,则下列有关说法正确的是
| A.Na+使此胶体发生聚沉的“聚沉值”等于Ca2+、Mg2+ |
| B.该胶体分散质微粒带正电荷 |
| C.该胶体遇氯化钡溶液或Fe(OH)3胶体可发生聚沉 |
| D.该胶体的微粒直径为10-7cm~10-9cm |
您最近一年使用:0次
2017-10-27更新
|
324次组卷
|
4卷引用:河南省焦作市沁阳一中2022-2023学年高一上学期第一次质量检测化学试题
河南省焦作市沁阳一中2022-2023学年高一上学期第一次质量检测化学试题江西省玉山县第一中学2018届高三上学期第一次月考化学试题【全国百强校】辽宁省沈阳市东北育才学校2019届高三上学期联合考试化学试题(已下线)第2单元 物质的组成分类与性质(B卷 滚动提升检测)-2021年高考化学一轮复习单元滚动双测卷
名校
解题方法
8 . 还原铁粉与水蒸气的反应装置如图所示。取少量反应后的固体加入稀硫酸使其完全溶解得溶液a;另取少量反应后的固体加入稀硝酸使其完全溶解,得溶液b.下列说法正确的是
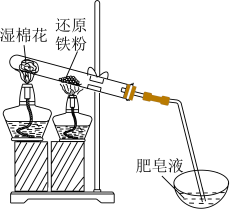
A.铁与水蒸气反应: |
B.肥皂液中产生气泡,不能证明铁与水蒸气反应生成 |
C.向溶液a中滴加 溶液,出现蓝色沉淀,说明铁粉未完全反应 溶液,出现蓝色沉淀,说明铁粉未完全反应 |
D.向溶液b中滴加 溶液,溶液变红,证实了固体中含有 溶液,溶液变红,证实了固体中含有 |
您最近一年使用:0次
2024-04-10更新
|
1090次组卷
|
6卷引用:2024届河南省焦作市博爱县第一中学高三下学期三模化学试题
2024届河南省焦作市博爱县第一中学高三下学期三模化学试题北京市西城区2024届高三统一测试(一模)化学试题(已下线)题型6 元素及其化合物 化学实验基础(25题)-2024年高考化学常考点必杀300题(新高考通用)(已下线)化学(北京卷03)-2024年高考押题预测卷(已下线)2024年东北三省四校高三下学期第四次模拟考试化学试卷东北三省三校2023-2024学年高三四模化学试卷
名校
9 . H2O2是一种绿色氧化还原试剂,在化学研究中应用广泛。某研究性学习小组设计如图所示实验装置,探究影响H2O2分解反应速率的因素。
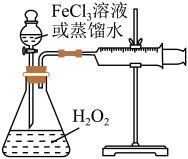
(1)①写出锥形瓶中反应的化学方程式________ 。
②设计实验方案:在不同条件下,测定_______ 。(要求所测得的数据能直接体现反应速率大小)
(2)探究影响H2O2分解反应速率的因素实验方案如下表所示,先向锥形瓶中加入质量分数为10%H2O2,再依次通过分液漏斗向锥形瓶中加入一定量的蒸馏水和FeCl3溶液,请回答问题:
①表格中a=_______ ,b=________ 。
②通过实验Ⅱ和Ⅲ探究浓度对反应速率影响。
(3)实验Ⅱ、Ⅲ中溶液颜色变深的原因是________ 。
(4)已知FeCl3溶液对H2O2的催化分解分为反应i和反应ii两步进行:
已知反应ii的离子方程式为:2Fe2++2H++H2O2=2Fe3++2H2O;
①反应i离子方程式为_______ 。
②某同学设计实验证明催化过程中有Fe2+产生:取2mLH2O2溶液于试管中,向试管中滴加2滴FeCl3溶液,再滴加2滴_______ 溶液,产生蓝色沉淀。
(5)向实验Ⅱ中反应后的溶液滴加KSCN溶液,溶液变红色,2min后溶液红色褪去;继续滴加KSCN溶液,溶液又变红色,一段时间后又褪色;此时再向溶液中滴加盐酸酸化后的BaCl2溶液,产生白色沉淀。请分析溶液红色褪去的原因______ 。

(1)①写出锥形瓶中反应的化学方程式
②设计实验方案:在不同条件下,测定
(2)探究影响H2O2分解反应速率的因素实验方案如下表所示,先向锥形瓶中加入质量分数为10%H2O2,再依次通过分液漏斗向锥形瓶中加入一定量的蒸馏水和FeCl3溶液,请回答问题:
| 实验序号 | 10%H2O2/mL | 蒸馏水/mL | 0.2mol·LFeCl3溶液/mL | 现象 |
| I | 10 | a | 0 | 无明显变化 |
| Ⅱ | 10 | b | 2 | 锥形瓶变热,溶液迅速变红棕色,并有较多气泡产生;2min时,反应变缓,溶液颜色明显变浅 |
| Ⅲ | 5 | 5 | 2 | 锥形瓶变热,溶液变棕色,开始5s后产生较少的气泡;2min时,反应速度加快 |
②通过实验Ⅱ和Ⅲ探究浓度对反应速率影响。
(3)实验Ⅱ、Ⅲ中溶液颜色变深的原因是
(4)已知FeCl3溶液对H2O2的催化分解分为反应i和反应ii两步进行:
已知反应ii的离子方程式为:2Fe2++2H++H2O2=2Fe3++2H2O;
①反应i离子方程式为
②某同学设计实验证明催化过程中有Fe2+产生:取2mLH2O2溶液于试管中,向试管中滴加2滴FeCl3溶液,再滴加2滴
(5)向实验Ⅱ中反应后的溶液滴加KSCN溶液,溶液变红色,2min后溶液红色褪去;继续滴加KSCN溶液,溶液又变红色,一段时间后又褪色;此时再向溶液中滴加盐酸酸化后的BaCl2溶液,产生白色沉淀。请分析溶液红色褪去的原因
您最近一年使用:0次
名校
解题方法
10 . 下列实验装置或实验方法不能达到实验目的的是




| A.装置①用于比较碳酸钠和碳酸氢钠的热稳定性 |
| B.装置②用于验证钠和水反应是否放热 |
| C.装置③为闻气体气味的方法 |
| D.装置④用于证明C12没有漂白性,HC1O有漂白性 |
您最近一年使用:0次
2023-11-06更新
|
280次组卷
|
2卷引用:河南省焦作市博爱县第一中学2023-2024学年高一上学期11月期中考试化学试题



