名校
解题方法
1 . 某处工厂排出的烟道气中含氮氧化物(主要为NO、 )、粉尘和少量水蒸气.课外兴趣活动小组对该工厂排出的烟道气进行处理,并检测其氮氧化物含量,实验装置如图:
)、粉尘和少量水蒸气.课外兴趣活动小组对该工厂排出的烟道气进行处理,并检测其氮氧化物含量,实验装置如图: 混合气体按一定比例被
混合气体按一定比例被 溶液完全吸收生成
溶液完全吸收生成 和
和 ,写出该反应的化学方程式
,写出该反应的化学方程式______________ ;若反应后尾气无残留,则参加反应的 、NO物质的量比值为
、NO物质的量比值为_____ (填字母)。
a.≥1 b.≤1 c.任意值
(2)可使用适量酸性 溶液,将溶液中的
溶液,将溶液中的 全部氧化为
全部氧化为 ,发生反应的离子方程式是
,发生反应的离子方程式是_______________ 。
(3)气囊用来储存处理后气体,其中可能含少量NO气体,可用酸性 溶液来处理。
溶液来处理。 氧化NO生成
氧化NO生成 和
和 ,发生反应的离子方程式是
,发生反应的离子方程式是_______________ 。
(4)有氧条件下,NO在催化剂作用下可被 还原为
还原为 。在钒基催化剂
。在钒基催化剂 作用下的脱硝反应机理如图所示:
作用下的脱硝反应机理如图所示: 在有氧条件下的总化学方程式是
在有氧条件下的总化学方程式是___________ 。
(5)羟基自由基( )也可以用于脱硫脱硝。如图表示光催化氧化技术可生成
)也可以用于脱硫脱硝。如图表示光催化氧化技术可生成 ﹔光照时,价带失去电子产生有强氧化性的空穴,价带上
﹔光照时,价带失去电子产生有强氧化性的空穴,价带上 直接转化为
直接转化为 ;描述产生
;描述产生 的另一种过程:
的另一种过程:______________ 。 等杂质,可以采用
等杂质,可以采用 测定含量。称取
测定含量。称取 该亚硝酸钠产品溶于水配制成
该亚硝酸钠产品溶于水配制成 的样品溶液。取
的样品溶液。取 该样品溶液于锥形瓶中,用稀
该样品溶液于锥形瓶中,用稀 酸化后,再向锥形瓶中滴加
酸化后,再向锥形瓶中滴加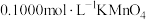 溶液,至恰好完全反应时,消耗
溶液,至恰好完全反应时,消耗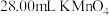 溶液。计算该产品中
溶液。计算该产品中 的质量分数
的质量分数__________ 。(写出计算过程)
 )、粉尘和少量水蒸气.课外兴趣活动小组对该工厂排出的烟道气进行处理,并检测其氮氧化物含量,实验装置如图:
)、粉尘和少量水蒸气.课外兴趣活动小组对该工厂排出的烟道气进行处理,并检测其氮氧化物含量,实验装置如图: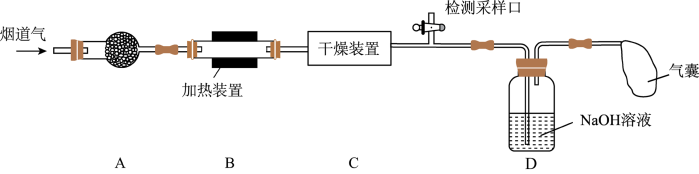
 混合气体按一定比例被
混合气体按一定比例被 溶液完全吸收生成
溶液完全吸收生成 和
和 ,写出该反应的化学方程式
,写出该反应的化学方程式 、NO物质的量比值为
、NO物质的量比值为a.≥1 b.≤1 c.任意值
(2)可使用适量酸性
 溶液,将溶液中的
溶液,将溶液中的 全部氧化为
全部氧化为 ,发生反应的离子方程式是
,发生反应的离子方程式是(3)气囊用来储存处理后气体,其中可能含少量NO气体,可用酸性
 溶液来处理。
溶液来处理。 氧化NO生成
氧化NO生成 和
和 ,发生反应的离子方程式是
,发生反应的离子方程式是(4)有氧条件下,NO在催化剂作用下可被
 还原为
还原为 。在钒基催化剂
。在钒基催化剂 作用下的脱硝反应机理如图所示:
作用下的脱硝反应机理如图所示: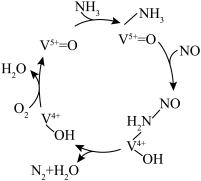
 在有氧条件下的总化学方程式是
在有氧条件下的总化学方程式是(5)羟基自由基(
 )也可以用于脱硫脱硝。如图表示光催化氧化技术可生成
)也可以用于脱硫脱硝。如图表示光催化氧化技术可生成 ﹔光照时,价带失去电子产生有强氧化性的空穴,价带上
﹔光照时,价带失去电子产生有强氧化性的空穴,价带上 直接转化为
直接转化为 ;描述产生
;描述产生 的另一种过程:
的另一种过程: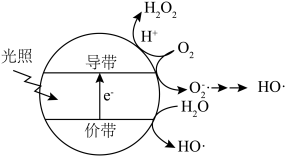
 等杂质,可以采用
等杂质,可以采用 测定含量。称取
测定含量。称取 该亚硝酸钠产品溶于水配制成
该亚硝酸钠产品溶于水配制成 的样品溶液。取
的样品溶液。取 该样品溶液于锥形瓶中,用稀
该样品溶液于锥形瓶中,用稀 酸化后,再向锥形瓶中滴加
酸化后,再向锥形瓶中滴加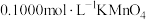 溶液,至恰好完全反应时,消耗
溶液,至恰好完全反应时,消耗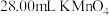 溶液。计算该产品中
溶液。计算该产品中 的质量分数
的质量分数
您最近一年使用:0次
2024-05-03更新
|
256次组卷
|
3卷引用:河南省焦作市博爱县第一中学2023-2024学年高一下学期4月期中考试化学试题
名校
2 . 钠及其化合物在生产、生活中有着重要的用途,根据所学知识,回答下列问题。
Ⅰ.某汽车安全气囊的产气药剂主要含有 等物质。 当汽车发生碰撞时,NaN3迅速分解产生N2和 Na,同时放出大量的热,
等物质。 当汽车发生碰撞时,NaN3迅速分解产生N2和 Na,同时放出大量的热, 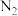 使气囊迅速膨胀,从而起到保护作用。
使气囊迅速膨胀,从而起到保护作用。
(1)KClO4 可处理产生的Na,KClO4中氯元素的化合价为_______ 。
(2) 是冷却剂,吸收产气过程中释放的热量而分解,其分解的化学方程式为
是冷却剂,吸收产气过程中释放的热量而分解,其分解的化学方程式为_______ 。
Ⅱ.某实验小组设计如下实验方案测定 与
与 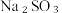 混合物中各组分的含量。
混合物中各组分的含量。
(3)方案一:称取30g样品,置于坩埚中加热至恒重,冷却、称量,剩余固体质量为31.6g,计算。
①实验中加热至恒重的目的是_______ 。
②样品中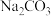 的质量分数为
的质量分数为_______ 。
(4)方案二:用如图所示装置(铁架台、铁夹等仪器未在图中画出)进行实验。

①装置C的作用是_______ ;装置F的作用是_______
②实验过程中,当装置A内的固体反应完全后,需打开活塞K,向 A 中通入大量的氮气。这样做的目的是_______ 。
(5)方案三:称取一定量样品,置于小烧杯中,加适量水溶解,向小烧杯中加入足量。 溶液。过滤、洗涤、干燥沉淀,称量固体质量。实验中判断沉淀洗涤干净的方法是
溶液。过滤、洗涤、干燥沉淀,称量固体质量。实验中判断沉淀洗涤干净的方法是_______ 。
Ⅰ.某汽车安全气囊的产气药剂主要含有
 等物质。 当汽车发生碰撞时,NaN3迅速分解产生N2和 Na,同时放出大量的热,
等物质。 当汽车发生碰撞时,NaN3迅速分解产生N2和 Na,同时放出大量的热, 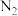 使气囊迅速膨胀,从而起到保护作用。
使气囊迅速膨胀,从而起到保护作用。(1)KClO4 可处理产生的Na,KClO4中氯元素的化合价为
(2)
 是冷却剂,吸收产气过程中释放的热量而分解,其分解的化学方程式为
是冷却剂,吸收产气过程中释放的热量而分解,其分解的化学方程式为Ⅱ.某实验小组设计如下实验方案测定
 与
与 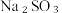 混合物中各组分的含量。
混合物中各组分的含量。(3)方案一:称取30g样品,置于坩埚中加热至恒重,冷却、称量,剩余固体质量为31.6g,计算。
①实验中加热至恒重的目的是
②样品中
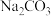 的质量分数为
的质量分数为(4)方案二:用如图所示装置(铁架台、铁夹等仪器未在图中画出)进行实验。

①装置C的作用是
②实验过程中,当装置A内的固体反应完全后,需打开活塞K,向 A 中通入大量的氮气。这样做的目的是
(5)方案三:称取一定量样品,置于小烧杯中,加适量水溶解,向小烧杯中加入足量。
 溶液。过滤、洗涤、干燥沉淀,称量固体质量。实验中判断沉淀洗涤干净的方法是
溶液。过滤、洗涤、干燥沉淀,称量固体质量。实验中判断沉淀洗涤干净的方法是
您最近一年使用:0次
2023-10-31更新
|
136次组卷
|
3卷引用:河南省焦作市博爱县第一中学2023-2024学年高一上学期11月期中考试化学试题
2023·全国·模拟预测
名校
解题方法
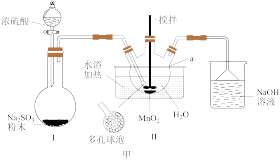
3 . MnSO4·H2O是一种浅粉色晶体,易溶于水,不溶于乙醇,是饲料中常用的添加剂,也是电解制备锰及其他锰盐的原料,工业用途广泛。某同学设计如图甲所示实验装置制备硫酸锰。
回答下列问题:
(1)仪器a的名称是_____ 。连接好实验仪器,装药品之前需进行的操作是______ 。
(2)装置Ⅱ中发生反应的化学方程式为_____ ;装置Ⅱ中水浴温度控制在80℃左右,温度过高时反应速率可能减慢的原因是______ 。
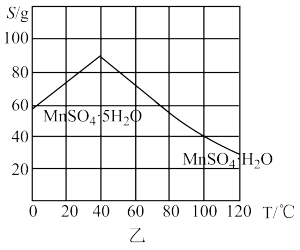
(3)结合图乙,分析反应后从溶液中获得MnSO4·H2O晶体的操作为_____ 、酒精洗涤、低温干燥。
(4)测定饲料中硫酸锰的含量常将饲料溶于水,以磷酸作络合剂,用硝酸铵作氧化剂,将试样中的二价锰定量氧化成三价锰,过量的硝酸铵立即与产生的亚硝酸盐反应而消除其影响。然后加入指示剂,用硫酸亚铁铵[Fe(NH4)2(SO4)2]标准溶液滴定生成的三价锰,溶液由红色变为亮黄色为滴定终点。有关反应的离子方程式如下:
①2Mn2++NO +4PO
+4PO +2H+=2[Mn(PO4)2]3-+NO
+2H+=2[Mn(PO4)2]3-+NO +H2O;
+H2O;
②NH +NO
+NO =N2↓+2H2O;
=N2↓+2H2O;
③[Mn(PO4)2]3-+Fe2+=Mn2++[Fe(PO4)2]3-。
取ag饲料,消耗浓度为cmol•L-1的硫酸亚铁铵标准溶液VmL,则饲料中MnSO4·H2O的质量分数为_____ %(用含a、c、V的式子表示)。若实验时未用标准溶液润洗滴定管,会导致测定结果_____ (填“偏大”“偏小”或“无影响”)。
(5)用惰性电极电解MnSO4酸性溶液可制得MnO2,请写出电解法制备MnO2时的阳极反应式:_____ 。

回答下列问题:
(1)仪器a的名称是
(2)装置Ⅱ中发生反应的化学方程式为
(3)结合图乙,分析反应后从溶液中获得MnSO4·H2O晶体的操作为

(4)测定饲料中硫酸锰的含量常将饲料溶于水,以磷酸作络合剂,用硝酸铵作氧化剂,将试样中的二价锰定量氧化成三价锰,过量的硝酸铵立即与产生的亚硝酸盐反应而消除其影响。然后加入指示剂,用硫酸亚铁铵[Fe(NH4)2(SO4)2]标准溶液滴定生成的三价锰,溶液由红色变为亮黄色为滴定终点。有关反应的离子方程式如下:
①2Mn2++NO
 +4PO
+4PO +2H+=2[Mn(PO4)2]3-+NO
+2H+=2[Mn(PO4)2]3-+NO +H2O;
+H2O;②NH
 +NO
+NO =N2↓+2H2O;
=N2↓+2H2O;③[Mn(PO4)2]3-+Fe2+=Mn2++[Fe(PO4)2]3-。
取ag饲料,消耗浓度为cmol•L-1的硫酸亚铁铵标准溶液VmL,则饲料中MnSO4·H2O的质量分数为
(5)用惰性电极电解MnSO4酸性溶液可制得MnO2,请写出电解法制备MnO2时的阳极反应式:
您最近一年使用:0次
2023-04-11更新
|
299次组卷
|
4卷引用:河南省焦作市博爱县第一中学2023-2024学年高三下学期开学化学试题
河南省焦作市博爱县第一中学2023-2024学年高三下学期开学化学试题(已下线)化学押题卷(一)重庆市乌江新高考协作体2023-2024学年高三上学期第一次联合调研抽测(一模)化学试题(已下线)T26-实验综合题
2022·北京·高考真题
4 . 煤中硫的存在形态分为有机硫和无机硫( 、硫化物及微量单质硫等)。库仑滴定法是常用的快捷检测煤中全硫含量的方法。其主要过程如下图所示。
、硫化物及微量单质硫等)。库仑滴定法是常用的快捷检测煤中全硫含量的方法。其主要过程如下图所示。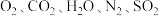 。
。
(1)煤样需研磨成细小粉末,其目的是___________ 。
(2)高温下,煤中 完全转化为
完全转化为 ,该反应的化学方程式为
,该反应的化学方程式为___________ 。
(3)通过干燥装置后,待测气体进入库仑测硫仪进行测定。
已知:库仑测硫仪中电解原理示意图如下。检测前,电解质溶液中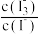 保持定值时,电解池不工作。待测气体进入电解池后,
保持定值时,电解池不工作。待测气体进入电解池后, 溶解并将
溶解并将 还原,测硫仪便立即自动进行电解到
还原,测硫仪便立即自动进行电解到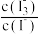 又回到原定值,测定结束,通过测定电解消耗的电量可以求得煤中含硫量。
又回到原定值,测定结束,通过测定电解消耗的电量可以求得煤中含硫量。 在电解池中发生反应的离子方程式为
在电解池中发生反应的离子方程式为___________ 。
②测硫仪工作时电解池的阳极反应式为___________ 。
(4)煤样为 ,电解消耗的电量为x库仑,煤样中硫的质量分数为
,电解消耗的电量为x库仑,煤样中硫的质量分数为___________ 。
已知:电解中转移 电子所消耗的电量为96500库仑。
电子所消耗的电量为96500库仑。
(5)条件控制和误差分析。
①测定过程中,需控制电解质溶液 ,当
,当 时,非电解生成的
时,非电解生成的 使得测得的全硫含量偏小,生成
使得测得的全硫含量偏小,生成 的离子方程式为
的离子方程式为___________ 。
②测定过程中,管式炉内壁上有 残留,测得全硫量结果为
残留,测得全硫量结果为___________ 。(填“偏大”或“偏小”)
 、硫化物及微量单质硫等)。库仑滴定法是常用的快捷检测煤中全硫含量的方法。其主要过程如下图所示。
、硫化物及微量单质硫等)。库仑滴定法是常用的快捷检测煤中全硫含量的方法。其主要过程如下图所示。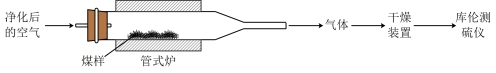
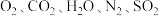 。
。(1)煤样需研磨成细小粉末,其目的是
(2)高温下,煤中
 完全转化为
完全转化为 ,该反应的化学方程式为
,该反应的化学方程式为(3)通过干燥装置后,待测气体进入库仑测硫仪进行测定。
已知:库仑测硫仪中电解原理示意图如下。检测前,电解质溶液中
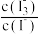 保持定值时,电解池不工作。待测气体进入电解池后,
保持定值时,电解池不工作。待测气体进入电解池后, 溶解并将
溶解并将 还原,测硫仪便立即自动进行电解到
还原,测硫仪便立即自动进行电解到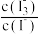 又回到原定值,测定结束,通过测定电解消耗的电量可以求得煤中含硫量。
又回到原定值,测定结束,通过测定电解消耗的电量可以求得煤中含硫量。
 在电解池中发生反应的离子方程式为
在电解池中发生反应的离子方程式为②测硫仪工作时电解池的阳极反应式为
(4)煤样为
 ,电解消耗的电量为x库仑,煤样中硫的质量分数为
,电解消耗的电量为x库仑,煤样中硫的质量分数为已知:电解中转移
 电子所消耗的电量为96500库仑。
电子所消耗的电量为96500库仑。(5)条件控制和误差分析。
①测定过程中,需控制电解质溶液
 ,当
,当 时,非电解生成的
时,非电解生成的 使得测得的全硫含量偏小,生成
使得测得的全硫含量偏小,生成 的离子方程式为
的离子方程式为②测定过程中,管式炉内壁上有
 残留,测得全硫量结果为
残留,测得全硫量结果为
您最近一年使用:0次
2022-07-01更新
|
7992次组卷
|
12卷引用:河南省焦作市博爱县第一中学2023-2024学年高三上学期12月月考化学试题
河南省焦作市博爱县第一中学2023-2024学年高三上学期12月月考化学试题(已下线)2022年北京市高考真题化学试题(部分试题)2022年北京市高考真题化学试题(已下线)2022年北京高考真题变式题1-14(已下线)易错点10 硫元素及其化合物-备战2023年高考化学考试易错题(已下线)易错点19 电化学基础-备战2023年高考化学考试易错题(已下线)热点情景汇编-专题十三 实验探究中的新思路湖南省长沙市第一中学2022-2023学年高二下学期第一次月考化学试题(已下线)2022年北京高考真题化学试题变式题(原理综合题)(已下线)专题14 化学实验综合题-2023年高考化学真题题源解密(全国通用)江苏省常州市联盟学校2023-2024学年高三上学期10月学情调研化学试题北京市第一六一中学2023-2024学年高三上学期12月月考化学试题
名校
5 . 硫氰化钾(KSCN)俗称玫瑰红酸钾,是一种用途广泛的化学药品。实验室模拟工业制备硫氰化钾的实验装置如图所示:
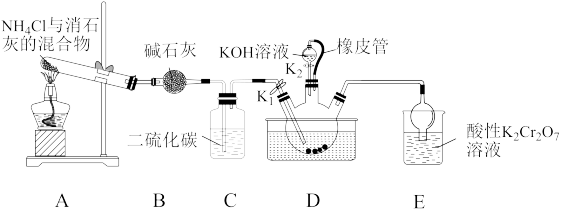
已知:①NH3不溶于CS2,CS2密度比水大且不溶于水;
②三颈烧瓶内盛放:CS2、水和催化剂;
③CS2+3NH3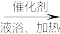 NH4SCN+NH4HS,该反应比较缓慢且NH4SCN在高于170℃易分解;
NH4SCN+NH4HS,该反应比较缓慢且NH4SCN在高于170℃易分解;
④NH4HS在105℃就会完全分解。
回答下列问题:
(1)装置A中反应的化学方程式是___ 。
(2)装置D中橡皮管的作用是___ 。
(3)制备KSCN溶液:熄灭A处的酒精灯,关闭K1,保持三颈烧瓶内液温为105℃一段时间,然后打开K2,继续保持液温105℃,缓缓滴入适量的KOH溶液,写出装置D中生成KSCN的离子方程式:___ 。
(4)制备硫氰化钾晶体:先滤去三颈烧瓶中的固体催化剂,再减压__ 、冷却结晶、过滤、洗涤、干燥,得到硫氰化钾晶体。
(5)测定晶体中KSCN的含量:称取6.0g样品,配成500mL溶液,量取25.00mL溶液于锥形瓶中,加入适量稀硝酸,再加入几滴Fe(NO3)3溶液作指示剂,用0.1000mol/LAgNO3标准溶液滴定,达到滴定终点时消耗AgNO3标准溶液18.00mL。[已知:滴定时发生反应的离子方程式:SCN-+Ag+=AgSCN↓(白色)]
①用AgNO3固体配制500mL0.1000mol•L-1的AgNO3标准溶液所需的玻璃仪器有烧杯、量筒、玻璃棒、胶头滴管、___ 。
②滴定终点溶液颜色的变化为___ 。
③晶体中KSCN的质量分数为___ 。

已知:①NH3不溶于CS2,CS2密度比水大且不溶于水;
②三颈烧瓶内盛放:CS2、水和催化剂;
③CS2+3NH3
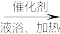 NH4SCN+NH4HS,该反应比较缓慢且NH4SCN在高于170℃易分解;
NH4SCN+NH4HS,该反应比较缓慢且NH4SCN在高于170℃易分解;④NH4HS在105℃就会完全分解。
回答下列问题:
(1)装置A中反应的化学方程式是
(2)装置D中橡皮管的作用是
(3)制备KSCN溶液:熄灭A处的酒精灯,关闭K1,保持三颈烧瓶内液温为105℃一段时间,然后打开K2,继续保持液温105℃,缓缓滴入适量的KOH溶液,写出装置D中生成KSCN的离子方程式:
(4)制备硫氰化钾晶体:先滤去三颈烧瓶中的固体催化剂,再减压
(5)测定晶体中KSCN的含量:称取6.0g样品,配成500mL溶液,量取25.00mL溶液于锥形瓶中,加入适量稀硝酸,再加入几滴Fe(NO3)3溶液作指示剂,用0.1000mol/LAgNO3标准溶液滴定,达到滴定终点时消耗AgNO3标准溶液18.00mL。[已知:滴定时发生反应的离子方程式:SCN-+Ag+=AgSCN↓(白色)]
①用AgNO3固体配制500mL0.1000mol•L-1的AgNO3标准溶液所需的玻璃仪器有烧杯、量筒、玻璃棒、胶头滴管、
②滴定终点溶液颜色的变化为
③晶体中KSCN的质量分数为
您最近一年使用:0次
2021-11-14更新
|
470次组卷
|
2卷引用:河南省温县第一高级中学2021-2022学年高三上学期11月月考化学试题
6 . 氮化铝(AlN)是一种新型无机材料,广泛应用于集成电路生产领域。其制取原理为: Al2O3+3C+N2 2 AlN+3CO
2 AlN+3CO
为了分析某AlN样品中 AlN的含量,某化学研究性学习小组成员设计了如下两种实验方案。
【方案1——量气法】用图中的一些装置来进行相关实验,根据反应中所生成氨气的体积来测定样品中的氮化铝的质量分数,并根据实验现象来确定杂质的成分(实验中导管体积忽略不计)。

(1)图中仪器A的名称是_______ ;写出AlN和NaOH溶液反应的化学方程式________ 。
(2)广口瓶中的试剂X最好选用下列试剂中的_______ (填选项的标号),广口瓶的液体没有装满(上方留有少量空间),实验测得NH3的体积将________ (填“偏大”、 “偏小”或“不变”)。
A.苯 B.酒精 C.植物油 D.CCl4
(3)若实验中测得样品的质量为2.56g,氨气的体积为1.12L(标况下),则样品中AlN的质量分数为______ 。
【方案2——测重量】按以下步骤测定样品中A1N的纯度:
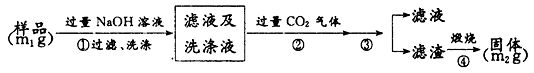
(4)步骤②生成沉淀的离子方程式为_______________ 。
(5)步骤③的操作是_____________ 。
(6)A1N的纯度是______________ (用m1、m2表示)。
 2 AlN+3CO
2 AlN+3CO为了分析某AlN样品中 AlN的含量,某化学研究性学习小组成员设计了如下两种实验方案。
【方案1——量气法】用图中的一些装置来进行相关实验,根据反应中所生成氨气的体积来测定样品中的氮化铝的质量分数,并根据实验现象来确定杂质的成分(实验中导管体积忽略不计)。

(1)图中仪器A的名称是
(2)广口瓶中的试剂X最好选用下列试剂中的
A.苯 B.酒精 C.植物油 D.CCl4
(3)若实验中测得样品的质量为2.56g,氨气的体积为1.12L(标况下),则样品中AlN的质量分数为
【方案2——测重量】按以下步骤测定样品中A1N的纯度:

(4)步骤②生成沉淀的离子方程式为
(5)步骤③的操作是
(6)A1N的纯度是
您最近一年使用:0次
名校
7 . H2O2是一种绿色氧化还原试剂,在化学研究中应用广泛。某研究性学习小组设计如图所示实验装置,探究影响H2O2分解反应速率的因素。
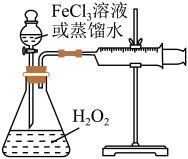
(1)①写出锥形瓶中反应的化学方程式________ 。
②设计实验方案:在不同条件下,测定_______ 。(要求所测得的数据能直接体现反应速率大小)
(2)探究影响H2O2分解反应速率的因素实验方案如下表所示,先向锥形瓶中加入质量分数为10%H2O2,再依次通过分液漏斗向锥形瓶中加入一定量的蒸馏水和FeCl3溶液,请回答问题:
①表格中a=_______ ,b=________ 。
②通过实验Ⅱ和Ⅲ探究浓度对反应速率影响。
(3)实验Ⅱ、Ⅲ中溶液颜色变深的原因是________ 。
(4)已知FeCl3溶液对H2O2的催化分解分为反应i和反应ii两步进行:
已知反应ii的离子方程式为:2Fe2++2H++H2O2=2Fe3++2H2O;
①反应i离子方程式为_______ 。
②某同学设计实验证明催化过程中有Fe2+产生:取2mLH2O2溶液于试管中,向试管中滴加2滴FeCl3溶液,再滴加2滴_______ 溶液,产生蓝色沉淀。
(5)向实验Ⅱ中反应后的溶液滴加KSCN溶液,溶液变红色,2min后溶液红色褪去;继续滴加KSCN溶液,溶液又变红色,一段时间后又褪色;此时再向溶液中滴加盐酸酸化后的BaCl2溶液,产生白色沉淀。请分析溶液红色褪去的原因______ 。

(1)①写出锥形瓶中反应的化学方程式
②设计实验方案:在不同条件下,测定
(2)探究影响H2O2分解反应速率的因素实验方案如下表所示,先向锥形瓶中加入质量分数为10%H2O2,再依次通过分液漏斗向锥形瓶中加入一定量的蒸馏水和FeCl3溶液,请回答问题:
| 实验序号 | 10%H2O2/mL | 蒸馏水/mL | 0.2mol·LFeCl3溶液/mL | 现象 |
| I | 10 | a | 0 | 无明显变化 |
| Ⅱ | 10 | b | 2 | 锥形瓶变热,溶液迅速变红棕色,并有较多气泡产生;2min时,反应变缓,溶液颜色明显变浅 |
| Ⅲ | 5 | 5 | 2 | 锥形瓶变热,溶液变棕色,开始5s后产生较少的气泡;2min时,反应速度加快 |
②通过实验Ⅱ和Ⅲ探究浓度对反应速率影响。
(3)实验Ⅱ、Ⅲ中溶液颜色变深的原因是
(4)已知FeCl3溶液对H2O2的催化分解分为反应i和反应ii两步进行:
已知反应ii的离子方程式为:2Fe2++2H++H2O2=2Fe3++2H2O;
①反应i离子方程式为
②某同学设计实验证明催化过程中有Fe2+产生:取2mLH2O2溶液于试管中,向试管中滴加2滴FeCl3溶液,再滴加2滴
(5)向实验Ⅱ中反应后的溶液滴加KSCN溶液,溶液变红色,2min后溶液红色褪去;继续滴加KSCN溶液,溶液又变红色,一段时间后又褪色;此时再向溶液中滴加盐酸酸化后的BaCl2溶液,产生白色沉淀。请分析溶液红色褪去的原因
您最近一年使用:0次
名校
解题方法
8 . 铁和铝及其化合物在日常生产生活中有着广泛的应用。
I.制备 晶体(实验装置如图所示)
晶体(实验装置如图所示)
氯化铁( )是一种棕色结晶,易升华,极易吸收空气里的水分而潮解。实验室制备无水氯化铁并探究氯化铁性质的相关实验如下:
)是一种棕色结晶,易升华,极易吸收空气里的水分而潮解。实验室制备无水氯化铁并探究氯化铁性质的相关实验如下:___________ 。
(2)实验装置接口的连接顺序是a→___________ →g,G中盛装的物质是___________ ,其作用是___________ 。
(3)实验开始应先点燃___________ (填“A”或“B”)处的酒精灯,当观察到___________ 时(填现象),再点燃另一处的酒精灯。
Ⅱ.测定铁铝合金中铝的质量分数(实验装置如图所示)___________ 。
(5)装置中导管a的作用除了使分液漏斗中的稀硫酸能顺利滴下以外,另一个作用是_______ 。
(6)若实验用铁铝合金的质量为0.334g,测得气体体积为67.2mL(已转换成标准状况),则合金中铝的质量分数为___________ (结果保留三位有效数字),该测量结果偏低,可能的原因是___________ (填字母)。
A.反应结束,未恢复至室温就读数
B.反应后读数时,甲侧液面低于乙侧液面
C.反应产生的气体没有完全被排入量气装置
D.反应后仰视刻度线读数
I.制备
 晶体(实验装置如图所示)
晶体(实验装置如图所示)氯化铁(
 )是一种棕色结晶,易升华,极易吸收空气里的水分而潮解。实验室制备无水氯化铁并探究氯化铁性质的相关实验如下:
)是一种棕色结晶,易升华,极易吸收空气里的水分而潮解。实验室制备无水氯化铁并探究氯化铁性质的相关实验如下: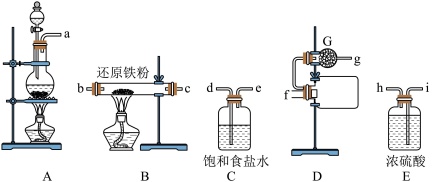
(2)实验装置接口的连接顺序是a→
(3)实验开始应先点燃
Ⅱ.测定铁铝合金中铝的质量分数(实验装置如图所示)
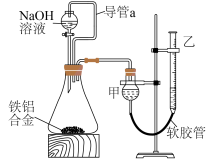
(5)装置中导管a的作用除了使分液漏斗中的稀硫酸能顺利滴下以外,另一个作用是
(6)若实验用铁铝合金的质量为0.334g,测得气体体积为67.2mL(已转换成标准状况),则合金中铝的质量分数为
A.反应结束,未恢复至室温就读数
B.反应后读数时,甲侧液面低于乙侧液面
C.反应产生的气体没有完全被排入量气装置
D.反应后仰视刻度线读数
您最近一年使用:0次
2023-12-12更新
|
221次组卷
|
4卷引用:河南省焦作市博爱县第一中学2023-2024学年高一下学期4月期中考试化学试题
名校
9 . 高铁酸钾 是一种高效净水剂.已知:
是一种高效净水剂.已知: 易溶于水,微溶于浓
易溶于水,微溶于浓 溶液;在酸性或中性溶液中不稳定,在
溶液;在酸性或中性溶液中不稳定,在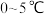 的强碱性溶液中较稳定.如图所示某实验小组欲制备高铁酸钾并测定其纯度.
的强碱性溶液中较稳定.如图所示某实验小组欲制备高铁酸钾并测定其纯度._____________ ,装置A中发生反应时,每生成 消耗的高锰酸钾的物质的量为
消耗的高锰酸钾的物质的量为_____________ .
(2)将除杂装置B补充完整并标明所用试剂_____________ .
(3)装置C中 与
与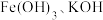 反应生成
反应生成 的化学方程式为
的化学方程式为________________________________________________ .
(4)实验时将装置C置于冰水浴中,其原因是__________________________________ .
(5)实验后经结晶法得到的 晶体仍含较多杂质,要得到更纯的晶体,还应采取的操作方法是
晶体仍含较多杂质,要得到更纯的晶体,还应采取的操作方法是_____________ .
(6)将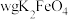 粗产品溶于过量的碱性亚铬酸盐溶液中,充分反应后,加入稀硫酸酸化至
粗产品溶于过量的碱性亚铬酸盐溶液中,充分反应后,加入稀硫酸酸化至 为2,在所得的重铬酸盐溶液中加入5滴二苯胺磺酸钠溶液作指示剂,然后用
为2,在所得的重铬酸盐溶液中加入5滴二苯胺磺酸钠溶液作指示剂,然后用 标准溶液滴定至终点,消耗标准溶液
标准溶液滴定至终点,消耗标准溶液 .已知该过程中涉及的离子反应主要有三个:
.已知该过程中涉及的离子反应主要有三个:
① ;
;
② ;
;
③ .
.
该粗产品中 的质量分数为
的质量分数为_____________ (用含w、c、V的代数式表示),若滴定管没有用标准液润洗,则测得的结果_____________ (填“偏高”“偏低”或“无影响”).
 是一种高效净水剂.已知:
是一种高效净水剂.已知: 易溶于水,微溶于浓
易溶于水,微溶于浓 溶液;在酸性或中性溶液中不稳定,在
溶液;在酸性或中性溶液中不稳定,在 的强碱性溶液中较稳定.如图所示某实验小组欲制备高铁酸钾并测定其纯度.
的强碱性溶液中较稳定.如图所示某实验小组欲制备高铁酸钾并测定其纯度.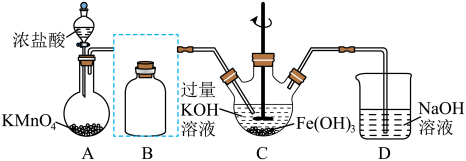
 消耗的高锰酸钾的物质的量为
消耗的高锰酸钾的物质的量为(2)将除杂装置B补充完整并标明所用试剂
(3)装置C中
 与
与 反应生成
反应生成 的化学方程式为
的化学方程式为(4)实验时将装置C置于冰水浴中,其原因是
(5)实验后经结晶法得到的
 晶体仍含较多杂质,要得到更纯的晶体,还应采取的操作方法是
晶体仍含较多杂质,要得到更纯的晶体,还应采取的操作方法是(6)将
 粗产品溶于过量的碱性亚铬酸盐溶液中,充分反应后,加入稀硫酸酸化至
粗产品溶于过量的碱性亚铬酸盐溶液中,充分反应后,加入稀硫酸酸化至 为2,在所得的重铬酸盐溶液中加入5滴二苯胺磺酸钠溶液作指示剂,然后用
为2,在所得的重铬酸盐溶液中加入5滴二苯胺磺酸钠溶液作指示剂,然后用 标准溶液滴定至终点,消耗标准溶液
标准溶液滴定至终点,消耗标准溶液 .已知该过程中涉及的离子反应主要有三个:
.已知该过程中涉及的离子反应主要有三个:①
 ;
;②
 ;
;③
 .
.该粗产品中
 的质量分数为
的质量分数为
您最近一年使用:0次
2024-01-14更新
|
61次组卷
|
2卷引用:河南省焦作市博爱县第一中学2023-2024学年高二上学期1月期末化学试题
名校
解题方法
10 . 双氧水是工业上常用的绿色氧化剂,也是治疗创伤伤口的消毒清洗剂。
(1)医疗上可用质量分数为 的过氧化氢溶液对伤口进行消毒,当过氧化氢溶液接触到伤口处时,H2O2就会迅速分解,可能原因是
的过氧化氢溶液对伤口进行消毒,当过氧化氢溶液接触到伤口处时,H2O2就会迅速分解,可能原因是___________ 。
(2)为了除去酸性溶液中的 ,常先加入双氧水将
,常先加入双氧水将 氧化成
氧化成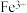 ,该反应的离子方程式为
,该反应的离子方程式为___________ 。
(3)金属空气电池具有很高的容量和功率密度,但在缺氧条件下性能受到限制。在无氧条件下,双氧水半燃料电池是一个可行的选择。下图为铝、铂电极与双氧水/氢氧化钾溶液构成的原电池。
金属空气电池具有很高的容量和功率密度,但在缺氧条件下性能受到限制。在无氧条件下,双氧水半燃料电池是一个可行的选择。下图为铝、铂电极与双氧水/氢氧化钾溶液构成的原电池。
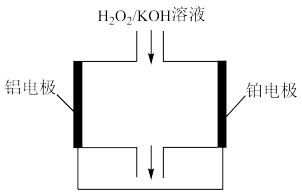
铝电极为原电池的___________ 极(填“正”或“负”),该电极发生___________ 反应(填“氧化”或“还原”)。电池放电时电解质溶液中的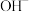 向
向___________ 电极(填“铝”或“铂”)移动。
(4)为探究外界条件对H2O2分解反应速率的影响,相关实验设计如下表所示:
表中a=___________ ;III中加2.0 水的目的是
水的目的是___________ 。
(5)过氧化氢一定条件下可发生分解: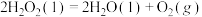 ,断裂1
,断裂1
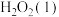 中的
中的 键和1
键和1
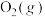 中的
中的 键所需的能量依次为142
键所需的能量依次为142 、497.3
、497.3 ,断裂
,断裂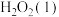 和
和 中1
中1
 键所需能量依次为367
键所需能量依次为367 、467
、467 ,则2
,则2
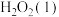 反应生成2
反应生成2
 和1
和1
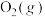
___________ (填“吸收"或“放出”)的能量为___________  。
。
(1)医疗上可用质量分数为
 的过氧化氢溶液对伤口进行消毒,当过氧化氢溶液接触到伤口处时,H2O2就会迅速分解,可能原因是
的过氧化氢溶液对伤口进行消毒,当过氧化氢溶液接触到伤口处时,H2O2就会迅速分解,可能原因是(2)为了除去酸性溶液中的
 ,常先加入双氧水将
,常先加入双氧水将 氧化成
氧化成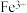 ,该反应的离子方程式为
,该反应的离子方程式为(3)金属空气电池具有很高的容量和功率密度,但在缺氧条件下性能受到限制。在无氧条件下,双氧水半燃料电池是一个可行的选择。下图为铝、铂电极与双氧水/氢氧化钾溶液构成的原电池。
金属空气电池具有很高的容量和功率密度,但在缺氧条件下性能受到限制。在无氧条件下,双氧水半燃料电池是一个可行的选择。下图为铝、铂电极与双氧水/氢氧化钾溶液构成的原电池。

铝电极为原电池的
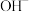 向
向(4)为探究外界条件对H2O2分解反应速率的影响,相关实验设计如下表所示:
| 试管编号 | 实验目的 | H2O2溶液 | 温度 | 水的体积/ |  溶液体积/ 溶液体积/ | |
| 质量分数 | 体积/ | |||||
| I | 为编号II作实验参照 | 10% | 2.0 | 常温 | 0 | 0 |
| II | 温度对反应速率的影响 | a | 2.0 | 50℃ | 0 | 0 |
| III | 为编号IV作实验参照 | 5.0% | 2.0 | 常温 | 2.0 | 0 |
| IV | 催化剂对反应速率的影响 | 5.0% | 2.0 | 常温 | 0 | 2.0 |
 水的目的是
水的目的是(5)过氧化氢一定条件下可发生分解:
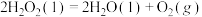 ,断裂1
,断裂1
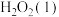 中的
中的 键和1
键和1
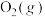 中的
中的 键所需的能量依次为142
键所需的能量依次为142 、497.3
、497.3 ,断裂
,断裂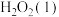 和
和 中1
中1
 键所需能量依次为367
键所需能量依次为367 、467
、467 ,则2
,则2
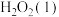 反应生成2
反应生成2
 和1
和1
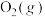
 。
。
您最近一年使用:0次
2023-04-13更新
|
257次组卷
|
2卷引用:河南省焦作市2022-2023学年高一下学期4月期中考试化学试题



