名校
1 . 对下列实验事实的结论表述正确的是
| 选项 | 实验 | 现象 | 结论 |
| A | 向Na2CO3溶液中加入浓盐酸,将产生的气体直接通入硅酸钠溶液中 | 产生白色浑浊 | 酸性: 盐酸>碳酸>硅酸 |
| B | 将常温下用冷的浓硝酸处理过的铝片插入硫酸铜溶液中 | 铝片表面无明显现象 | 用硝酸处理后,铝的金属性减弱 |
| C | 取少量Na2SO3样品溶于蒸馏水,加入足量稀盐酸,再加入足量BaCl2溶液 | 有白色沉淀产生 | 样品已经变质 |
| D | 向黄色的Fe(NO3)3溶液中滴加氢碘酸,再加入四氯化碳 | 溶液变为紫红色 | 氧化性:Fe3+>I2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-07-13更新
|
230次组卷
|
3卷引用:河南省温县第一高级中学2021-2022学年高二上学期开学考试化学试题
解题方法
2 . 2020年新冠肺炎(COVID-19)疫情肆虐全球,含氯消毒剂、过氧化物等均能有效灭活病毒。请回答下列问题:
(1)下列消毒剂中,被称为绿色氧化剂的是_______ (填序号)。
A. B.
B.  C.
C. 
(2) 保存不当会变质生成
保存不当会变质生成 ,某兴趣小组为了探究过氧化钠样品是否变质进行如下操作:取少量样品,用蒸馏水溶解,加入
,某兴趣小组为了探究过氧化钠样品是否变质进行如下操作:取少量样品,用蒸馏水溶解,加入 溶液,振荡,
溶液,振荡,_______ (填现象),证明 已变质;否则,
已变质;否则, 未变质。
未变质。
(3)某兴趣小组设计如图所示实验装置制取少量漂白液。
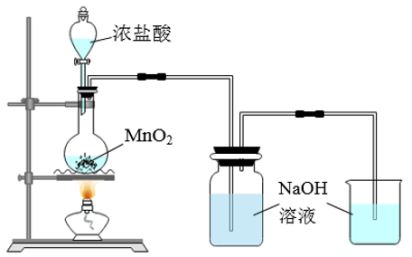
①写出制取漂白液反应的离子方程式:_______ 。
②此实验所得漂白液的有效成分 含量偏低,该小组经分析并查阅资料发现,主要原因是还存在两个副反应:一个副反应是氯气与
含量偏低,该小组经分析并查阅资料发现,主要原因是还存在两个副反应:一个副反应是氯气与 溶液反应放热,温度较高时生成
溶液反应放热,温度较高时生成 ,为避免此副反应的发生,可采取的措施是
,为避免此副反应的发生,可采取的措施是_______ ;另一个副反应是_______ (写化学方程式)。
(1)下列消毒剂中,被称为绿色氧化剂的是
A.
 B.
B.  C.
C. 
(2)
 保存不当会变质生成
保存不当会变质生成 ,某兴趣小组为了探究过氧化钠样品是否变质进行如下操作:取少量样品,用蒸馏水溶解,加入
,某兴趣小组为了探究过氧化钠样品是否变质进行如下操作:取少量样品,用蒸馏水溶解,加入 溶液,振荡,
溶液,振荡, 已变质;否则,
已变质;否则, 未变质。
未变质。(3)某兴趣小组设计如图所示实验装置制取少量漂白液。

①写出制取漂白液反应的离子方程式:
②此实验所得漂白液的有效成分
 含量偏低,该小组经分析并查阅资料发现,主要原因是还存在两个副反应:一个副反应是氯气与
含量偏低,该小组经分析并查阅资料发现,主要原因是还存在两个副反应:一个副反应是氯气与 溶液反应放热,温度较高时生成
溶液反应放热,温度较高时生成 ,为避免此副反应的发生,可采取的措施是
,为避免此副反应的发生,可采取的措施是
您最近一年使用:0次
解题方法
3 . 过量排放含氮化合物对大气和水体造成环境污染,研究氮及其化合物的性质及转化,对降低含氮物质的污染有着重大的意义。
(1)水体中过量氨氮(以 表示)会导致水体富营养化。次氯酸钠去除氨氮的反应历程可以表示如下:
表示)会导致水体富营养化。次氯酸钠去除氨氮的反应历程可以表示如下:
I.
II.
III.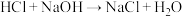
①写出用次氯酸钠去除氨氮的总反应的化学方程式:_____ 。
②从该反应历程并结合 的性质分析,温度过高时氨氮的去除率降低的主要原因是
的性质分析,温度过高时氨氮的去除率降低的主要原因是_____ 。
(2)用零价铁( )可以去除水体中的
)可以去除水体中的 以修复环境。在用
以修复环境。在用 去除水体中的
去除水体中的 时,
时,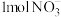 转化成
转化成 时转移
时转移____  电子。
电子。
(3)实验室模拟测定大气中 的含量,将含有
的含量,将含有 的气体样品
的气体样品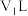 通入适量酸化的
通入适量酸化的 溶液中,使
溶液中,使 恰好完全被氧化为
恰好完全被氧化为 ,加水稀释至
,加水稀释至 ,向其中加入
,向其中加入 溶液时恰好完全反应。
溶液时恰好完全反应。
①加入 溶液时发生反应的离子方程式是
溶液时发生反应的离子方程式是_______ 。
②气体样品中 折合成
折合成 的含量为
的含量为_______  (用含
(用含 、
、 、c的代数式表示)。若
、c的代数式表示)。若 溶液部分变质,会使测定结果
溶液部分变质,会使测定结果_______ (填“偏高”“偏低”或“无影响”)。
(1)水体中过量氨氮(以
 表示)会导致水体富营养化。次氯酸钠去除氨氮的反应历程可以表示如下:
表示)会导致水体富营养化。次氯酸钠去除氨氮的反应历程可以表示如下:I.

II.

III.
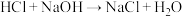
①写出用次氯酸钠去除氨氮的总反应的化学方程式:
②从该反应历程并结合
 的性质分析,温度过高时氨氮的去除率降低的主要原因是
的性质分析,温度过高时氨氮的去除率降低的主要原因是(2)用零价铁(
 )可以去除水体中的
)可以去除水体中的 以修复环境。在用
以修复环境。在用 去除水体中的
去除水体中的 时,
时,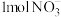 转化成
转化成 时转移
时转移 电子。
电子。(3)实验室模拟测定大气中
 的含量,将含有
的含量,将含有 的气体样品
的气体样品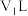 通入适量酸化的
通入适量酸化的 溶液中,使
溶液中,使 恰好完全被氧化为
恰好完全被氧化为 ,加水稀释至
,加水稀释至 ,向其中加入
,向其中加入 溶液时恰好完全反应。
溶液时恰好完全反应。①加入
 溶液时发生反应的离子方程式是
溶液时发生反应的离子方程式是②气体样品中
 折合成
折合成 的含量为
的含量为 (用含
(用含 、
、 、c的代数式表示)。若
、c的代数式表示)。若 溶液部分变质,会使测定结果
溶液部分变质,会使测定结果
您最近一年使用:0次
解题方法
4 . 在有机化学中,硫酰氯(SO2Cl2)常用作氯化剂和氯磺化剂,在染料、药品、除草剂和农用杀虫剂的生产过程中有重要作用。现在拟用干燥的Cl2和SO2在活性炭催化下制取硫酰氯。反应的化学方程式为:SO2(g)+ Cl2(g) =SO2Cl2(l) ΔH =−97.3 kJ·mol−1,实验装置如图所示(部分夹持装置未画出)。
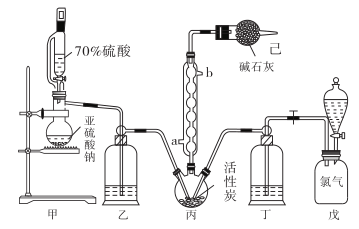
已知:硫酰氯通常条件下为无色液体,熔点−54.1℃,沸点69.1℃。在潮湿空气中“发烟”;100°C以上开始分解,生成二氧化硫和氯气,长期放置也会发生分解。
回答下列问题:
(1)装置丙中作为反应容器的仪器的名称为_______ ,装置丙中球形冷凝管的作用是________ ;如何控制两种反应物体积相等:____________________________________ 。
(2)装置戊上方分液漏斗中最好选用下列试剂:_________________ (选填字母)
A.蒸馏水 B.饱和食盐水 C.浓氢氧化钠溶液 D.6.0 mol·L-1盐酸
(3)若缺少装置己,硫酰氯(SO2Cl2)会和空气中的水反应而变质,其化学方程式是______________________________ 。
(4)氯磺酸(ClSO3H)加热分解,也能制得硫酰氯:2ClSO3H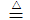 SO2Cl2 + H2SO4,分离两种产物的方法是
SO2Cl2 + H2SO4,分离两种产物的方法是_____________ (选填字母)。
A.重结晶 B.过滤 C.蒸馏 D.萃取
(5)长期储存的硫酰氯会发黄,可能的原因是_________________________________ (用化学方程式和必要的文字加以解释)。
(6)若反应中消耗的氯气体积为896 mL(标准状况下),最后经过分离提纯得到4.05 g纯净的硫酰氯,则硫酰氯的产率为___________ 。
(7)请设计实验方案检验产品中有硫酸(可选试剂:稀盐酸、稀硝酸、BaCl2溶液、蒸馏水、石蕊溶液):___________________________ 。

已知:硫酰氯通常条件下为无色液体,熔点−54.1℃,沸点69.1℃。在潮湿空气中“发烟”;100°C以上开始分解,生成二氧化硫和氯气,长期放置也会发生分解。
回答下列问题:
(1)装置丙中作为反应容器的仪器的名称为
(2)装置戊上方分液漏斗中最好选用下列试剂:
A.蒸馏水 B.饱和食盐水 C.浓氢氧化钠溶液 D.6.0 mol·L-1盐酸
(3)若缺少装置己,硫酰氯(SO2Cl2)会和空气中的水反应而变质,其化学方程式是
(4)氯磺酸(ClSO3H)加热分解,也能制得硫酰氯:2ClSO3H
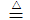 SO2Cl2 + H2SO4,分离两种产物的方法是
SO2Cl2 + H2SO4,分离两种产物的方法是A.重结晶 B.过滤 C.蒸馏 D.萃取
(5)长期储存的硫酰氯会发黄,可能的原因是
(6)若反应中消耗的氯气体积为896 mL(标准状况下),最后经过分离提纯得到4.05 g纯净的硫酰氯,则硫酰氯的产率为
(7)请设计实验方案检验产品中有硫酸(可选试剂:稀盐酸、稀硝酸、BaCl2溶液、蒸馏水、石蕊溶液):
您最近一年使用:0次
2018-06-06更新
|
427次组卷
|
3卷引用:河南省焦作市县级重点中学2021-2022学年高三上学期期中考试化学试题
名校
解题方法
5 . 我国规定,食盐中加入KIO3。某厂生产碘酸钾(KIO3)的工艺流程如图:
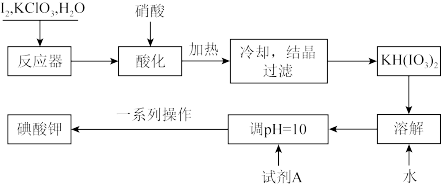
请回答下列问题:
(1)试剂A是____ ;流程图中“一系列操作”包括蒸发浓缩、降温结晶、过滤、洗涤、干燥。其中,“洗涤剂”是75%的酒精,而不用蒸馏水,其主要原因是____ 。
(2)工业上,还可用电解法制取KIO3。以石墨和不锈钢为电极材料,电解KI溶液。化学方程式为KI+3H2O KIO3+3H2↑。在该反应中,氧化产物是
KIO3+3H2↑。在该反应中,氧化产物是____ 。
(3)常用KI淀粉试纸检验碘盐,其操作是:取少量样品溶于蒸馏水,加几滴食醋,用KI淀粉试纸蘸取该溶液,若变蓝色,则该盐为加碘盐。写出离子方程式____ 。
(4)测定产品纯度:取wg产品溶于蒸馏水,配制成250mL溶液。取20mL所配制溶液于锥形瓶中,加入过量的KI溶液,滴适量稀硫酸,再滴加几滴指示剂B,用cmol·L-1Na2S2O3溶液滴定至终点,消耗标准溶液为VmL。已知:I2+2S2O =2I-+S4O
=2I-+S4O 。
。
①根据上述数据,测得产品纯度为____ (用含w、c、V表达式表示)。
②为了充分反应,滴定之前需要“振荡”锥形瓶中溶液,如果振荡时间过长,测得结果会____ (填“偏高”、“偏低”或“无影响”)。

请回答下列问题:
(1)试剂A是
(2)工业上,还可用电解法制取KIO3。以石墨和不锈钢为电极材料,电解KI溶液。化学方程式为KI+3H2O
 KIO3+3H2↑。在该反应中,氧化产物是
KIO3+3H2↑。在该反应中,氧化产物是(3)常用KI淀粉试纸检验碘盐,其操作是:取少量样品溶于蒸馏水,加几滴食醋,用KI淀粉试纸蘸取该溶液,若变蓝色,则该盐为加碘盐。写出离子方程式
(4)测定产品纯度:取wg产品溶于蒸馏水,配制成250mL溶液。取20mL所配制溶液于锥形瓶中,加入过量的KI溶液,滴适量稀硫酸,再滴加几滴指示剂B,用cmol·L-1Na2S2O3溶液滴定至终点,消耗标准溶液为VmL。已知:I2+2S2O
 =2I-+S4O
=2I-+S4O 。
。①根据上述数据,测得产品纯度为
②为了充分反应,滴定之前需要“振荡”锥形瓶中溶液,如果振荡时间过长,测得结果会
您最近一年使用:0次
2022-07-29更新
|
207次组卷
|
3卷引用:河南省焦作市修武县第一中学2022-2023学年高二上学期定位考试化学试题
名校
解题方法
6 . 现有由Al2O3、SiO2、CuO、C、Fe中的几种物质组成的混合粉末,取样品进行下列实验(部分产物略去)。下列关于混合粉末的组成判断错误的是
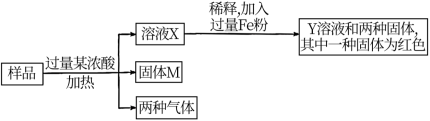

| A.“过量某浓酸”可能是浓硝酸 |
| B.M是SiO2 |
| C.混合粉末中一定含有CuO、C |
| D.“两种气体”遇水一定发生氧化还原反应 |
您最近一年使用:0次
2021-04-29更新
|
165次组卷
|
2卷引用:河南省焦作市普通高中2020-2021学年高一下学期期中考试化学试题



