18. 氢气是未来理想的能源。
(1)实验室用铁与2mol·L
-1的硫酸反应生成H
2的物质的量与反应时间的关系如图所示。按要求回答下列问题。
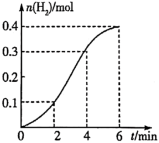
①产生H
2的平均反应速率最大的时间段是
___(填“0~2min”“2~4min”或“4~6min”),该时间段内对反应速率起关键作用的影响因素是
___。
②若向体系中加入少量硫酸铜溶液,可以加快氢气的生成速率,其原因是
___。
③要加快上述实验中产生氢气的速率,还可采取的措施是
__(填一种)。
(2)工业上用海水制氢气的新技术的原理为2H
2O
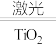
2H
2↑+O
2↑。回答下列问题:
①分解海水的反应属于
___“反应(填“放热”或“吸热”)。
②分解产生的氢气储存比较困难,有一种储存方法的原理可表示为NaHCO
3+H
2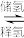
HCOONa+H
2O。下列说法正确的是
__(填序号)。
A.储氢、释氢过程中均有能量变化
B.储氢时反应物中只有离子键、非极性键的断裂
C.储氢过程中,NaHCO
3被还原
D.释氢过程中,每消耗0.1molH
2O放出2.24LH
2(3)H
2可与I
2发生反应:I
2(g)+H
2(g)

2HI(g)。一定温度下,在恒容密闭容器中进行该反应,下列叙述能说明该反应达到平衡的是
___(填序号)。
A.2v(H
2)=v(HI)
B.断裂1molH—H键的同时形成1molI—I键
C.容器内气体的压强不变
D.容器内气体的颜色不变