名校
解题方法
1 . 2-甲基-2-丁醇是一种有机合成中间体,通常以溴乙烷、镁、丙酮等为原料,无水乙醚为溶剂,在无水、无氧的条件下,通过格氏反应制备。
反应过程:
ⅰ.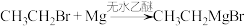 (乙基溴化镁);
(乙基溴化镁);
反应装置如图所示:
步骤1:乙基溴化镁的制备
在干燥的三颈烧瓶中加入1.8g镁粉、1小粒碘,在仪器A中加入7mL溴乙烷、15mL无水乙醚,混匀。安装搅拌、回流装置,由仪器A向三口瓶中滴入40滴(约2mL)溴乙烷、乙醚混合液。待反应缓和后,开动搅拌器,滴加剩余的混合液,控制滴速,维持反应液呈微沸状态,滴加完毕,用温水浴继续回流搅拌0.5h。使镁粉反应完全,冷却至室温。
步骤2:2-甲基-2-丁醇粗产品的制备
开动搅拌器,向仪器A中加入3.7mL(约0.05mol)无水丙酮和5mL无水乙醚的混合液,滴加完毕,继续搅拌15min,三颈烧瓶中有灰白色粘稠状固体析出。冷却后,在搅拌条件下滴加30mL 20%硫酸溶液。待反应完全后,分离得到醚溶液。
步骤3:蒸馏
将醚溶液加入烧瓶中,蒸去乙醚,再在电热套上直接加热蒸出产品,收集95~105℃馏分。
回答下列问题:
(1)仪器A的名称为_______ ;步骤3中蒸去乙醚的最佳加热方式为_______ 。
(2)本实验无需加入沸石的原因为_______ 。
(3)反应装置图中碱石灰的作用是_______ 。
(4)本实验采用乙醚作溶剂的优点为_______(填选项字母)。
(5)步骤2中的反应是放热反应,为避免反应过于剧烈,可采取的措施有_______ (任写两条)。
(6)步骤2中分离出醚溶液的具体操作为_______ 。
(7)实验结束后,测得产品质量为3.2g,则本实验的产率为_______ (保留三位有效数字)。
反应过程:
ⅰ.
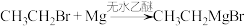 (乙基溴化镁);
(乙基溴化镁);ⅱ.CH3CH2MgBr+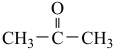
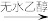
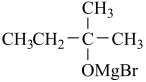 ;
;
ⅲ.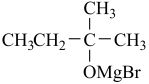

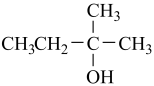 (未配平,部分生成物略)。
(未配平,部分生成物略)。
| 名称 | 相对分子质量 | 性状 | 密度( ) ) | 沸点(℃) | 溶解度(g/100mL溶剂) | |
| 水 | 乙醚 | |||||
| 乙醚 | 74 | 无色透明液体 | 0.7097 | 34.5 | 微溶 | — |
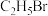 | 109 | 无色透明液体 | 1.2990 | 38.4 | 0.914 | 混溶 |
| 丙酮 | 58 | 无色透明液体 | 0.7899 | 56.2 | 混溶 | 混溶 |
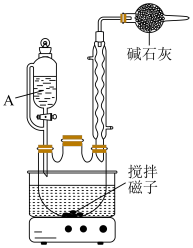
步骤1:乙基溴化镁的制备
在干燥的三颈烧瓶中加入1.8g镁粉、1小粒碘,在仪器A中加入7mL溴乙烷、15mL无水乙醚,混匀。安装搅拌、回流装置,由仪器A向三口瓶中滴入40滴(约2mL)溴乙烷、乙醚混合液。待反应缓和后,开动搅拌器,滴加剩余的混合液,控制滴速,维持反应液呈微沸状态,滴加完毕,用温水浴继续回流搅拌0.5h。使镁粉反应完全,冷却至室温。
步骤2:2-甲基-2-丁醇粗产品的制备
开动搅拌器,向仪器A中加入3.7mL(约0.05mol)无水丙酮和5mL无水乙醚的混合液,滴加完毕,继续搅拌15min,三颈烧瓶中有灰白色粘稠状固体析出。冷却后,在搅拌条件下滴加30mL 20%硫酸溶液。待反应完全后,分离得到醚溶液。
步骤3:蒸馏
将醚溶液加入烧瓶中,蒸去乙醚,再在电热套上直接加热蒸出产品,收集95~105℃馏分。
回答下列问题:
(1)仪器A的名称为
(2)本实验无需加入沸石的原因为
(3)反应装置图中碱石灰的作用是
(4)本实验采用乙醚作溶剂的优点为_______(填选项字母)。
| A.使有机镁化合物更稳定,并能溶解于乙醚 |
| B.易挥发,可以排除反应器中大部分空气 |
| C.无毒、无害、绿色环保 |
D.沸点与 接近,便于步骤1分离出未反应的 接近,便于步骤1分离出未反应的 |
(5)步骤2中的反应是放热反应,为避免反应过于剧烈,可采取的措施有
(6)步骤2中分离出醚溶液的具体操作为
(7)实验结束后,测得产品质量为3.2g,则本实验的产率为
您最近一年使用:0次
7日内更新
|
143次组卷
|
3卷引用:陕西省渭南高级中学2025届高三上学期9月份联考化学试题
名校
解题方法
2 . 二氧化碳加氢制甲烷有利于实现“碳达峰、碳中和”,该过程中的主要反应为
①
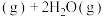
 ;
;
②
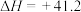
 。
。
回答下列问题:
(1)写出甲烷与 反应制取水煤气(CO、
反应制取水煤气(CO、 )的热化学方程式:
)的热化学方程式:_______ 。
(2)已知部分化学键的键能数据如表所示:
其中x=_______ 。
(3)恒温恒压下,向某密闭容器中充入一定量的 和
和 ,同时发生反应①和②,下列事实能说明反应②达到化学平衡状态的是_______。
,同时发生反应①和②,下列事实能说明反应②达到化学平衡状态的是_______。
(4)向若干个体积均为2L的恒容密闭容器中均充入1mol  、3.6mol
、3.6mol  ,若只发生反应①
,若只发生反应①
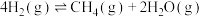 △H=-165kJ/mol,在不同温度下经过10min测得各容器中
△H=-165kJ/mol,在不同温度下经过10min测得各容器中 的转化率如图所示。
的转化率如图所示。 转化率先升高后降低的原因是
转化率先升高后降低的原因是_______ 。
②X点对应的坐标为(400,80),X点对应 的转化率为
的转化率为_______ (保留三位有效数字);X点对应的容器中压强为 kPa,则X点对应的平衡常数
kPa,则X点对应的平衡常数
_______ 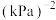 (用含
(用含 的代数式表示,
的代数式表示, 为用分压表示的平衡常数,气体的分压=总压×该气体的物质的量分数)。
为用分压表示的平衡常数,气体的分压=总压×该气体的物质的量分数)。
③X、Y两点对应的平衡常数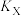
_______ 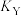 (填“大于”、“等于”或“小于”)。
(填“大于”、“等于”或“小于”)。
①

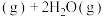
 ;
;②

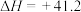
 。
。回答下列问题:
(1)写出甲烷与
 反应制取水煤气(CO、
反应制取水煤气(CO、 )的热化学方程式:
)的热化学方程式:(2)已知部分化学键的键能数据如表所示:
| 化学键 | C-H | H-H | O-H | C=O |
| 键能(kJ/mol) | 414 | 436 | 463 | x |
(3)恒温恒压下,向某密闭容器中充入一定量的
 和
和 ,同时发生反应①和②,下列事实能说明反应②达到化学平衡状态的是_______。
,同时发生反应①和②,下列事实能说明反应②达到化学平衡状态的是_______。| A.容器内气体密度不再变化 | B.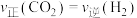 |
| C.气体的平均相对分子质量不再变化 | D.混合气体的总质量不变 |
 、3.6mol
、3.6mol  ,若只发生反应①
,若只发生反应①
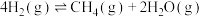 △H=-165kJ/mol,在不同温度下经过10min测得各容器中
△H=-165kJ/mol,在不同温度下经过10min测得各容器中 的转化率如图所示。
的转化率如图所示。
 转化率先升高后降低的原因是
转化率先升高后降低的原因是②X点对应的坐标为(400,80),X点对应
 的转化率为
的转化率为 kPa,则X点对应的平衡常数
kPa,则X点对应的平衡常数
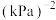 (用含
(用含 的代数式表示,
的代数式表示, 为用分压表示的平衡常数,气体的分压=总压×该气体的物质的量分数)。
为用分压表示的平衡常数,气体的分压=总压×该气体的物质的量分数)。③X、Y两点对应的平衡常数
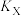
 (填“大于”、“等于”或“小于”)。
(填“大于”、“等于”或“小于”)。
您最近一年使用:0次
7日内更新
|
417次组卷
|
3卷引用:陕西省渭南高级中学2025届高三上学期9月份联考化学试题
名校
3 . 一种熔盐液相氧化法制备高价铬盐(如 、
、 )的新工艺如图所示,该工艺不消耗除铬铁矿、氢氧化钠和空气以外的其他原料,也不产生废弃物,能实现Cr-Fe-Al-Mg的深度利用和
)的新工艺如图所示,该工艺不消耗除铬铁矿、氢氧化钠和空气以外的其他原料,也不产生废弃物,能实现Cr-Fe-Al-Mg的深度利用和 的循环利用。
的循环利用。
(1) 中Fe、Cr元素的化合价分别为
中Fe、Cr元素的化合价分别为_______ 价、_______ 价。
(2)固体Ⅲ的成分是_______ (填化学式);工序ⅲ中反应的化学方程式为_______ 。
(3)混合气体Ⅳ最适宜返回工序_______ (填序号,只填一项)参与内循环。
(4)工业上常利用电解法制 ,其原理如图(电极均为惰性电极)所示:
,其原理如图(电极均为惰性电极)所示:_______ (填离子符号)离子交换膜。
②电极a的电极反应式为_______ 。
③电路中有0.2mol电子转移时,右侧溶液总质量理论上减少_______ g。
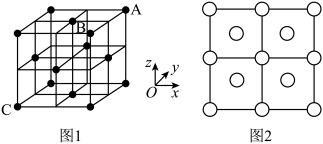
(5)某氮化铬的晶胞结构与氯化钠相似,若该晶胞中N原子的位置如图1所示,请画出晶胞中Cr原子沿x轴方向的投影图(在图2中涂黑相应位置的圆圈)_______ 。
 、
、 )的新工艺如图所示,该工艺不消耗除铬铁矿、氢氧化钠和空气以外的其他原料,也不产生废弃物,能实现Cr-Fe-Al-Mg的深度利用和
)的新工艺如图所示,该工艺不消耗除铬铁矿、氢氧化钠和空气以外的其他原料,也不产生废弃物,能实现Cr-Fe-Al-Mg的深度利用和 的循环利用。
的循环利用。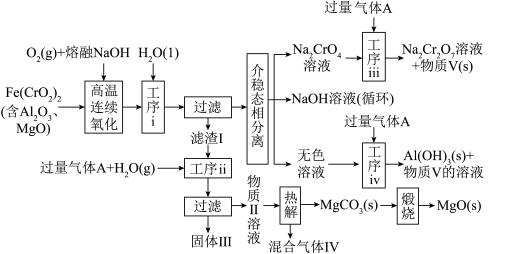
(1)
 中Fe、Cr元素的化合价分别为
中Fe、Cr元素的化合价分别为(2)固体Ⅲ的成分是
(3)混合气体Ⅳ最适宜返回工序
(4)工业上常利用电解法制
 ,其原理如图(电极均为惰性电极)所示:
,其原理如图(电极均为惰性电极)所示:
②电极a的电极反应式为
③电路中有0.2mol电子转移时,右侧溶液总质量理论上减少
(5)某氮化铬的晶胞结构与氯化钠相似,若该晶胞中N原子的位置如图1所示,请画出晶胞中Cr原子沿x轴方向的投影图(在图2中涂黑相应位置的圆圈)
您最近一年使用:0次
7日内更新
|
205次组卷
|
3卷引用:陕西省渭南高级中学2025届高三上学期9月份联考化学试题
4 . 麻黄是一种发散风寒药,其结构简式如图所示。下列关于麻黄的说法正确的是
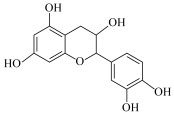
A.分子式为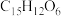 |
B.分子中碳原子均为 杂化 杂化 |
C.理论上1mol麻黄与溴水反应时最多可消耗5mol  |
| D.可以发生取代反应、氧化反应、加成反应和加聚反应 |
您最近一年使用:0次
7日内更新
|
300次组卷
|
3卷引用:陕西省渭南高级中学2025届高三上学期9月份联考化学试题
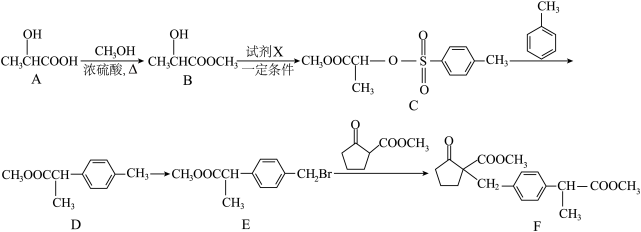
5 . 化合物F可用于治疗急性上呼吸道炎症,F的一种合成路线如下:
(1)A的化学名称为___________ 。
(2)B中官能团的名称是___________ 。
(3)试剂X的分子式为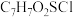 ,其结构简式为
,其结构简式为___________ 。
(4)1个C分子含有___________ 个手性碳原子。
(5)由E生成F的化学方程式为___________ ,其反应类型为___________ 。
(6)在D的同分异构体中,同时满足下列条件的有___________ 种(不包括立体异构),其中核磁共振氢谱显示为4组峰的同分异构体的结构简式为___________ 。
①苯环上只有两个取代基且在对位;
②能与银氨溶液反应生成单质银;
③能发生水解反应,且水解产物之一能与FeCl3溶液发生显色反应。
(1)A的化学名称为
(2)B中官能团的名称是
(3)试剂X的分子式为
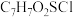 ,其结构简式为
,其结构简式为(4)1个C分子含有
(5)由E生成F的化学方程式为
(6)在D的同分异构体中,同时满足下列条件的有
①苯环上只有两个取代基且在对位;
②能与银氨溶液反应生成单质银;
③能发生水解反应,且水解产物之一能与FeCl3溶液发生显色反应。
您最近一年使用:0次
6 . 某小组设计实验探究 性质,如图所示。下列叙述正确的是
性质,如图所示。下列叙述正确的是
 性质,如图所示。下列叙述正确的是
性质,如图所示。下列叙述正确的是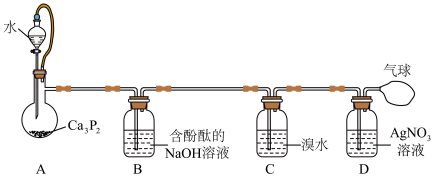
A.装置A中产生 和 和 ,发生了氧化还原反应 ,发生了氧化还原反应 |
B.根据装置B中现象可知, 不能与碱反应 不能与碱反应 |
| C.根据装置C中现象可知,磷的非金属性比溴的强 |
D.装置D中 与 与 反应还原产物只有Ag 反应还原产物只有Ag |
您最近一年使用:0次
7 . 乙醇酸和乳酸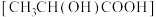 的聚合物是一种新型可降解材料,未来可取代塑料制品以及应用于人体内埋植型修复器械等。高选择性实现甘油在双氧水中被氧化为乙醇酸的反应如图所示。下列叙述正确的是
的聚合物是一种新型可降解材料,未来可取代塑料制品以及应用于人体内埋植型修复器械等。高选择性实现甘油在双氧水中被氧化为乙醇酸的反应如图所示。下列叙述正确的是
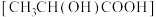 的聚合物是一种新型可降解材料,未来可取代塑料制品以及应用于人体内埋植型修复器械等。高选择性实现甘油在双氧水中被氧化为乙醇酸的反应如图所示。下列叙述正确的是
的聚合物是一种新型可降解材料,未来可取代塑料制品以及应用于人体内埋植型修复器械等。高选择性实现甘油在双氧水中被氧化为乙醇酸的反应如图所示。下列叙述正确的是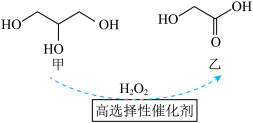
A.向足量酸性 溶液中加入乙可制草酸 溶液中加入乙可制草酸 |
| B.乙和乳酸发生加聚反应生成聚酯可降解材料 |
C.可以用 溶液区别甲和乙 溶液区别甲和乙 |
| D.常温下,甲难溶于水 |
您最近一年使用:0次
8 . 亚硒酸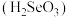 能与酸性
能与酸性 溶液发生如下反应:
溶液发生如下反应: 。下列叙述正确的是
。下列叙述正确的是
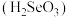 能与酸性
能与酸性 溶液发生如下反应:
溶液发生如下反应: 。下列叙述正确的是
。下列叙述正确的是A.氧化剂与还原剂的物质的量之比为 |
B.在该反应中 表现强氧化性 表现强氧化性 |
C. 完全反应转移 完全反应转移 电子 电子 |
D.分离产物中 宜采用分液操作 宜采用分液操作 |
您最近一年使用:0次
9 . Casnati等报道通过“一锅煮”法制备杯芳烃Q(Bn代表苯甲基)。下列说法正确的是
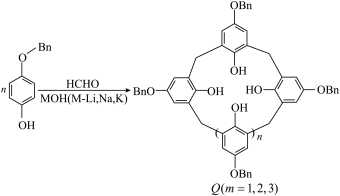
| A.杯芳烃Q分子中所有碳原子一定处于同一平面 |
| B.杯芳烃Q分子内不存在氢键 |
C.杯芳烃Q分子中碳原子均采取 杂化 杂化 |
D. 分子的空间结构为平面三角形 分子的空间结构为平面三角形 |
您最近一年使用:0次
解题方法
10 . 一种从废电池材料中高效回收和利用锂资源的工艺如图。下列叙述错误的是
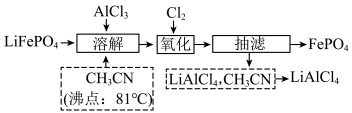
| A.将废电池放电处理时,电能转化为化学能 |
B.“氧化”的目的是将 转化为 转化为 |
C.乙氰 在反应中只作溶剂 在反应中只作溶剂 |
| D.“抽滤”的优点是可以加快过滤速度,使固液分离更彻底 |
您最近一年使用:0次



