解题方法
1 . 一种治疗慢性便秘药品中间体的合成路线如下,回答下列问题。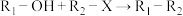
___________ 。
(2)E的结构简式为___________ 。
(3)下列说法正确的是___________。
(4)F→G有一种分子式为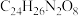 的副产物生成,写出生成该副产物的反应方程式
的副产物生成,写出生成该副产物的反应方程式___________ 。
(5)设计以苯,1,3-丁二烯为原料合成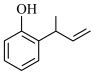 的路线(用流程图表示,无机试剂、有机溶剂任选)
的路线(用流程图表示,无机试剂、有机溶剂任选)___________ 。
(6)写出比E少一个C原子,两个H原子且同时满足以下条件的同分异构体的结构简式___________ 。
①不能与 发生显色反应,但能发生银镜反应
发生显色反应,但能发生银镜反应
② 最多能与
最多能与 溶液恰好完全反应
溶液恰好完全反应
③核磁共振氢谱有4组吸收峰
④分子中没有两个甲基连在同一个碳原子上
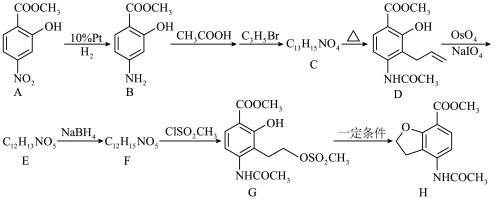
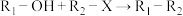
②克莱森重排: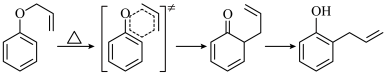
(2)E的结构简式为
(3)下列说法正确的是___________。
A.C能与 发生显色反应 发生显色反应 |
B.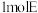 最多能与 最多能与 发生加成反应 发生加成反应 |
| C.B分子中所有碳原子可能共平面 |
| D.图示流程中没有发生克莱森重排反应 |
(4)F→G有一种分子式为
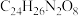 的副产物生成,写出生成该副产物的反应方程式
的副产物生成,写出生成该副产物的反应方程式(5)设计以苯,1,3-丁二烯为原料合成
 的路线(用流程图表示,无机试剂、有机溶剂任选)
的路线(用流程图表示,无机试剂、有机溶剂任选)(6)写出比E少一个C原子,两个H原子且同时满足以下条件的同分异构体的结构简式
①不能与
 发生显色反应,但能发生银镜反应
发生显色反应,但能发生银镜反应②
 最多能与
最多能与 溶液恰好完全反应
溶液恰好完全反应③核磁共振氢谱有4组吸收峰
④分子中没有两个甲基连在同一个碳原子上
您最近一年使用:0次
2024-08-21更新
|
325次组卷
|
2卷引用:浙江省第二届辛愉杯2025届高三上学期线上模拟考试 化学试题
2 . 以黄铜矿(主要成分为 ,含少量
,含少量 )为原料,相关转化关系如下。
)为原料,相关转化关系如下。 不变价,且固体A为单一化合物;
不变价,且固体A为单一化合物;
② 具有疏松结构。
具有疏松结构。
(1)固体A的化学式为___________ ; 中心原子的杂化方式为
中心原子的杂化方式为___________ 。
(2)下列说法不正确 的是___________。
(3)反应2的化学方程式为___________ 。
(4)①反应4生成的物质D难溶于水,且同时生成两种酸性气体,则反应4的化学方程式为___________ 。
②设计实验验证物质D中的氯元素___________ 。
 ,含少量
,含少量 )为原料,相关转化关系如下。
)为原料,相关转化关系如下。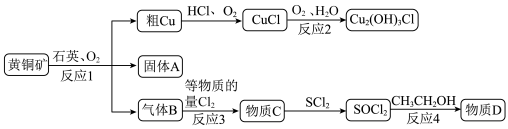
 不变价,且固体A为单一化合物;
不变价,且固体A为单一化合物;②
 具有疏松结构。
具有疏松结构。(1)固体A的化学式为
 中心原子的杂化方式为
中心原子的杂化方式为(2)下列说法
A. 不溶于水,但溶于稀硝酸 不溶于水,但溶于稀硝酸 |
B. 在该环境生锈后,铜锈可隔绝空气,减缓生锈速度 在该环境生锈后,铜锈可隔绝空气,减缓生锈速度 |
| C.气体B具有还原性所以能使品红溶液褪色 |
D. 与 与 混合共热可制得无水 混合共热可制得无水 |
(3)反应2的化学方程式为
(4)①反应4生成的物质D难溶于水,且同时生成两种酸性气体,则反应4的化学方程式为
②设计实验验证物质D中的氯元素
您最近一年使用:0次
3 . “碳达峰”“碳中和”是近年来的热门话题,以二氧化氮和氢气为原料反应时,通常存在以下几个反应:
I.
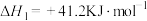
II.
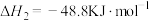
III.
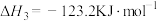
IV.

请回答下列问题。
(1)①
___________ 。
②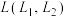 、X分别代表温度或压强,如图表示不同L下,反应III中二甲醚的平衡产率随X变化的关系,判断L1,L2的大小并说明理由
、X分别代表温度或压强,如图表示不同L下,反应III中二甲醚的平衡产率随X变化的关系,判断L1,L2的大小并说明理由___________ 。 的恒容密闭容器中通入
的恒容密闭容器中通入 和
和 发生反应,初始压强为
发生反应,初始压强为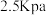 ,达到平衡时,
,达到平衡时, 的转化率为
的转化率为 ,
, 浓度为
浓度为 ,则反应I的
,则反应I的
___________ 。
(3)有科学家提出利用 和
和 制备合成气(
制备合成气( ,
, ),发生的反应为
),发生的反应为 。在体积为
。在体积为 的密闭容器甲和乙中,向甲充入
的密闭容器甲和乙中,向甲充入 和
和 ,向乙中充入
,向乙中充入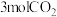 和
和 。
。
①下列说法能表示甲中反应达到平衡的是___________ 。
A.反应速率:
B.同时断裂 键和生成
键和生成 键
键
C.容器内混合气体的压强保持不变
D.容器内混合气体的密度保持不变
②在相同温度下达到平衡状态时, 的转化率α(甲)
的转化率α(甲)___________ α(乙)(填“>”“<”或“=”,下同);达到平衡所需时间t(甲)___________ t(乙)
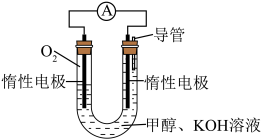
(4)可将反应制得的甲醇设计成如图所示的燃料电池,其中负极的电极反应式为___________ ;若该燃料电池消耗 甲醇,U形管内溶液体积为1L,则溶液中
甲醇,U形管内溶液体积为1L,则溶液中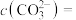
___________ (忽略溶液体积变化)。
I.

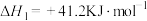
II.

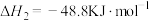
III.

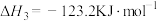
IV.


请回答下列问题。
(1)①

②
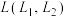 、X分别代表温度或压强,如图表示不同L下,反应III中二甲醚的平衡产率随X变化的关系,判断L1,L2的大小并说明理由
、X分别代表温度或压强,如图表示不同L下,反应III中二甲醚的平衡产率随X变化的关系,判断L1,L2的大小并说明理由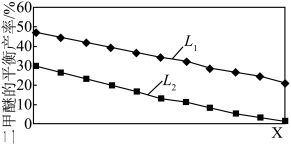
 的恒容密闭容器中通入
的恒容密闭容器中通入 和
和 发生反应,初始压强为
发生反应,初始压强为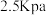 ,达到平衡时,
,达到平衡时, 的转化率为
的转化率为 ,
, 浓度为
浓度为 ,则反应I的
,则反应I的
(3)有科学家提出利用
 和
和 制备合成气(
制备合成气( ,
, ),发生的反应为
),发生的反应为 。在体积为
。在体积为 的密闭容器甲和乙中,向甲充入
的密闭容器甲和乙中,向甲充入 和
和 ,向乙中充入
,向乙中充入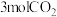 和
和 。
。①下列说法能表示甲中反应达到平衡的是
A.反应速率:

B.同时断裂
 键和生成
键和生成 键
键C.容器内混合气体的压强保持不变
D.容器内混合气体的密度保持不变
②在相同温度下达到平衡状态时,
 的转化率α(甲)
的转化率α(甲)(4)可将反应制得的甲醇设计成如图所示的燃料电池,其中负极的电极反应式为
 甲醇,U形管内溶液体积为1L,则溶液中
甲醇,U形管内溶液体积为1L,则溶液中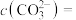
您最近一年使用:0次
解题方法
4 . 利用石灰乳和硝酸工业的尾气反应,既能净化尾气,又能获得应用广泛的 ,已知
,已知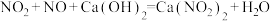 ,下列说法
,下列说法不正确 的是
 ,已知
,已知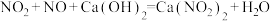 ,下列说法
,下列说法A.氧化剂与还原剂之比为 |
B. 的空间构型为角形 的空间构型为角形 |
C.每生成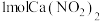 ,有 ,有 电子参与反应 电子参与反应 |
D.当 与 与 的比值为 的比值为 时,反应所得的 时,反应所得的 的纯度最高 的纯度最高 |
您最近一年使用:0次
解题方法
5 . 十二钨硅酸 是一种一种性能优越的多功能催化剂,它的一种制备方法如下(步骤I、II的装置如图所示)。
是一种一种性能优越的多功能催化剂,它的一种制备方法如下(步骤I、II的装置如图所示)。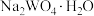 置于三颈烧瓶中,加入蒸馏水剧烈后搅拌至澄清,加热;
置于三颈烧瓶中,加入蒸馏水剧烈后搅拌至澄清,加热;
II.在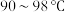 下缓慢加入
下缓慢加入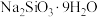 使其充分溶解后,微沸时从滴液漏斗中缓慢地向其中加入浓盐酸,调节
使其充分溶解后,微沸时从滴液漏斗中缓慢地向其中加入浓盐酸,调节 值为2,继续搅拌加热
值为2,继续搅拌加热 ,自然冷却;
,自然冷却;
III.将冷却后的全部液体转移至分液漏斗中,加入乙醚,分多次加入浓盐酸,充分振荡,萃取;
IV.将下层醚合物分出放于蒸发皿中,加水,水浴蒸发至溶液表面有晶体析出时为止,冷却结晶,抽滤,即可得到产品。
(1)装置a的名称是___________ 。
(2)请写出步骤II中生成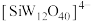 的离子方程式:
的离子方程式:___________ 。
(3)步骤III的详细操作如下,请补充操作a并对下列操作进行排序:a→b→___________ →f,步骤c中放出的气体是___________ 。
a.___________ 。
b.将溶液和乙醚转入分液漏斗并逐滴加入盐酸
c.旋开旋塞放气
d.倒转分液漏斗,小心振荡
e.将分液漏斗置于铁架台上静置
f.打开旋塞,待下层液体完全流出后,关闭旋塞,将上层液体倒出
(4)步骤Ⅳ中为防止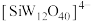 转化为
转化为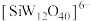 ,可以补充的操作为
,可以补充的操作为___________ 。
(5) 的热重曲线图如图所示,当温度达到
的热重曲线图如图所示,当温度达到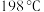 (A点)时,物质中的结晶水全部失去,则化学式中的n=
(A点)时,物质中的结晶水全部失去,则化学式中的n=________ ,A点过后曲线仍有微弱的下降趋势,试推测原因________ 。
 是一种一种性能优越的多功能催化剂,它的一种制备方法如下(步骤I、II的装置如图所示)。
是一种一种性能优越的多功能催化剂,它的一种制备方法如下(步骤I、II的装置如图所示)。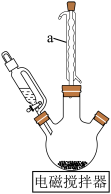
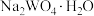 置于三颈烧瓶中,加入蒸馏水剧烈后搅拌至澄清,加热;
置于三颈烧瓶中,加入蒸馏水剧烈后搅拌至澄清,加热;II.在
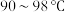 下缓慢加入
下缓慢加入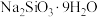 使其充分溶解后,微沸时从滴液漏斗中缓慢地向其中加入浓盐酸,调节
使其充分溶解后,微沸时从滴液漏斗中缓慢地向其中加入浓盐酸,调节 值为2,继续搅拌加热
值为2,继续搅拌加热 ,自然冷却;
,自然冷却;III.将冷却后的全部液体转移至分液漏斗中,加入乙醚,分多次加入浓盐酸,充分振荡,萃取;
IV.将下层醚合物分出放于蒸发皿中,加水,水浴蒸发至溶液表面有晶体析出时为止,冷却结晶,抽滤,即可得到产品。
(1)装置a的名称是
(2)请写出步骤II中生成
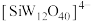 的离子方程式:
的离子方程式:(3)步骤III的详细操作如下,请补充操作a并对下列操作进行排序:a→b→
a.
b.将溶液和乙醚转入分液漏斗并逐滴加入盐酸
c.旋开旋塞放气
d.倒转分液漏斗,小心振荡
e.将分液漏斗置于铁架台上静置
f.打开旋塞,待下层液体完全流出后,关闭旋塞,将上层液体倒出
(4)步骤Ⅳ中为防止
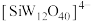 转化为
转化为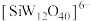 ,可以补充的操作为
,可以补充的操作为(5)
 的热重曲线图如图所示,当温度达到
的热重曲线图如图所示,当温度达到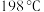 (A点)时,物质中的结晶水全部失去,则化学式中的n=
(A点)时,物质中的结晶水全部失去,则化学式中的n=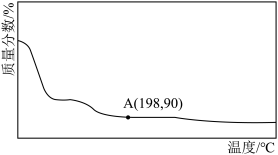
您最近一年使用:0次
2024-08-02更新
|
175次组卷
|
3卷引用:浙江省第二届辛愉杯2025届高三上学期线上模拟考试 化学试题
浙江省第二届辛愉杯2025届高三上学期线上模拟考试 化学试题(已下线)浙江省名校协作体2024-2025学年上学期开学适应性考试高三化学试题浙江省名校协作体2024-2025学年高三上学期9月联考化学试题
6 . 氮及其化合物在生产生活中有重要用途。
(1)同周期第一电离能比N大的元素有___________ (用元素符号表示); 的大π键可表示为
的大π键可表示为___________ 。
(2)三硝基甲苯可用来制作炸药TNT,试从分子结构中分析其易爆炸的原因___________ 。
(3)下列说法不正确 的是___________。
(4)已知 ,
,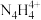 的空间结构均为正四面体形,
的空间结构均为正四面体形, 的结构式为
的结构式为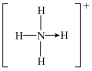 (→表示共用电子对由N原子单方面提供),请画出
(→表示共用电子对由N原子单方面提供),请画出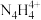 的结构式(要求画出配位键)
的结构式(要求画出配位键)___________ 。
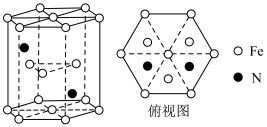
(5) 与N形成的某种化合物晶体的晶体结构如图所示,已知六棱柱底面边长为
与N形成的某种化合物晶体的晶体结构如图所示,已知六棱柱底面边长为 ,高为
,高为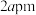 ,阿伏伽德罗常数为
,阿伏伽德罗常数为 ,则该晶体的密度为
,则该晶体的密度为___________  。
。
(1)同周期第一电离能比N大的元素有
 的大π键可表示为
的大π键可表示为(2)三硝基甲苯可用来制作炸药TNT,试从分子结构中分析其易爆炸的原因
(3)下列说法
A. 分子的极性比 分子的极性比 的大 的大 |
B.碱性: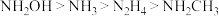 |
C. 的熔点为 的熔点为 ,硬度高,推测它为共价晶体 ,硬度高,推测它为共价晶体 |
D. 中存在配位键,提供空轨道的是B 中存在配位键,提供空轨道的是B |
(4)已知
 ,
,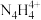 的空间结构均为正四面体形,
的空间结构均为正四面体形, 的结构式为
的结构式为 (→表示共用电子对由N原子单方面提供),请画出
(→表示共用电子对由N原子单方面提供),请画出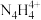 的结构式(要求画出配位键)
的结构式(要求画出配位键)(5)
 与N形成的某种化合物晶体的晶体结构如图所示,已知六棱柱底面边长为
与N形成的某种化合物晶体的晶体结构如图所示,已知六棱柱底面边长为 ,高为
,高为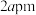 ,阿伏伽德罗常数为
,阿伏伽德罗常数为 ,则该晶体的密度为
,则该晶体的密度为 。
。
您最近一年使用:0次
2024-08-02更新
|
198次组卷
|
3卷引用:浙江省第二届辛愉杯2025届高三上学期线上模拟考试 化学试题
浙江省第二届辛愉杯2025届高三上学期线上模拟考试 化学试题(已下线)浙江省名校协作体2024-2025学年上学期开学适应性考试高三化学试题浙江省名校协作体2024-2025学年高三上学期9月联考化学试题
解题方法
7 . 已知 ,速率方程为
,速率方程为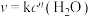 ,其中k为速率常数,只与温度、催化剂、固体接触面积有关,与浓度无关;n为该反应中
,其中k为速率常数,只与温度、催化剂、固体接触面积有关,与浓度无关;n为该反应中 的反应级数,也是该反应总级数,可以为正数、0、负数;起始浓度消耗一半的时间叫半衰期,
的反应级数,也是该反应总级数,可以为正数、0、负数;起始浓度消耗一半的时间叫半衰期, 在某催化剂表面上分解的实验数据如表:
在某催化剂表面上分解的实验数据如表:
下列说法正确的是
 ,速率方程为
,速率方程为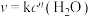 ,其中k为速率常数,只与温度、催化剂、固体接触面积有关,与浓度无关;n为该反应中
,其中k为速率常数,只与温度、催化剂、固体接触面积有关,与浓度无关;n为该反应中 的反应级数,也是该反应总级数,可以为正数、0、负数;起始浓度消耗一半的时间叫半衰期,
的反应级数,也是该反应总级数,可以为正数、0、负数;起始浓度消耗一半的时间叫半衰期, 在某催化剂表面上分解的实验数据如表:
在某催化剂表面上分解的实验数据如表: | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
 | 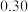 |  | 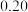 | 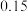 |  |  |  |
A.该反应速率常数为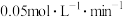 |
| B.该反应为0级反应 |
C.若起始浓度为 ,半衰期为 ,半衰期为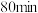 |
| D.工业上用该反应制备氢气 |
您最近一年使用:0次
名校
8 . 根据实验目的设计方案并进行实验,下列方案设计、现象、和结论正确的是
| 目的 | 方案 | 现象 | 结论 | |
| A | 探究浓硫酸的性质 | 取少量蔗糖于烧杯,向其中加入浓硫酸 | 蔗糖变黑,同时膨胀变大 | 浓硫酸具有脱水性及强氧化性 |
| B | 探究温度对化学反应速率的影响 | 取相同的 和 和 分别在冷水和热水中存放,一段时间后将 分别在冷水和热水中存放,一段时间后将 和 和 混合 混合 | 热水组产生气泡的速率快 | 高温可以加快反应速率 |
| C | 比较相同浓度的 和 和 溶液的酸碱性 溶液的酸碱性 | 用洁净干燥的玻璃棒蘸取同浓度的 和 和 溶液,滴在 溶液,滴在 试纸上,并与标准比色卡对比 试纸上,并与标准比色卡对比 |  溶液对应的 溶液对应的 更小 更小 |  溶液的酸性更强 溶液的酸性更强 |
| D | 探究臭氧的极性 | 将集满臭氧的两支试管分别用铁架台固定并倒置在盛有水和 的两个烧杯中 的两个烧杯中 | 倒置在盛有水的烧杯中的试管液面上升较高 | 臭氧是极性分子,在极性溶剂中溶解度大 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-08-02更新
|
297次组卷
|
2卷引用:浙江省第二届辛愉杯2025届高三上学期线上模拟考试 化学试题
解题方法
9 . 目前新能源汽车多采用三元锂电池,某三元锂电池的工作原理如图所示,下列说法正确的是
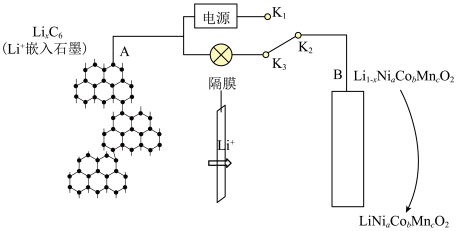
A.充电时,需连接 , , ,且B极为阴极 ,且B极为阴极 |
B.放电时,A极发生的反应为: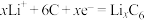 |
| C.放电时,电子流向为A极→用电器→B极→电解质溶液→A极 |
D.外电路每通过 时,通过隔膜的 时,通过隔膜的 质量为 质量为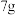 |
您最近一年使用:0次
2024-08-02更新
|
309次组卷
|
3卷引用:浙江省第二届辛愉杯2025届高三上学期线上模拟考试 化学试题
浙江省第二届辛愉杯2025届高三上学期线上模拟考试 化学试题(已下线)浙江省名校协作体2024-2025学年上学期开学适应性考试高三化学试题浙江省名校协作体2024-2025学年高三上学期9月联考化学试题
名校
10 . 已知A、B、C、D、E为原子序数依次增大的前四周期元素。A是宇宙中含量最高的元素,B元素的一种核素可对文物进行年代测定,C元素最高价氧化物对应水化物是常见的最强酸,D元素的焰色试验呈砖红色,基态E+的轨道全部充满。下列说法不正确 的是
| A.A、B两种元素可以形成成千上万种化合物 |
| B.C的单质可用于自来水消毒 |
| C.电负性大小:C>B>A>D |
| D.工业上常用电解C和E的化合物来制备E单质 |
您最近一年使用:0次
2024-08-02更新
|
303次组卷
|
4卷引用:浙江省第二届辛愉杯2025届高三上学期线上模拟考试 化学试题
浙江省第二届辛愉杯2025届高三上学期线上模拟考试 化学试题(已下线)浙江省名校协作体2024-2025学年上学期开学适应性考试高三化学试题浙江省名校协作体2024-2025学年高三上学期9月联考化学试题 2024—2025学年度第一学期高三开学质量检测模拟卷(一)



