名校
1 . 短周期主族元素A、B、C、D的原子序数依次增大,A元素与C元素同主族,B的单质可以在A的单质中燃烧,生成一种具有强氧化性的物质,C元素与D元素相邻,D元素最高价氧化物对应的水化物和氢化物溶于水都能完全电离。下列说法错误的是
| A.元素A与元素B形成的两种化合物中,阴、阳离子个数比都是1:2 |
| B.D的氢化物酸性强于C的氢化物酸性,可证明非金属性:D>C |
| C.可用CS2清洗试管内壁附着的C单质 |
| D.简单离子半径:C>D>A>B |
您最近一年使用:0次
名校
解题方法
2 . 下列是某兴趣小组根据课本实验设计的一个能说明Na2CO3与NaHCO3热稳定性的套管实验。请观察如图实验装置并分析实验原理,判断下列说法错误的是
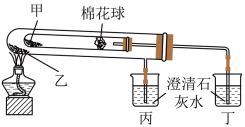
| A.Na2CO3热稳定性大于NaHCO3 |
| B.甲为Na2CO3,乙为NaHCO3 |
| C.要证明物质受热能产生水,可在两支试管内塞上沾有无水硫酸铜粉末的棉花球 |
| D.整个实验过程中可以看到丙烧杯的澄清石灰水不变浑浊 |
您最近一年使用:0次
2024-01-16更新
|
107次组卷
|
4卷引用:宁夏银川市永宁县永宁中学2023-2024学年高一上学期第一次月考化学试卷
名校
解题方法
3 . 下列说法不正确 的是
A.测定0.1 醋酸溶液的 醋酸溶液的 可证明醋酸是弱电解质 可证明醋酸是弱电解质 |
| B.稀释氨水,溶液中c(OH-)减小 |
C.常温下,将1  的盐酸稀释至1L, 的盐酸稀释至1L, 约为 约为 |
D.相同温度下,中和相同 、相同体积的盐酸和醋酸溶液,消耗 、相同体积的盐酸和醋酸溶液,消耗 物质的量不同 物质的量不同 |
您最近一年使用:0次
名校
4 . 我国化学家侯德榜先生发明了联合制碱法,对世界制碱工业做出了巨大贡献。联合制碱法的主要流程如下(部分物质已略去):

(1)①一③所涉及的操作方法中,包含过滤的是___________ (填序号),操作中用到的主要玻璃仪器有烧杯、漏斗和___________ 。
(2)根据上述流程图,将化学方程式补充完整:___________ 。
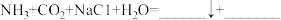
(3)下列关于联合制碱法流程说法正确的是___________ (填字母)。
a.可循环使用的物质有CO2
b.副产物NH4C1可用作氮肥
c.优先通入CO2气体,后通入NH3
(4)该反应能够发生是因为在相同条件下,溶解度:NaCl___________ NaHCO3(填“>”或“<”)。
(5)上述流程中,得到产品纯碱的化学方程式为:___________ 。
(6)鉴别NaHCO3固体中含有NaCl杂质的方法是:取少量固体于试管中,加适量水溶解后,向其中滴加足量的___________ 溶液,然后滴加___________ 溶液,若出现白色沉淀,则证明有NaCl杂质。

(1)①一③所涉及的操作方法中,包含过滤的是
(2)根据上述流程图,将化学方程式补充完整:
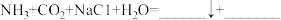
(3)下列关于联合制碱法流程说法正确的是
a.可循环使用的物质有CO2
b.副产物NH4C1可用作氮肥
c.优先通入CO2气体,后通入NH3
(4)该反应能够发生是因为在相同条件下,溶解度:NaCl
(5)上述流程中,得到产品纯碱的化学方程式为:
(6)鉴别NaHCO3固体中含有NaCl杂质的方法是:取少量固体于试管中,加适量水溶解后,向其中滴加足量的
您最近一年使用:0次
名校
解题方法
5 . 石嘴山市施行的《石嘴山市小规模食品生产经营管理规定》中明确规定:小规模食经营者不得购进、存放、使用亚硝酸盐等易滥用的食品添加剂。
(1)根据物质组成分类,亚硝酸钠(NaNO2)属于___________ (填序号),写出其电离方程式:___________ 。
A.钠盐 B.硝酸盐 C.氧化物
(2)实验室中,亚硝酸钠可用来处理过量的叠氮化钠,有关反应的化学方程式如下:
a. NaNO2+H2SO4=HNO2+NaHSO4
b. 2NaN3+2HNO2=3N2↑+2NO↑+2NaOH
上述氧化还原反应中的氧化剂与还原剂的比值为___________ ,反应生成3个N2转移的电子数为___________ 。
(3)亚硝酸钠外观与食盐相似,且均有咸味。
①若误食亚硝酸钠会导致血红蛋白中的亚铁离子转化为铁离子而中毒,服用维生素C可解除亚硝酸钠的中毒,下列关于上述中毒、解毒过程的说法中正确的是___________ (填序号)。
A. 亚硝酸钠是还原剂 B.维生素C是氧化剂
C. 维生素C能把铁离子还原成为亚铁离子 D.亚硝酸钠被还原
②鉴别方法如下:将样品盐放入稀硫酸与另外一种溶液(溶质为X)的混合液中,振荡,再滴加淀粉溶液,如果溶液显蓝色,则可以证明该样品盐是亚硝酸钠,如果溶液颜色无变化,则证明该样品盐为氯化钠。X与亚硝酸钠发生的反应可表示为2NaNO2 + 2X + 2H2SO4 = 2NO↑ + I2 + K2SO4 + Na2SO4 + 2H2O(已配平),其中X是___________ (填化学式)该反应的离子方程式为___________ 。
③含NaNO2的废水必须经处理后才能排放,用铵盐来处理亚硝酸钠反应生成一种无毒气体写出该反应的离子方程式:___________ 。
(1)根据物质组成分类,亚硝酸钠(NaNO2)属于
A.钠盐 B.硝酸盐 C.氧化物
(2)实验室中,亚硝酸钠可用来处理过量的叠氮化钠,有关反应的化学方程式如下:
a. NaNO2+H2SO4=HNO2+NaHSO4
b. 2NaN3+2HNO2=3N2↑+2NO↑+2NaOH
上述氧化还原反应中的氧化剂与还原剂的比值为
(3)亚硝酸钠外观与食盐相似,且均有咸味。
①若误食亚硝酸钠会导致血红蛋白中的亚铁离子转化为铁离子而中毒,服用维生素C可解除亚硝酸钠的中毒,下列关于上述中毒、解毒过程的说法中正确的是
A. 亚硝酸钠是还原剂 B.维生素C是氧化剂
C. 维生素C能把铁离子还原成为亚铁离子 D.亚硝酸钠被还原
②鉴别方法如下:将样品盐放入稀硫酸与另外一种溶液(溶质为X)的混合液中,振荡,再滴加淀粉溶液,如果溶液显蓝色,则可以证明该样品盐是亚硝酸钠,如果溶液颜色无变化,则证明该样品盐为氯化钠。X与亚硝酸钠发生的反应可表示为2NaNO2 + 2X + 2H2SO4 = 2NO↑ + I2 + K2SO4 + Na2SO4 + 2H2O(已配平),其中X是
③含NaNO2的废水必须经处理后才能排放,用铵盐来处理亚硝酸钠反应生成一种无毒气体写出该反应的离子方程式:
您最近一年使用:0次
名校
6 . 某白色固体粉末由KNO3、NaCl、CuSO4、CaCO3、BaCl2中的一种或几种组成,进行如下实验:①进行焰色反应,透过蓝色钴玻璃火焰颜色呈紫色;②混合物溶于水,得到澄清溶液;③向②所得的溶液中通入少量NH3,产生沉淀。下列说法不正确的是
| A.实验①证明固体粉末中一定含有KNO3 |
| B.实验②证明固体粉末中一定不含CaCO3 |
| C.实验③证明固体粉末中一定含有CuSO4 |
| D.实验①②③证明固体粉末中可能含有BaCl2、NaCl |
您最近一年使用:0次
7 . 据报道有不法明胶企业将皮革废料熬制成工业明胶,出售给某些制药企业,最终变成药用胶囊。由工业明胶制成的胶囊往往含有超标的重金属铬(Cr),从而对人体造成伤害。明胶是水溶性蛋白质混合物,溶于水形成胶体。
(1)已知CrO 是一种酸根离子,则Fe(CrO2)2属于
是一种酸根离子,则Fe(CrO2)2属于_______ (填“酸”“碱”“盐”或“氧化物”)。
(2)明胶与水构成的分散系和K2SO4溶液共同具备的性质是_______ (填标号)。
A.都不稳定,密封放置产生沉淀
B.两者均能产生丁达尔效应
C.分散质微粒可通过滤纸
(3)已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。提纯明胶的装置是下列装置中的_______ (填标号)。
A. B.
B.  C.
C.
(4)现有10 mL明胶与水构成的分散系与5 mL Na2SO4溶液混合装入半透膜内,将此半透膜浸入盛蒸馏水的烧杯中,证明Na2SO4能透过半透膜的实验操作是:取烧杯中的少量液体,向其中加入稀盐酸,再加入_______ ,若产生_______ ,则证明Na2SO4能透过半透膜。
(5)下列关于胶体的说法正确的是_______(填标号)。
(1)已知CrO
 是一种酸根离子,则Fe(CrO2)2属于
是一种酸根离子,则Fe(CrO2)2属于(2)明胶与水构成的分散系和K2SO4溶液共同具备的性质是
A.都不稳定,密封放置产生沉淀
B.两者均能产生丁达尔效应
C.分散质微粒可通过滤纸
(3)已知胶体的分散质不能透过半透膜,但水分子等小分子或离子能透过半透膜。提纯明胶的装置是下列装置中的
A.
 B.
B.  C.
C.
(4)现有10 mL明胶与水构成的分散系与5 mL Na2SO4溶液混合装入半透膜内,将此半透膜浸入盛蒸馏水的烧杯中,证明Na2SO4能透过半透膜的实验操作是:取烧杯中的少量液体,向其中加入稀盐酸,再加入
(5)下列关于胶体的说法正确的是_______(填标号)。
| A.制备氢氧化铁胶体时,可以用蒸馏水,也可以用自来水 |
| B.按照分散剂的不同,胶体可分为液溶胶、气溶胶和固溶胶 |
| C.氢氧化铁胶体属于电解质 |
| D.已知土壤胶体中的胶粒带负电,在土壤中施用含氮总量相同的(NH4)2SO4与NH4NO3,肥效相同 |
您最近一年使用:0次
2022-10-10更新
|
340次组卷
|
4卷引用:宁夏吴忠市吴忠中学2022-2023学年高一上学期第一次测试化学试题(B卷)
名校
解题方法
8 . 将电能转化为化学能在生活、生产和科学研究中具有重要意义。某学习小组用石墨电极持续电解 溶液。
溶液。
(1)下列说法中正确的是___________ (填序号)。
①a极是阳极 ②通电后 开始电离
开始电离
③通电后 和
和 向阳极移动 ④总反应为:
向阳极移动 ④总反应为: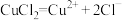
(2) 时刻,a极的电极反应式为
时刻,a极的电极反应式为___________ 。
(3) ~
~ ,b极产生刺激性气体,能使湿润的KI淀粉试纸变蓝,该气体是
,b极产生刺激性气体,能使湿润的KI淀粉试纸变蓝,该气体是___________ 。
(4)为证明a极的白色沉淀是CuCl,从a极刮取白色沉淀(含少量红色固体),进行如下实验:
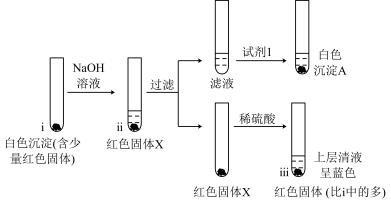
资料卡片:
①向试管i中加入NaOH溶液,生成的黄色沉淀很快转变为红色,补全物质的转化过程:CuCl→___________ → 。
。
②白色沉淀A为AgCl,试剂1是___________ 。
(5)针对CuCl沉淀是如何产生的,小组提出两种假设。
假设1:由氧化还原反应产生的,离子方程式为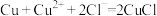
假设2:由电极反应产生:___________ 。
(6) 时a极未产生气体,而
时a极未产生气体,而 时a极产生气体,该气体可能是
时a极产生气体,该气体可能是___________ 。
 溶液。
溶液。| 实验 | 时刻 | 现象 |
 |  | a极析出红色固体b极产生气体 |
 | a极产生白色沉淀;a极附近溶液变为黄绿色;b极产生气体 | |
| … | …… | |
 | a极产生气体;b极产生气体 |
(1)下列说法中正确的是
①a极是阳极 ②通电后
 开始电离
开始电离 ③通电后
 和
和 向阳极移动 ④总反应为:
向阳极移动 ④总反应为: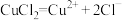
(2)
 时刻,a极的电极反应式为
时刻,a极的电极反应式为(3)
 ~
~ ,b极产生刺激性气体,能使湿润的KI淀粉试纸变蓝,该气体是
,b极产生刺激性气体,能使湿润的KI淀粉试纸变蓝,该气体是(4)为证明a极的白色沉淀是CuCl,从a极刮取白色沉淀(含少量红色固体),进行如下实验:

资料卡片:
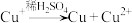 ,CuOH(黄色,不溶)→ ,CuOH(黄色,不溶)→ (红色,不溶) (红色,不溶) |
 。
。②白色沉淀A为AgCl,试剂1是
(5)针对CuCl沉淀是如何产生的,小组提出两种假设。
假设1:由氧化还原反应产生的,离子方程式为
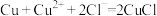
假设2:由电极反应产生:
(6)
 时a极未产生气体,而
时a极未产生气体,而 时a极产生气体,该气体可能是
时a极产生气体,该气体可能是
您最近一年使用:0次
2024-01-21更新
|
97次组卷
|
3卷引用:宁夏回族自治区石嘴山市第三中学2023-2024学年高二上学期1月期末化学试题
宁夏回族自治区石嘴山市第三中学2023-2024学年高二上学期1月期末化学试题北京市西城外国语学校2023-2024学年高二上学期期中考试化学试题(已下线)专题08 电解池 金属的腐蚀与防护-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)
名校
9 . 中国地质科学院地质研究所对嫦娥五号月球玄武岩开展了年代学、元素、同位素分析,证明月球在19.6亿年前仍存在岩浆活动。A、B、C、D、E是月核中含有的五种原子序数依次增大的前20号元素,A、D同族,D的单质常在地球火山口附近沉积,B、D、E最高价氧化物的水化物可以两两反应,C是地壳中含量第二的元素。下列说法错误的是
| A.简单离子半径:E>D>B |
| B.简单氢化物的稳定性:A>D |
| C.A与C形成的化合物是制备玻璃的原料之一 |
| D.单质C广泛应用于信息技术和新能源技术等领域 |
您最近一年使用:0次
2023-05-15更新
|
355次组卷
|
3卷引用:宁夏石嘴山第三中学2023-2024学年高三上学期期中考试化学试题
名校
10 . 下图是元素周期表的一部分。按要求填写下列空白:

(1)元素⑦在周期表中的位置为_______ 。
(2)④、⑧、⑨的简单离子半径的大小顺序为_______ (填离子符号)。
(3)①~⑩元素的最高价氧化物对应的水化物中,酸性最强的是_______ (填化学式)。
(4)④⑧⑨三种元素形成的气态氢化物稳定性由大到小的顺序是_______ (用化学式表示)。
(5)⑤的最高价氧化物对应的水化物中所含的化学键为_______ ;③的氢化物的电子式为_______ 。
(6)为了证明⑤和⑥两种元素的金属性强弱,下列说法或实验能提供证据的是_______ 。
A.比较两种元素的单质的熔点、沸点高低
B.将两种元素的单质分别与冷水反应,观察反应的剧烈程度
C.比较两种元素的最高价氧化物对应的水化物的碱性强弱

(1)元素⑦在周期表中的位置为
(2)④、⑧、⑨的简单离子半径的大小顺序为
(3)①~⑩元素的最高价氧化物对应的水化物中,酸性最强的是
(4)④⑧⑨三种元素形成的气态氢化物稳定性由大到小的顺序是
(5)⑤的最高价氧化物对应的水化物中所含的化学键为
(6)为了证明⑤和⑥两种元素的金属性强弱,下列说法或实验能提供证据的是
A.比较两种元素的单质的熔点、沸点高低
B.将两种元素的单质分别与冷水反应,观察反应的剧烈程度
C.比较两种元素的最高价氧化物对应的水化物的碱性强弱
您最近一年使用:0次
2023-01-31更新
|
191次组卷
|
2卷引用:宁夏青铜峡市宁朔中学2022-2023学年高一下学期3月月考化学试题



