1 . 下列分散系中分散质直径最小的是
| A.氢氧化铁悬浊液 | B.氢氧化铝胶体 |
| C.淀粉溶液 | D.硫酸铜溶液 |
您最近一年使用:0次
2 . 黑火药是中国古代四大发明之一,其爆炸反应为2KNO3+S+3C=K2S+N2↑+3CO2↑。下列说法正确的是
| A.黑火药中含有两种单质 | B.反应中C作为氧化剂 |
| C.反应中S作还原剂 | D.反应为置换反应 |
您最近一年使用:0次
名校
3 . 滴定是一种重要的定量实验方法:
Ⅰ.酸碱中和滴定:常温下,用0.1000mol/L NaOH溶液分别滴定20.00mL 等浓度的盐酸和醋酸溶液,得到两条滴定曲线,如下图所示:
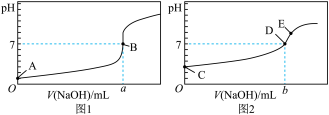
(1)滴定盐酸的曲线是图_______ (填“1”或“2”)
(2)达到B、D状态时,反应消耗的NaOH溶液的体积a_______ b(填“>”“<”或“=”)
Ⅱ.氧化还原滴定原理与中和滴定原理相似, 为了测定某草酸样品的纯度,进行如下实验:称取w g草酸晶体,配成100.00mL水溶液,取25.00mL所配制的草酸溶液置于锥形瓶内,加入适量稀H2SO4后,用浓度为a mol•L﹣1的KMnO4溶液滴定到KMnO4不再褪色为止,所发生的反应为:2KMnO4 + 5H2C2O4 + 3H2SO4 = K2SO4 +10CO2↑ + 2MnSO4 +8H2O。试回答:
(3)实验中,标准液KMnO4溶液应装在_______ 中。
(4)实验中眼睛注视锥形瓶内溶液颜色的变化,直至滴定终点。判断到达终点的现象是_____ 。
(5)若滴定开始和结束时,盛装KMnO4溶液的滴定管中的液面如图所示,则所用KMnO4溶液的体积为______ mL。以此计算出该草酸样品的纯度为____ 。(用“a”和“w”表示)

(6)实验中,下列操作(其它操作均正确),会使所测草酸浓度偏大的是____ 。
A.滴定前俯视刻度,滴定后仰视刻度
B.锥形瓶在盛放待测液前未干燥,有少量蒸馏水
C.滴定过程中摇动锥形瓶,不慎将瓶内的溶液溅出一部分
Ⅰ.酸碱中和滴定:常温下,用0.1000mol/L NaOH溶液分别滴定20.00mL 等浓度的盐酸和醋酸溶液,得到两条滴定曲线,如下图所示:

(1)滴定盐酸的曲线是图
(2)达到B、D状态时,反应消耗的NaOH溶液的体积a
Ⅱ.氧化还原滴定原理与中和滴定原理相似, 为了测定某草酸样品的纯度,进行如下实验:称取w g草酸晶体,配成100.00mL水溶液,取25.00mL所配制的草酸溶液置于锥形瓶内,加入适量稀H2SO4后,用浓度为a mol•L﹣1的KMnO4溶液滴定到KMnO4不再褪色为止,所发生的反应为:2KMnO4 + 5H2C2O4 + 3H2SO4 = K2SO4 +10CO2↑ + 2MnSO4 +8H2O。试回答:
(3)实验中,标准液KMnO4溶液应装在
(4)实验中眼睛注视锥形瓶内溶液颜色的变化,直至滴定终点。判断到达终点的现象是
(5)若滴定开始和结束时,盛装KMnO4溶液的滴定管中的液面如图所示,则所用KMnO4溶液的体积为

(6)实验中,下列操作(其它操作均正确),会使所测草酸浓度偏大的是
A.滴定前俯视刻度,滴定后仰视刻度
B.锥形瓶在盛放待测液前未干燥,有少量蒸馏水
C.滴定过程中摇动锥形瓶,不慎将瓶内的溶液溅出一部分
您最近一年使用:0次
名校
解题方法
4 . 用下列实验装置进行的相应实验,能达到实验目的的是
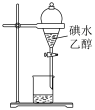 |  | 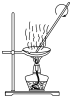 | 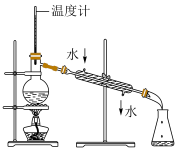 |
| 图1 | 图2 | 图3 | 图4 |
| A.图1所示装置可萃取碘水中的碘 |
| B.图2所示装置可测定反应过程中所放出的热量计算中和热 |
| C.图3所示装置蒸发MgCl2溶液得氯化镁晶体 |
| D.图4所示装置可分离两种互溶但沸点相差较大的液体混合物 |
您最近一年使用:0次
名校
解题方法
5 . 下列实验现象(或操作)与盐类水解有关的是
①NH4Cl与ZnCl2溶液可作焊接金属中的除锈剂
② 1 mol/L的醋酸加水稀释,溶液的pH增大,导电能力减弱
③用Al2(SO4)3与NaHCO3两种溶液作泡沫灭火剂
④ 配制FeCl3溶液时,将FeCl3固体溶解在浓盐酸中,再用水稀释到所需浓度
⑤氮肥NH4HCO3与钾肥K2CO3混施可能会降低肥效
①NH4Cl与ZnCl2溶液可作焊接金属中的除锈剂
② 1 mol/L的醋酸加水稀释,溶液的pH增大,导电能力减弱
③用Al2(SO4)3与NaHCO3两种溶液作泡沫灭火剂
④ 配制FeCl3溶液时,将FeCl3固体溶解在浓盐酸中,再用水稀释到所需浓度
⑤氮肥NH4HCO3与钾肥K2CO3混施可能会降低肥效
| A.①③④⑤ | B.①②③④ | C.①②④⑤ | D.②③④⑤ |
您最近一年使用:0次
名校
解题方法
6 . 用如图所示的装置电解K2SO4溶液同时制备H2SO4和KOH溶液,Ⅱ中装入K2SO4溶液,下列有关分析正确的是(a、b是离子交换膜)


| A.Ⅰ区生成H2SO4 | B.b是阳离子交换膜 |
| C.Ⅱ区中的K+进入Ⅰ区 | D.Ⅲ区溶液的pH会升高 |
您最近一年使用:0次
名校
解题方法
7 . X、Y、Z、W、Q是原子序数依次增大的5种短周期主族元素,X元素的一种核素的中子数为0,X与Z、Y与W处于同一主族,W的最内层电子数和最外层电子数之和等于次外层电子数。下列说法中错误的是
| A.原子半径:Q>W>Z>Y>X |
| B.最简单氢化物的沸点:Y>W |
| C.化合物ZQY和XQY中化学键的类型不同 |
| D.由Z、W、Y形成的一种化合物加入水中能促进水的电离 |
您最近一年使用:0次
名校
解题方法
8 . 常温下,下列各组离子在指定溶液中能大量共存的是
A.无色透明的溶液中:Al3+、Fe3+、 、S2- 、S2- |
B.含0.1 mol·L−1的FeCl2溶液中:H+、Al3+、 、 、 |
C.加入Al单质生成气体的溶液:Na+、 、 、 、Cl − 、Cl − |
D.常温下,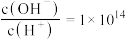 的溶液中:K+、Na+、I−、 的溶液中:K+、Na+、I−、 |
您最近一年使用:0次
名校
9 . NA代表阿伏加德罗常数的数值。下列说法不正确的是
| A.0.1mol液态NaHSO4中含有0.1NA个阳离子 |
| B.当氢氧燃料电池正极消耗11.2 L气体时,电路中通过电子的数目为2NA |
| C.常温下,1 L 1 mol·L−1盐酸与46 g钠反应生成H2分子的数目为NA |
| D.在电解精炼粗铜的过程中,当阴极析出32 g铜时转移电子数目为NA |
您最近一年使用:0次
名校
10 . 当氢氧化钙固体在水中达到溶解平衡时,为使Ca(OH)2固体的量减少,可以加入少量的
| A.NaOH固体 | B.CaCl2固体 | C.NH4NO3固体 | D.Ca(OH)2固体 |
您最近一年使用:0次



