1 . 某工厂采用软锰矿(主要成分为 )与辉铋矿(主要成分为
)与辉铋矿(主要成分为 ,含有
,含有 、
、 杂质)联合焙烧法制备电池级的
杂质)联合焙烧法制备电池级的 和BiOCl,工艺流程如下:
和BiOCl,工艺流程如下:

已知:①焙烧时过量的 分解为
分解为 ,加热时
,加热时 在酸性溶液中转化为
在酸性溶液中转化为 和Mn²⁺,MnO与酸反应生成
和Mn²⁺,MnO与酸反应生成 ;
;
②金属活动性顺序:Fe>(H)>Bi>Cu;
③相关金属离子形成氢氧化物的pH范围:
④BiOCl的式量:260.5
回答下列问题:
(1)下列有关说法错误的是___________。
(2) 经热解、酸浸等步骤可制备
经热解、酸浸等步骤可制备 。
。 在空气气流中热解得到三种价态锰的氧化物,锰元素所占比例(某价态锰的元素的中锰元素质量×100%)随热解温度变化的曲线如图所示。为获得较高产率的
在空气气流中热解得到三种价态锰的氧化物,锰元素所占比例(某价态锰的元素的中锰元素质量×100%)随热解温度变化的曲线如图所示。为获得较高产率的 ,请选出正确操作并按序排列:取一定量
,请选出正确操作并按序排列:取一定量 置于热解装置中,通空气气流,
置于热解装置中,通空气气流,___________ ,充分反应后过滤、洗涤、干燥,得到 。
。

a.冷却至室温
b.加热到450℃分解一段时间
c.加热到480℃分解一段时间
d.边搅拌边加入一定量1 mol⋅L-1的 溶液
溶液
e.边搅拌边加入一定量1 mol⋅L-1的HCl溶液0
(3)BiOCl含量的测定。称取产品0.1302g于锥形瓶中,加15 mL 36%的盐酸溶解,加掩蔽剂防止杂质离子对终点判断产生干扰,调pH至1.5~1.8,加入饱和硫脲与 形成黄色络合物,再用0.0200 mol⋅L-1的EDTA滴定至终点,消耗溶液22.50 mL。已知EDTA与
形成黄色络合物,再用0.0200 mol⋅L-1的EDTA滴定至终点,消耗溶液22.50 mL。已知EDTA与 1∶1发生络合反应,所得产物的稳定性远大于硫脲与
1∶1发生络合反应,所得产物的稳定性远大于硫脲与 形成的黄色络合物。
形成的黄色络合物。
①根据滴定实验测得的数据计算,产品的质量分数为___________ 。
②临近滴定终点时的操作方法是:将旋塞稍稍转动,使半滴溶液悬于管口,___________ ,再用洗瓶以少量蒸馏水吹洗锥形瓶内壁,直到滴入最后半滴EDTA,溶液恰好由黄色变为无色,半分钟内不变色。
③下列关于滴定分析的操作,错误的是___________ 。
A.装入滴定管中的溶液无需用量筒量取
B.滴定时要适当控制滴定速度
C.滴定时应一直观察滴定管中溶液体积的变化
D.读数时应将滴定管从架上取下,捏住管上端无刻度处,使滴定管保持垂直
E.①中计算所得数据即为产品纯度
 )与辉铋矿(主要成分为
)与辉铋矿(主要成分为 ,含有
,含有 、
、 杂质)联合焙烧法制备电池级的
杂质)联合焙烧法制备电池级的 和BiOCl,工艺流程如下:
和BiOCl,工艺流程如下:
已知:①焙烧时过量的
 分解为
分解为 ,加热时
,加热时 在酸性溶液中转化为
在酸性溶液中转化为 和Mn²⁺,MnO与酸反应生成
和Mn²⁺,MnO与酸反应生成 ;
;②金属活动性顺序:Fe>(H)>Bi>Cu;
③相关金属离子形成氢氧化物的pH范围:
| 开始沉淀pH | 完全沉淀pH | |
 | 6.5 | 8.3 |
 | 1.6 | 2.8 |
 | 8.1 | 10.1 |
回答下列问题:
(1)下列有关说法错误的是___________。
A.焙烧时,只有 是还原剂 是还原剂 |
| B.为提高焙烧效率,鼓入适当过量的空气 |
C.滤渣A是 ,气体A是 ,气体A是 |
D.加入金属铋的作用是将 转化为Fe 转化为Fe |
 经热解、酸浸等步骤可制备
经热解、酸浸等步骤可制备 。
。 在空气气流中热解得到三种价态锰的氧化物,锰元素所占比例(某价态锰的元素的中锰元素质量×100%)随热解温度变化的曲线如图所示。为获得较高产率的
在空气气流中热解得到三种价态锰的氧化物,锰元素所占比例(某价态锰的元素的中锰元素质量×100%)随热解温度变化的曲线如图所示。为获得较高产率的 ,请选出正确操作并按序排列:取一定量
,请选出正确操作并按序排列:取一定量 置于热解装置中,通空气气流,
置于热解装置中,通空气气流, 。
。
a.冷却至室温
b.加热到450℃分解一段时间
c.加热到480℃分解一段时间
d.边搅拌边加入一定量1 mol⋅L-1的
 溶液
溶液e.边搅拌边加入一定量1 mol⋅L-1的HCl溶液0
(3)BiOCl含量的测定。称取产品0.1302g于锥形瓶中,加15 mL 36%的盐酸溶解,加掩蔽剂防止杂质离子对终点判断产生干扰,调pH至1.5~1.8,加入饱和硫脲与
 形成黄色络合物,再用0.0200 mol⋅L-1的EDTA滴定至终点,消耗溶液22.50 mL。已知EDTA与
形成黄色络合物,再用0.0200 mol⋅L-1的EDTA滴定至终点,消耗溶液22.50 mL。已知EDTA与 1∶1发生络合反应,所得产物的稳定性远大于硫脲与
1∶1发生络合反应,所得产物的稳定性远大于硫脲与 形成的黄色络合物。
形成的黄色络合物。①根据滴定实验测得的数据计算,产品的质量分数为
②临近滴定终点时的操作方法是:将旋塞稍稍转动,使半滴溶液悬于管口,
③下列关于滴定分析的操作,错误的是
A.装入滴定管中的溶液无需用量筒量取
B.滴定时要适当控制滴定速度
C.滴定时应一直观察滴定管中溶液体积的变化
D.读数时应将滴定管从架上取下,捏住管上端无刻度处,使滴定管保持垂直
E.①中计算所得数据即为产品纯度
您最近一年使用:0次
2 . 下列说法正确的是
| A.所有α-氨基酸都存在对映异构体 |
| B.淀粉、纤维素、蛋白质和核苷酸都属于高分子化合物 |
C.以CO和 为原料,通过加成反应可合成液态烃和甲醇等有机物 为原料,通过加成反应可合成液态烃和甲醇等有机物 |
| D.石油裂解的产物除了乙烯、丙烯等不饱和烃外,还含有甲烷、乙烷等 |
您最近一年使用:0次
名校
3 . 下列实验装置(部分夹持装置略)或现象错误的是
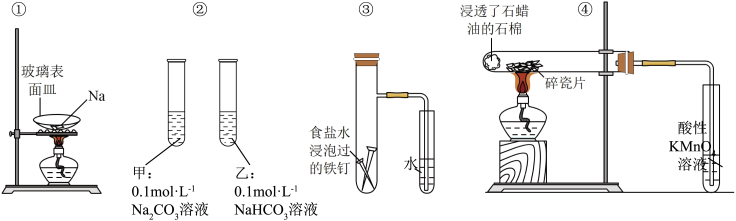

| A.图①:观察到钠燃烧的火焰颜色为黄色,且有淡黄色固体生成 |
| B.图②:两支试管中滴入酚酞溶液后,甲中溶液为红色,乙中溶液为浅红色 |
| C.图③:一段时间后,观察到右侧导管有一段高于液面的水柱 |
D.图④:石蜡油受热分解,右侧试管盛放的酸性 溶液褪色 溶液褪色 |
您最近一年使用:0次
2023-07-15更新
|
210次组卷
|
2卷引用:浙江省嘉兴市2022届高三一模考试化学试题
4 . 某化学兴趣小组在老师指导下进行课外实验,利用下列装置来探究磷单质在空气中燃烧后氧气浓度变化情况。
[提出问题]足量红磷在密闭的四颈平底烧瓶内燃烧熄灭后,容器中是否有氧气剩余
[猜想假设]猜想①:有氧气剩余
猜想②:无氧气剩余
[实验验证]该小组同学按图组装好实验装置,利用高能激光笔照射燃烧匙上的红磷,红磷燃烧直至熄灭;待装置完全冷却后,将装有白磷的燃烧匙提出水面,再次用高能激光笔照射,白磷居然也被点燃。

(1)激光笔的作用是_____ 。
(2)实验过程中,刚开始即使用激光笔照射,燃烧匙内的白磷也不会燃烧的原因是_____ 。
[实验结论]根据上述实验,得出结论如下:
(3)用“燃磷法测定空气中氧气含量”时,选择_____ (填“红磷”或“白磷”)更合适,理由是_____ 。
[拓展延伸]如图是该小组同学从开始实验到最后装置冷却后的整个实验过程中,用氧气传感器测量容器内氧气浓度变化的曲线图。

(4)请你解释上图曲线AB段氧气浓度变化的主要原因_____ 。
(5)小组同学通过查阅资料得知,验证空气中氧气体积分数较好的药品是铁丝绒,利用铁与氧气、水等的缓慢氧化,可将空气中氧气浓度消耗至0.2%。将足量细铁丝绒置于试管底部,并倒扣在装有水的烧杯中(如图),一段时间后你将看到的现象是_____ 。

[提出问题]足量红磷在密闭的四颈平底烧瓶内燃烧熄灭后,容器中是否有氧气剩余
[猜想假设]猜想①:有氧气剩余
猜想②:无氧气剩余
[实验验证]该小组同学按图组装好实验装置,利用高能激光笔照射燃烧匙上的红磷,红磷燃烧直至熄灭;待装置完全冷却后,将装有白磷的燃烧匙提出水面,再次用高能激光笔照射,白磷居然也被点燃。

(1)激光笔的作用是
(2)实验过程中,刚开始即使用激光笔照射,燃烧匙内的白磷也不会燃烧的原因是
[实验结论]根据上述实验,得出结论如下:
(3)用“燃磷法测定空气中氧气含量”时,选择
[拓展延伸]如图是该小组同学从开始实验到最后装置冷却后的整个实验过程中,用氧气传感器测量容器内氧气浓度变化的曲线图。

(4)请你解释上图曲线AB段氧气浓度变化的主要原因
(5)小组同学通过查阅资料得知,验证空气中氧气体积分数较好的药品是铁丝绒,利用铁与氧气、水等的缓慢氧化,可将空气中氧气浓度消耗至0.2%。将足量细铁丝绒置于试管底部,并倒扣在装有水的烧杯中(如图),一段时间后你将看到的现象是

您最近一年使用:0次
21-22高一上·浙江·阶段练习
5 . 英国科学家法拉第曾用蜡烛(主要成分是石蜡)为少年儿童做过一个有趣的“母子火焰”实验如图所示,下列说法正确的是


| A.这一现象说明石蜡的熔点比较低 |
| B.子火焰被燃烧的物质是石蜡分解产生的气体氢气 |
| C.导管的一端要插入母火焰的中心部位是因为该处氧气充足 |
| D.实验时宜使用管径大点的导管 |
您最近一年使用:0次
6 . 证据推理是化学学科核心素养的重要内容,下列说法正确的是
| A.化合物由不同元素组成,因此含有不同种元素的物质一定是化合物 |
| B.氢氧混合气体点燃会有爆炸声,因此点燃有爆鸣声现象的气体一定含有氢气 |
| C.金刚石、石墨、足球烯(C60)都是由碳元素组成的单质,因此它们的性质相同 |
| D.铜在空气中久置后表面生成铜绿(Cu2(OH)2CO3),说明铜的锈蚀和水、空气有关,这与铁的锈蚀原理相似 |
您最近一年使用:0次
21-22高一上·浙江·阶段练习
名校
7 . 据权威杂志《Nature》报道:科学家在距离地球3000光年的一个年轻的行星状星云NGC7027中,首次发现宇宙中最早的化学反应产物氦合氢离子(HeH+)(其模型如图所示),科学家认为氦合氢离子是宇宙中最早的氢气来源,并于1925年就在实验室中合成了HeH+,下列说法正确的是


| A.一个氦合氢离子有3个电子 |
| B.如图模型中大球为H+ |
| C.宇宙中早形成的元素是相对原子质量大的元素 |
| D.推测HeH+可能具有强酸性 |
您最近一年使用:0次
解题方法
8 . 工业上利用电解饱和食盐水可制得重要化工产品,该工业又称为“氯碱工业”。
(1)电解饱和食盐水的化学方程式为_______ ;常用_______ 检验与电源正极相连的电极上产生的气体,相关的化学方程式为_______ 。
(2)新制的氯水具有杀菌消毒,漂白作用。研究证明,溶解在水中的部分氯气能与水发生反应,其反应的化学方程式为_______ ;氯水不稳定,需现用现配,下列制备氯水的装置最合理的是_______ (填字母)。

(3)氯水不稳定,生活中常用漂白粉进行杀菌消毒。工业上以氯气和石灰乳为原料制备漂白粉的化学方程式为_______ 。
(1)电解饱和食盐水的化学方程式为
(2)新制的氯水具有杀菌消毒,漂白作用。研究证明,溶解在水中的部分氯气能与水发生反应,其反应的化学方程式为

(3)氯水不稳定,生活中常用漂白粉进行杀菌消毒。工业上以氯气和石灰乳为原料制备漂白粉的化学方程式为
您最近一年使用:0次
解题方法
9 . 下列说法不正确 的是
| A.可用分液漏斗分离氯化钠溶液和四氯化碳的混合物 |
| B.用托盘天平称量11.7g氯化钠晶体 |
| C.用润湿的pH试纸测定pH值一定有误差 |
| D.用元素分析仪确定物质中是否含有C、H、O、N、S、Cl、Br等元素 |
您最近一年使用:0次
10 . 请按要求书写:
(1)写出丙烷的结构简式:_______ 。
(2)甲烷的电子式为:_______ 。
(3)乙烯与氯化氢化学反应为:_______ 。
(4)写出少量二氧化碳气体中通入硅酸钠溶液的化学方程式:_______ 。
(5)写出硫化氢溶液中通入二氧化硫气体的化学方程式:_______ 。
(6)乙烷与氯气光照生成一氯代物的化学方程式_______ 。
(7)相对分子质量为72的烷烃的分子式为_______ ,其中直链烷烃的习惯命名为_______ 。
(8)焦炭和石英高温条件下制粗硅的化学方程式_______ 。
(9)实验室制氨气的化学方程式_______ 。
(1)写出丙烷的结构简式:
(2)甲烷的电子式为:
(3)乙烯与氯化氢化学反应为:
(4)写出少量二氧化碳气体中通入硅酸钠溶液的化学方程式:
(5)写出硫化氢溶液中通入二氧化硫气体的化学方程式:
(6)乙烷与氯气光照生成一氯代物的化学方程式
(7)相对分子质量为72的烷烃的分子式为
(8)焦炭和石英高温条件下制粗硅的化学方程式
(9)实验室制氨气的化学方程式
您最近一年使用:0次



