1 . 按要求回答下列问题:
(1)下列变化属于吸热反应的是______ (填序号)。
①钠与冷水的反应 ②氢氧化钡晶体与氯化铵固体的反应 ③蓝矾失水变为白色粉末 ④干冰升华
⑤ 固体溶于水
固体溶于水
(2)强酸与强碱的稀溶液发生中和反应生成1mol 时的反应热
时的反应热 。若用一定浓度的稀硫酸与含10gNaOH的稀碱溶液完全反应,反应放出的热量为
。若用一定浓度的稀硫酸与含10gNaOH的稀碱溶液完全反应,反应放出的热量为______ 。(结果保留小数点后一位)
(3)已知1g 完全燃烧生成液态水时放出热量142.9kJ,则氢气的燃烧热为
完全燃烧生成液态水时放出热量142.9kJ,则氢气的燃烧热为______ ,试写出该反应的热化学方程式为______ 。
(4)试比较反应热的大小:
①



则
______  (填“>”或“<”,下同)。
(填“>”或“<”,下同)。
②已知常温时红磷比白磷稳定。
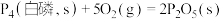

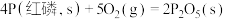

则
______  。
。
(5)已知:25℃、101kPa时,
①

②

③
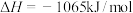
则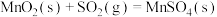

______ 。
(1)下列变化属于吸热反应的是
①钠与冷水的反应 ②氢氧化钡晶体与氯化铵固体的反应 ③蓝矾失水变为白色粉末 ④干冰升华
⑤
 固体溶于水
固体溶于水(2)强酸与强碱的稀溶液发生中和反应生成1mol
 时的反应热
时的反应热 。若用一定浓度的稀硫酸与含10gNaOH的稀碱溶液完全反应,反应放出的热量为
。若用一定浓度的稀硫酸与含10gNaOH的稀碱溶液完全反应,反应放出的热量为(3)已知1g
 完全燃烧生成液态水时放出热量142.9kJ,则氢气的燃烧热为
完全燃烧生成液态水时放出热量142.9kJ,则氢气的燃烧热为(4)试比较反应热的大小:
①




则

 (填“>”或“<”,下同)。
(填“>”或“<”,下同)。②已知常温时红磷比白磷稳定。
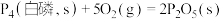

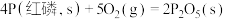

则

 。
。(5)已知:25℃、101kPa时,
①


②


③

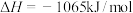
则
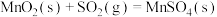

您最近一年使用:0次
2024-05-17更新
|
292次组卷
|
2卷引用:云南省临沧市沧源佤族自治县民族中学2022-2023学年高二上学期第一次月考化学试题
2 . 回答下列问题
(1)在密闭容器中,使1mol X和4mol Y混合发生下列反应: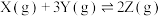
 。
。
①反应过程中X和Y的转化率之比______ 1(填“>”“<”或“=”)。
②当达到平衡时,保持恒温,压缩容器体积,平衡将______ (填“正向”“逆向”或“不”)移动,化学平衡常数K______ (填“变大”“变小”或“不变”)。
(2) 在密闭真空容器中发生反应:
在密闭真空容器中发生反应: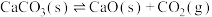 达到平衡。保持温度不变,缩小容器容积,体系重新达到平衡,则
达到平衡。保持温度不变,缩小容器容积,体系重新达到平衡,则 浓度
浓度______ (填“变大”“变小”或“不变”)。
(3)已知反应:
 。其他条件相同时,该反应使用两种不同催化剂,反应相同的反应时间,测得
。其他条件相同时,该反应使用两种不同催化剂,反应相同的反应时间,测得 的转化率随温度变化的影响如图所示。
的转化率随温度变化的影响如图所示。______ 、______ 。
②温度高于320℃时, 转化率减小的原因可能是
转化率减小的原因可能是______ 。
(1)在密闭容器中,使1mol X和4mol Y混合发生下列反应:
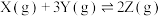
 。
。①反应过程中X和Y的转化率之比
②当达到平衡时,保持恒温,压缩容器体积,平衡将
(2)
 在密闭真空容器中发生反应:
在密闭真空容器中发生反应: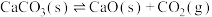 达到平衡。保持温度不变,缩小容器容积,体系重新达到平衡,则
达到平衡。保持温度不变,缩小容器容积,体系重新达到平衡,则 浓度
浓度(3)已知反应:

 。其他条件相同时,该反应使用两种不同催化剂,反应相同的反应时间,测得
。其他条件相同时,该反应使用两种不同催化剂,反应相同的反应时间,测得 的转化率随温度变化的影响如图所示。
的转化率随温度变化的影响如图所示。
②温度高于320℃时,
 转化率减小的原因可能是
转化率减小的原因可能是
您最近一年使用:0次
3 . 下列有关说法正确的是

| A.利用图甲装置可准确测定中和反应的反应热 |
| B.向图乙a中加入某一固体和液体,若注射器活塞右移,则a一定发生了放热反应 |
| C.为使测定的中和反应反应热更准确,可分多次向稀盐酸中加稀NaOH溶液 |
| D.有化学键断裂或形成的变化一定有能量变化,但不一定有新物质生成 |
您最近一年使用:0次
4 . 下列现象或操作可用勒夏特列原理解释的是
| A.与同浓度盐酸反应时,粉末状石灰石比块状石灰石产生气泡快 |
B.反应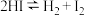 达到平衡后,压缩容器体积,体系颜色变深 达到平衡后,压缩容器体积,体系颜色变深 |
| C.为增强新制氯水的漂白能力可向其中加少量石灰石 |
D.实验室向盛 溶液的试剂瓶中加适量的铁屑 溶液的试剂瓶中加适量的铁屑 |
您最近一年使用:0次
5 . 在测定中和反应反应热的实验中,下列说法正确的是
| A.测定中和反应的反应热时,需要用到天平 |
| B.测定中和反应的反应热时,不可以用稀硫酸与稀NaOH溶液反应 |
| C.测定中和反应的反应热时,可以用保温杯代替简易量热计 |
| D.只需做一次实验,再根据公式即可得出中和反应的反应热 |
您最近一年使用:0次
名校
6 . 下列说法正确的是
| A.烷基是推电子基团,故甲酸的酸性强于乙酸 |
| B.水分子在较高温度下也很稳定与氢键有关 |
C.白磷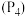 空间结构呈正四面体形,1mol白磷含 空间结构呈正四面体形,1mol白磷含 个P-P 个P-P |
D.邻羟基苯甲醛分子内氢键示意图: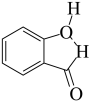 |
您最近一年使用:0次
名校
7 . 下列说法正确的是
A.电子排布不同的两种氮原子:①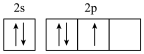 ② ②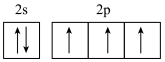 ,能量 ,能量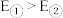 |
| B.焰火、霓虹灯光、激光、苂光、LED灯光等,都与原子核外电子跃迁吸收能量有关 |
C.若以 表示某能级的能量,则 表示某能级的能量,则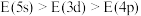 |
| D.三氯乙酸的酸性强于三氟乙酸 |
您最近一年使用:0次
8 . 回答下列问题。
(1)双氧水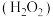 和水都是极弱电解质,若把
和水都是极弱电解质,若把 看成是二元弱酸,请写出在水中的电离方程式:
看成是二元弱酸,请写出在水中的电离方程式:___________ 。鉴于 显弱酸性,它能同强碱作用形成正盐,在一定条件下也可形成酸式盐。请写出
显弱酸性,它能同强碱作用形成正盐,在一定条件下也可形成酸式盐。请写出 与
与 作用形成盐的两个化学方程式:
作用形成盐的两个化学方程式:___________ 。
(2)如图是向 的盐酸中逐渐加入
的盐酸中逐渐加入 溶液时,溶液的
溶液时,溶液的 变化图像。
变化图像。___________  。
。
②X的值为___________ 。
(3)已知 的高碘酸
的高碘酸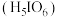 溶液与
溶液与 的
的 溶液等体积混合,所得混合溶液呈酸性,
溶液等体积混合,所得混合溶液呈酸性, 的碘酸
的碘酸 或高锰酸
或高锰酸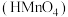 溶液与
溶液与 的
的 溶液等体积混合,所得溶液呈中性,高碘酸是
溶液等体积混合,所得溶液呈中性,高碘酸是___________ (填“强酸”或“弱酸”),理由是___________ 。
(4) 时,在一定体积
时,在一定体积 的
的 溶液中,逐滴加入一定物质的量浓度的
溶液中,逐滴加入一定物质的量浓度的 溶液,当溶液中的
溶液,当溶液中的 恰好完全沉淀时,溶液
恰好完全沉淀时,溶液 ,忽略溶液体积变化,则
,忽略溶液体积变化,则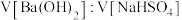 为
为___________ 。
(1)双氧水
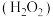 和水都是极弱电解质,若把
和水都是极弱电解质,若把 看成是二元弱酸,请写出在水中的电离方程式:
看成是二元弱酸,请写出在水中的电离方程式: 显弱酸性,它能同强碱作用形成正盐,在一定条件下也可形成酸式盐。请写出
显弱酸性,它能同强碱作用形成正盐,在一定条件下也可形成酸式盐。请写出 与
与 作用形成盐的两个化学方程式:
作用形成盐的两个化学方程式:(2)如图是向
 的盐酸中逐渐加入
的盐酸中逐渐加入 溶液时,溶液的
溶液时,溶液的 变化图像。
变化图像。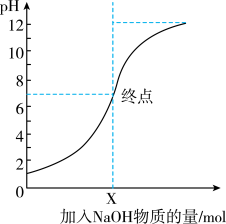
 。
。②X的值为
(3)已知
 的高碘酸
的高碘酸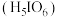 溶液与
溶液与 的
的 溶液等体积混合,所得混合溶液呈酸性,
溶液等体积混合,所得混合溶液呈酸性, 的碘酸
的碘酸 或高锰酸
或高锰酸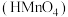 溶液与
溶液与 的
的 溶液等体积混合,所得溶液呈中性,高碘酸是
溶液等体积混合,所得溶液呈中性,高碘酸是(4)
 时,在一定体积
时,在一定体积 的
的 溶液中,逐滴加入一定物质的量浓度的
溶液中,逐滴加入一定物质的量浓度的 溶液,当溶液中的
溶液,当溶液中的 恰好完全沉淀时,溶液
恰好完全沉淀时,溶液 ,忽略溶液体积变化,则
,忽略溶液体积变化,则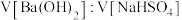 为
为
您最近一年使用:0次
9 . 试回答下列有关热化学问题。
(1)根据键能数据计算 的反应热
的反应热
___________ 。
(2) 催化重整反应为
催化重整反应为 。
。
已知:
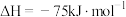

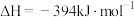

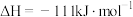
该催化重整反应的
___________  。
。
(3)近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。过程如图: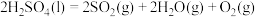

反应Ⅲ:
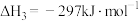
反应Ⅱ的热化学方程式:___________ 。
(4)工业上常用磷精矿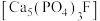 和硫酸反应制备磷酸。已知
和硫酸反应制备磷酸。已知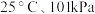 时:
时:

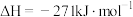
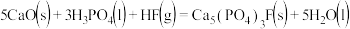
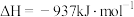
则 和硫酸反应生成磷酸的热化学方程式是
和硫酸反应生成磷酸的热化学方程式是___________ 。
(5)已知: 钒催化剂参与反应的能量变化如图所示,
钒催化剂参与反应的能量变化如图所示,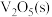 与
与 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为___________ 。
(1)根据键能数据计算
 的反应热
的反应热
| 化学键 |  |  |  |  |
键能 | 414 | 489 | 565 | 155 |
(2)
 催化重整反应为
催化重整反应为 。
。已知:

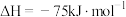

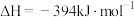

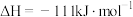
该催化重整反应的

 。
。(3)近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。过程如图:
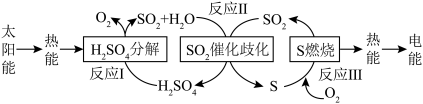
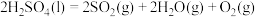

反应Ⅲ:

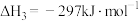
反应Ⅱ的热化学方程式:
(4)工业上常用磷精矿
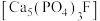 和硫酸反应制备磷酸。已知
和硫酸反应制备磷酸。已知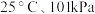 时:
时:
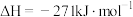
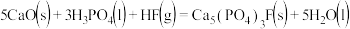
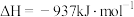
则
 和硫酸反应生成磷酸的热化学方程式是
和硫酸反应生成磷酸的热化学方程式是(5)已知:
 钒催化剂参与反应的能量变化如图所示,
钒催化剂参与反应的能量变化如图所示,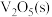 与
与 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为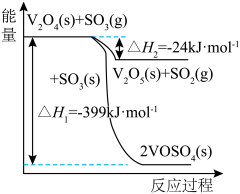
您最近一年使用:0次
名校
10 . 填空
(1) 的名称为
的名称为_______ 。
(2)乙醚(C4H10O)的同分异构体有多种,请写出符合下列条件的同分异构体的结构简式_______ 。
a.属于醇类; b.不能发生催化氧化。
(3)模拟“人工树叶”电化学实验装置如下图所示,该装置能将H2O和CO2转化为O2和燃料(C3H8O)。

a电极的反应式为_______ ;每生成1molO2,转移_______ mol电子。
(4)高能火箭燃料肼(H2N—NH2)在燃烧过程的能量变化如下图所示。
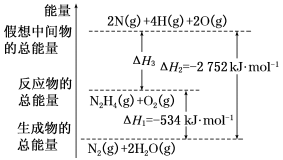
N2H4在O2中燃烧的热化学方程式为_______ 。
(1)
 的名称为
的名称为(2)乙醚(C4H10O)的同分异构体有多种,请写出符合下列条件的同分异构体的结构简式
a.属于醇类; b.不能发生催化氧化。
(3)模拟“人工树叶”电化学实验装置如下图所示,该装置能将H2O和CO2转化为O2和燃料(C3H8O)。

a电极的反应式为
(4)高能火箭燃料肼(H2N—NH2)在燃烧过程的能量变化如下图所示。

N2H4在O2中燃烧的热化学方程式为
您最近一年使用:0次



