1 . 现有如图所示的转化关系,已知:A为高级脂肪酸甘油酯。回答下列问题:___________ ,D的结构简式为___________ 。
(2)①的化学方程式为________________ ;③的反应类型为________ 反应。
(3)完全燃烧等物质的量的B和某烷烃消耗等量的氧气,则该烷烃的名称为___________ 。
(4)m g某天然油脂完全水解需要18gNaOH,则m g该油脂的物质的量为___________ mol。
(5)一定量的CH3COOH和O2混合后完全反应生成CO2、CO和H2O(g)。产物分别经过浓硫酸和碱石灰,浓硫酸增重10.8g,碱石灰增重13.2g。则n(CH3COOH)︰n(O2)=___________ 。

(2)①的化学方程式为
(3)完全燃烧等物质的量的B和某烷烃消耗等量的氧气,则该烷烃的名称为
(4)m g某天然油脂完全水解需要18gNaOH,则m g该油脂的物质的量为
(5)一定量的CH3COOH和O2混合后完全反应生成CO2、CO和H2O(g)。产物分别经过浓硫酸和碱石灰,浓硫酸增重10.8g,碱石灰增重13.2g。则n(CH3COOH)︰n(O2)=
您最近一年使用:0次
名校
2 . 关于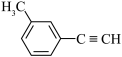 的说法正确的是
的说法正确的是
| A.分子中有6个原子共线 | B.分子中共平面的原子数目最多为14 |
| C.分子中的苯环由单双键交替组成 | D.该有机物的一氯代物有两种 |
您最近一年使用:0次
名校
3 . 下列选项中除杂试剂或操作正确的是
选项 | 物质(杂质) | 除杂试剂或操作 |
A | 甲烷(丙烯) | 酸性高锰酸钾溶液 |
B | 乙酸乙酯(乙醇) | 浓硫酸、乙酸、加热 |
C | 二氧化硫(乙烯) | 溴水 |
D | 蛋白质溶液(NaCl) | 渗析 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-04-20更新
|
983次组卷
|
3卷引用:江西省南昌十九中2021-2022学年高一下学期第三次月考化学试卷
名校
解题方法
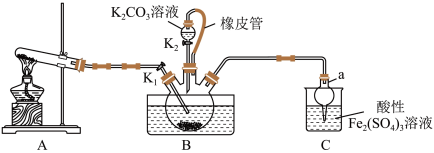
4 . 硫氰化钾(KSCN)是一种用途广泛的化工原料,常用于染料、药物的生产。实验小组设计如图实验装置模拟工业制备 KSCN 并进行相关探究实验。___________ 。
(2)装置A用于实验室制备氨气,反应的化学方程式为___________ 。
(3)装置B中,三颈烧瓶内盛放有 CS₂、水和固体催化剂,通入氨气的导管口需要浸没在 CS₂液体中,其目的是___________ (写两点)。
(4)KSCN 溶液的制备:实验开始时打开K₁,加热装置A、D,待三颈烧瓶内液体不分层后,熄灭装置A处的酒精灯,关闭K₁,移开水浴。将装置B继续加热至 待 NH₄HS 完全分解后(
待 NH₄HS 完全分解后(  打开 K₂,缓缓滴入适量的)
打开 K₂,缓缓滴入适量的)  溶液,继续加热有气泡产生,制得KSCN 溶液,该反应的化学方程式是
溶液,继续加热有气泡产生,制得KSCN 溶液,该反应的化学方程式是___________ 。
(5)尾气处理:装置C 中仪器a的名称是___________ ,酸性Fe₂(SO₄)₃溶液用于除去尾气中两种污染性气体,其中一种气体M能使酚酞溶液变红,另一种气体N能使溶液产生淡黄色沉淀,写出除去气体N的离子方程式___________ 。
(6)过滤装置C中吸收尾气后的悬浊液,得到滤液x。取少量滤液x进行如图实验[已知 (白色)]:
(白色)]:___________ [可供选择的试剂:  溶液、
溶液、  溶液、
溶液、  溶液、
溶液、  溶液]。
溶液]。

(2)装置A用于实验室制备氨气,反应的化学方程式为
(3)装置B中,三颈烧瓶内盛放有 CS₂、水和固体催化剂,通入氨气的导管口需要浸没在 CS₂液体中,其目的是
(4)KSCN 溶液的制备:实验开始时打开K₁,加热装置A、D,待三颈烧瓶内液体不分层后,熄灭装置A处的酒精灯,关闭K₁,移开水浴。将装置B继续加热至
 待 NH₄HS 完全分解后(
待 NH₄HS 完全分解后(  打开 K₂,缓缓滴入适量的)
打开 K₂,缓缓滴入适量的)  溶液,继续加热有气泡产生,制得KSCN 溶液,该反应的化学方程式是
溶液,继续加热有气泡产生,制得KSCN 溶液,该反应的化学方程式是(5)尾气处理:装置C 中仪器a的名称是
(6)过滤装置C中吸收尾气后的悬浊液,得到滤液x。取少量滤液x进行如图实验[已知
 (白色)]:
(白色)]: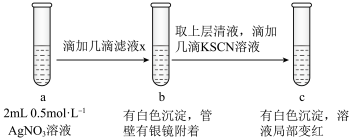
 溶液、
溶液、  溶液、
溶液、  溶液、
溶液、  溶液]。
溶液]。
您最近一年使用:0次
2024-04-16更新
|
318次组卷
|
2卷引用:福建师范大学附属中学2021-2022学年高一下学期期末考试化学试题
解题方法
5 . 有200mlMgCl2和AlCl3的混合物,其中c(Mg2+)为0.2mol/L,c(C1-)为1.3mol/L。为使Mg2+全部转化为沉淀分离出来,至少需加4mol/L溶液的NaOH体积为
| A.40ml | B.72ml | C.80ml | D.128ml |
您最近一年使用:0次
2024-04-08更新
|
97次组卷
|
6卷引用:云南省富宁县第一中学2021-2022学年高一下学期开学考试化学试题
云南省富宁县第一中学2021-2022学年高一下学期开学考试化学试题2015-2016学年江苏省海安实验中学高二上学期期中必修化学试卷浙江省湖州市长兴县等三县2017-2018学年高二上学期期中考试化学试题江西省余干县第二中学2020-2021学年高一上学期12月月考化学试题云南省大理白族自治州实验中学2020-2021学年高一上学期(理科)期末考试化学试题(已下线)第03讲 物质的量在化学方程式计算中的应用(练习)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)
名校
解题方法
6 . 资源化利用CO2,不仅可以减少温室气体的排放,还可以获得燃料或重要的化工产品。
(1)CO2的捕集:
①CO2属于___________ 分子(填“极性”或“非极性”),其晶体(干冰)属于__________ 晶体。
②用饱和 溶液做吸收剂可“捕集”CO2。若所得溶液
溶液做吸收剂可“捕集”CO2。若所得溶液 ,溶液中c(HCO
,溶液中c(HCO ):c(CO
):c(CO )=
)=_______ ;(室温下, 的K1=4×10-7;K2=5×10-11)若吸收剂失效,可利用NaOH溶液使其再生,写出该反应的离子方程式
的K1=4×10-7;K2=5×10-11)若吸收剂失效,可利用NaOH溶液使其再生,写出该反应的离子方程式_____ 。
③聚合离子液体是目前广泛研究的CO2吸附剂。结合下图 分析聚合离子液体吸附CO2的有利条件是____________ 。
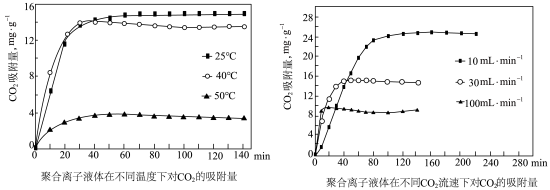
(2)生产尿素:工业上以CO2、 为原料生产尿素[CO(NH2)2],该反应分为二步进行:
为原料生产尿素[CO(NH2)2],该反应分为二步进行:
第一步: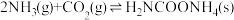
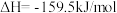
第二步:
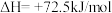
写出上述合成尿素的热化学方程式_______ 。
(3)合成乙酸:中国科学家首次以 、CO2和H2为原料高效合成乙酸,其反应路径如图所示:
、CO2和H2为原料高效合成乙酸,其反应路径如图所示:
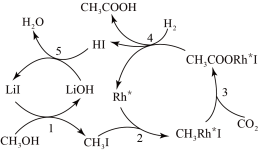
①原料中的 可通过电解法由
可通过电解法由 制取,用稀硫酸作电解质溶液,写出生成
制取,用稀硫酸作电解质溶液,写出生成 的电极反应式:
的电极反应式:____________ 。
②根据图示 ,写出总反应的化学方程式:_______ 。
(1)CO2的捕集:
①CO2属于
②用饱和
 溶液做吸收剂可“捕集”CO2。若所得溶液
溶液做吸收剂可“捕集”CO2。若所得溶液 ,溶液中c(HCO
,溶液中c(HCO ):c(CO
):c(CO )=
)= 的K1=4×10-7;K2=5×10-11)若吸收剂失效,可利用NaOH溶液使其再生,写出该反应的离子方程式
的K1=4×10-7;K2=5×10-11)若吸收剂失效,可利用NaOH溶液使其再生,写出该反应的离子方程式③聚合离子液体是目前广泛研究的CO2吸附剂。

(2)生产尿素:工业上以CO2、
 为原料生产尿素[CO(NH2)2],该反应分为二步进行:
为原料生产尿素[CO(NH2)2],该反应分为二步进行:第一步:
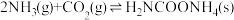
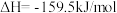
第二步:

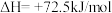
写出上述合成尿素的热化学方程式
(3)合成乙酸:中国科学家首次以
 、CO2和H2为原料高效合成乙酸,其反应路径如图所示:
、CO2和H2为原料高效合成乙酸,其反应路径如图所示:
①原料中的
 可通过电解法由
可通过电解法由 制取,用稀硫酸作电解质溶液,写出生成
制取,用稀硫酸作电解质溶液,写出生成 的电极反应式:
的电极反应式:②
您最近一年使用:0次
2024-04-04更新
|
363次组卷
|
3卷引用:湖南省株洲市第一中学2021-2022学年高三上学期期末测试化学试题
名校
解题方法
7 . 有机物M是一种制备液晶材料的重要中间体,其合成路线如图所示。
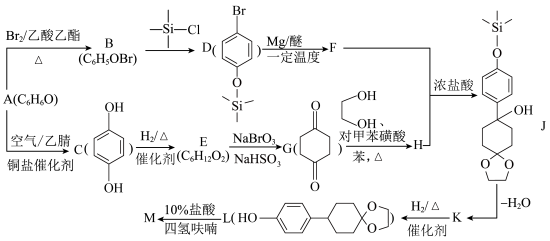
已知:Ⅰ.RX+Mg R-MgX(格林试剂),X=Cl、Br、I;
R-MgX(格林试剂),X=Cl、Br、I;
Ⅱ.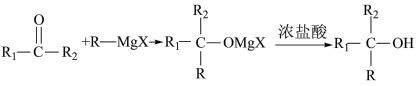 ;
;
Ⅲ.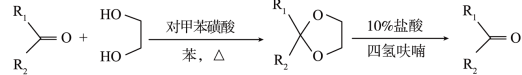 。
。
回答下列问题:
(1)A的俗称是___________ ,B的结构简式为___________ 。
(2)B→D的反应类型是___________ ,反应中使用三甲基氯硅烷(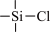 )的作用是
)的作用是___________ ,在本流程中起类似作用的有机物还有___________ (填名称)。
(3)G→H的化学方程式是___________ 。
(4)M的结构简式为___________ ,所含官能团有___________ (填名称)。
(5)符合下列条件的E的同分异构体有___________ 种(不考虑立体异构);其中核磁共振氢谱中显示有6组峰且峰面积之比为6∶2∶1∶1∶1∶1,同时含有1个手性碳原子的有机物结构简式为___________ (写一种)。
①能与金属钠反应产生氢气;②含两个甲基;③能发生银镜反应。

已知:Ⅰ.RX+Mg
 R-MgX(格林试剂),X=Cl、Br、I;
R-MgX(格林试剂),X=Cl、Br、I;Ⅱ.
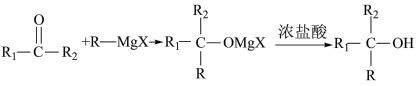 ;
;Ⅲ.
 。
。回答下列问题:
(1)A的俗称是
(2)B→D的反应类型是
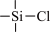 )的作用是
)的作用是(3)G→H的化学方程式是
(4)M的结构简式为
(5)符合下列条件的E的同分异构体有
①能与金属钠反应产生氢气;②含两个甲基;③能发生银镜反应。
您最近一年使用:0次
2024-04-04更新
|
180次组卷
|
2卷引用:湖南省株洲市第一中学2021-2022学年高三上学期期末测试化学试题
名校
8 . 几种短周期元素的原子半径及主要化合价如下表所示,下列叙述正确的是
元素代号 | X | Y | Z | W | Q |
原子半径/pm | 130 | 118 | 75 | 73 | 102 |
主要化合价 | +2 | +3 | +5、-3 | -2 | +6、-2 |
| A.简单离子半径:X<Y |
B.一定条件下,Z单质与W的常见单质直接生成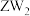 |
| C.W的简单氢化物比Q的更稳定,是因为W的简单氢化物中含有氢键 |
| D.最高价氧化物对应的水化物的碱性:X>Y |
您最近一年使用:0次
名校
9 . 某种离子液体的结构如图示,X、Y、Z、M、R为原子序数依次增大的短周期元素,Z的质子数等于X、Y的质子数之和,R为电负性最大的元素。下列说法正确的是
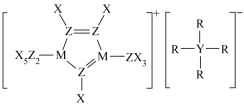
| A.Y的电负性大于Z |
| B.M、X形成的化合物分子间易形成氢键 |
| C.阴离子的空间构型为平面四边形 |
| D.分子的极性:MR3<YR3 |
您最近一年使用:0次
2024-03-24更新
|
342次组卷
|
2卷引用:重庆市第八中学校2022届高三下学期高考适应性月考(七)化学试题
名校
10 . 直接排放含 的烟气会形成酸雨,危害环境。某化学实验小组进行如下有关
的烟气会形成酸雨,危害环境。某化学实验小组进行如下有关 性质的探究活动。
性质的探究活动。
(1)写出证明 弱氧化性的化学方程式
弱氧化性的化学方程式________ 。
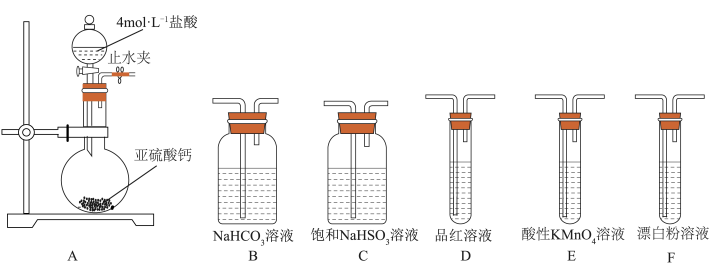
(2)写出下图装置A中滴加盐酸仪器的名称:________ 。
①甲同学认为按照A→C→F顺序连接装置可以比较亚硫酸和次氯酸的酸性强弱,乙同学认为该方案不合理,其理由是________ 。
②丙同学设计的合理实验方案为A→________ →尾气处理(填字母)。其中装置C的作用是________ 。证明亚硫酸酸性强于次氯酸的实验现象是________ 。
(4)利用下图的装置可测定装置A残液中 的含量。量取1.00mL残液于烧瓶中,加适量蒸馏水稀释,加热使
的含量。量取1.00mL残液于烧瓶中,加适量蒸馏水稀释,加热使 全部逸出并与锥形瓶中的
全部逸出并与锥形瓶中的 溶液恰好完全反应,然后用浓度为
溶液恰好完全反应,然后用浓度为 溶液测定锥形瓶中生成的酸的含量,消耗NaOH溶液的体积为20.00mL。
溶液测定锥形瓶中生成的酸的含量,消耗NaOH溶液的体积为20.00mL。
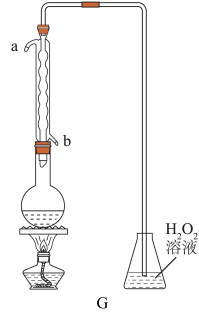
残液中 的含量为
的含量为________  。
。
 的烟气会形成酸雨,危害环境。某化学实验小组进行如下有关
的烟气会形成酸雨,危害环境。某化学实验小组进行如下有关 性质的探究活动。
性质的探究活动。(1)写出证明
 弱氧化性的化学方程式
弱氧化性的化学方程式(2)写出下图装置A中滴加盐酸仪器的名称:
①甲同学认为按照A→C→F顺序连接装置可以比较亚硫酸和次氯酸的酸性强弱,乙同学认为该方案不合理,其理由是
②丙同学设计的合理实验方案为A→
(4)利用下图的装置可测定装置A残液中
 的含量。量取1.00mL残液于烧瓶中,加适量蒸馏水稀释,加热使
的含量。量取1.00mL残液于烧瓶中,加适量蒸馏水稀释,加热使 全部逸出并与锥形瓶中的
全部逸出并与锥形瓶中的 溶液恰好完全反应,然后用浓度为
溶液恰好完全反应,然后用浓度为 溶液测定锥形瓶中生成的酸的含量,消耗NaOH溶液的体积为20.00mL。
溶液测定锥形瓶中生成的酸的含量,消耗NaOH溶液的体积为20.00mL。
残液中
 的含量为
的含量为 。
。
您最近一年使用:0次
2024-03-14更新
|
237次组卷
|
2卷引用:广东省深圳市高级中学2021-2022学年高一下学期期中考试化学试卷



