名校
解题方法
1 . X、Y、Z、M为短周期元素,原子序数依次增大。A~J均由该四种元素构成的单质或化合物,其转化关系如图所示,部分生成物省略。
已知:①A、B、C、G都是由两种元素构成的化合物,其中A、G分子所含的电子数为10e-,B、C分子所含的电子数为18e-;D为空气的主要成分之一、
②另取16.8gJ在真空条件下,控制温度350~400oC加热至完全分解,得到F和8.96L(已折算成标准状况)A两种物质。

请回答下列问题:
(1)写出C的化学式是___________ ;D的电子式是___________ 。
(2)请写出金属单质E在生产生活中的一种作用___________ 。
(3)写出次氯酸钠与过量气体A反应生成B的化学方程式是___________ ;B在制备过程中,气体A需要过量的理由是___________ 。
(4)写出F和G反应生成H和A的化学方程式是___________ 。
(5)B在加热条件下与CuO反应可生成气体D和金属单质,请设计实验方案,验证B与CuO反应后固体的成分(不考虑其他反应)___________ 。
(6)写出J在已知②条件下受热分解的化学方程式是___________ 。
已知:①A、B、C、G都是由两种元素构成的化合物,其中A、G分子所含的电子数为10e-,B、C分子所含的电子数为18e-;D为空气的主要成分之一、
②另取16.8gJ在真空条件下,控制温度350~400oC加热至完全分解,得到F和8.96L(已折算成标准状况)A两种物质。

请回答下列问题:
(1)写出C的化学式是
(2)请写出金属单质E在生产生活中的一种作用
(3)写出次氯酸钠与过量气体A反应生成B的化学方程式是
(4)写出F和G反应生成H和A的化学方程式是
(5)B在加热条件下与CuO反应可生成气体D和金属单质,请设计实验方案,验证B与CuO反应后固体的成分(不考虑其他反应)
(6)写出J在已知②条件下受热分解的化学方程式是
您最近一年使用:0次
2021-11-05更新
|
1137次组卷
|
2卷引用:浙江省诸暨市2018-2019学年高二下学期期末考试化学试题
2 . 癌症是威胁人类健康的主要疾病之一。肿瘤的发病涉及到多种因素多个步骤的病理过程。研究表明,肿瘤的发生与核小体核心组蛋白N-端的赖氨酸残基的乙酰化和去乙酰化的失衡有着密切的关系。组蛋白去乙酰化酶(histone deacetylases,HDACs)抑制剂通过调节组蛋白N-端的赖氨酸残基的乙酰化和去乙酰化,激活抑癌基因,从而抑制肿瘤细胞生长,诱导肿瘤细胞凋亡,因此是近几年来抗肿瘤药物的研究热点之一。下面是一种HDAC抑制剂(F)的合成路线,请根据该路线回答问题。
(甲)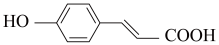
 (A)
(A)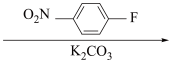 (B)
(B) (C)
(C)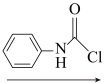 (D)
(D) (E)
(E)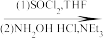 (F)
(F)
(1)写出A、B、D、E的结构式:A_______ B_______ D_______ E_______
(2)F与Zn2+配位是其发挥作用的前提之一。F中哪个部位最易与Zn2+配位?为什么_______ 。
(3)以3-(2-异丁基-4-羟基)苯基丙烯酸为原料,也可合成一种HDAC,该原料可能的立体异构体有_______ 种。
(甲)

 (A)
(A) (B)
(B) (C)
(C) (D)
(D) (E)
(E)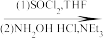 (F)
(F)
(1)写出A、B、D、E的结构式:A
(2)F与Zn2+配位是其发挥作用的前提之一。F中哪个部位最易与Zn2+配位?为什么
(3)以3-(2-异丁基-4-羟基)苯基丙烯酸为原料,也可合成一种HDAC,该原料可能的立体异构体有
您最近一年使用:0次
3 . 以乳糖、 玉米浆为原料在微生物作用下得到含青霉素(~ 8mg/L)的溶液,过滤掉微生物后,溶液经下列萃取和反萃取过程(已略去所加试剂),可得到青霉素钠盐(~8g/L)。 流程为:滤液打入萃取釜,先调节pH=2后加入溶剂,再调节pH=7.5,加入水;反复此过程,最后加丁醇,得到产物纯的青霉素钠盐。(如下流程图)_______ 。为什么不用便宜的乙酸乙酯_______ 。
(2)在pH=7.5时,加水的原因是_______ 。
(3)加丁醇的原因是_______ 。

已知青霉素结构式: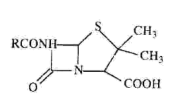
(2)在pH=7.5时,加水的原因是
(3)加丁醇的原因是
您最近一年使用:0次
4 . 回答下列问题
(1)最近报道,在一100℃低温下合成了化合物X,元素分析仪得出其分子式为C5H4,红外光谱和核磁共振表明其分子中的氢原子的化学环境没有区别,而碳的化学环境却有两种,温度升高将迅速分解,X的可能结构式是___________ 、___________ 、___________ ;
(2)如果分子中有三种环境不同的氢,有四种环境不同的碳,该烃的可能结构式为___________ 、___________ ;
(3)如果氢有两种环境,碳有四种环境,该烃可能结构式为___________ 、___________ ;
(4)如果氢有两种环境,碳有三种环境,该烃的结构简式可能为___________ 、___________ 、___________ 。
(1)最近报道,在一100℃低温下合成了化合物X,元素分析仪得出其分子式为C5H4,红外光谱和核磁共振表明其分子中的氢原子的化学环境没有区别,而碳的化学环境却有两种,温度升高将迅速分解,X的可能结构式是
(2)如果分子中有三种环境不同的氢,有四种环境不同的碳,该烃的可能结构式为
(3)如果氢有两种环境,碳有四种环境,该烃可能结构式为
(4)如果氢有两种环境,碳有三种环境,该烃的结构简式可能为
您最近一年使用:0次
5 . 化合物(A)(C12H14O2)由一个芳香醛和丙酮在碱中合成得到。化合物(A)在红外光谱1675cm-1处有一个尖锐的峰(表示存在有一个 ),(A)催化氢化得到(B)(C12H16O2)。(A)用碘和碳酸钾溶液处理得到碘仿和化合物(C)(C11H12O3),氧化(B)和(C)都得到酸(|D)(C9H10O3)。(D)用溴化氢处理得到另一个酸(E)(C7H6O3),(E)在水蒸气流中易挥发。试回答下列问题:
),(A)催化氢化得到(B)(C12H16O2)。(A)用碘和碳酸钾溶液处理得到碘仿和化合物(C)(C11H12O3),氧化(B)和(C)都得到酸(|D)(C9H10O3)。(D)用溴化氢处理得到另一个酸(E)(C7H6O3),(E)在水蒸气流中易挥发。试回答下列问题:
(1)写出(A)—(E)的结构式:A___________ 、B___________ 、C___________ 、D___________ 、E___________ 。
(2)将化合物(A)、(C)和(E)用系统命名法命名:A___________ 、C___________ 、E___________ 。
(3)试说明(E)在水蒸气流中易挥发的原因___________ 。
(4)化合物(C)和(E)中有无手性碳原子,若有,请用*符号表示出___________ 、___________ 。
 ),(A)催化氢化得到(B)(C12H16O2)。(A)用碘和碳酸钾溶液处理得到碘仿和化合物(C)(C11H12O3),氧化(B)和(C)都得到酸(|D)(C9H10O3)。(D)用溴化氢处理得到另一个酸(E)(C7H6O3),(E)在水蒸气流中易挥发。试回答下列问题:
),(A)催化氢化得到(B)(C12H16O2)。(A)用碘和碳酸钾溶液处理得到碘仿和化合物(C)(C11H12O3),氧化(B)和(C)都得到酸(|D)(C9H10O3)。(D)用溴化氢处理得到另一个酸(E)(C7H6O3),(E)在水蒸气流中易挥发。试回答下列问题:(1)写出(A)—(E)的结构式:A
(2)将化合物(A)、(C)和(E)用系统命名法命名:A
(3)试说明(E)在水蒸气流中易挥发的原因
(4)化合物(C)和(E)中有无手性碳原子,若有,请用*符号表示出
您最近一年使用:0次
2021-08-13更新
|
360次组卷
|
2卷引用:第30届( 2016年)全国中学生化学竞赛(安徽赛区)初赛试题
6 . 已知铁元素的电势图为:FeO
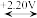 Fe3+
Fe3+ Fe2+
Fe2+ Fe,φ0(Cl2/Cl-)=+1.36V。下列有关说法正确的是
Fe,φ0(Cl2/Cl-)=+1.36V。下列有关说法正确的是

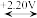 Fe3+
Fe3+ Fe2+
Fe2+ Fe,φ0(Cl2/Cl-)=+1.36V。下列有关说法正确的是
Fe,φ0(Cl2/Cl-)=+1.36V。下列有关说法正确的是| A.Fe2+在水溶液中可发生歧化反应 |
| B.无论在酸性或碱性条件下,Fe均可还原水 |
C.FeO 在水溶液中可稳定存在 在水溶液中可稳定存在 |
D.Cl2无论在何条件下均不能氧化Fe3+生成FeO |
您最近一年使用:0次
解题方法
7 . 按表格内容完成填空。
| 配离子化学式 | 中心离子氧化态 | 中心离子杂环轨道类型 | 配离子几何构型 | 配离子磁性(顺磁或逆磁) |
CoF | ||||
Cr(H2O) | ||||
Zn(NH3) | ||||
Cu(NH3) |
您最近一年使用:0次
解题方法
8 . 饱和多元醇A,含碳39.13%,碳氧原子个数比为1:1,A的名称为_______ 。A与等摩尔的醋酸酐反应,得到的化合物结构简式为_______ 。A的水溶液在碱存在下可溶解Cu(OH)2,使溶液变蓝,溶液中的蓝色物质结构为_______ 。
您最近一年使用:0次
解题方法
9 . 黄铜矿是由Fe、 Cu、S三种元素组成的复盐X为主要成分,其中Cu、Fe两种元素质量比为8:7;将mg X粉末溶于200mL。浓HNO3,反应后溶液加水稀释至2.12L时,测得其pH=0.将稀释后溶液分成二等份,向其中一份加入6.05mol/L NaOH溶液;向另一份加入0.600mol/L Ba(NO3)2溶液,两溶液均生成沉淀,且沉淀的量随加入溶液体积的变化如下图所示:
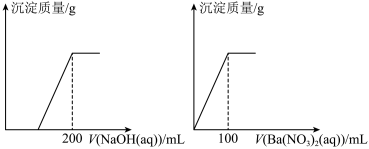
计算推断(填入推断结果):
(1)X粉末;mg的值为___________ ;
(2)则X的化学式为___________ 。

计算推断(填入推断结果):
(1)X粉末;mg的值为
(2)则X的化学式为
您最近一年使用:0次
名校
解题方法
10 . 取一定质量含Cu,Cu2O,CuO的固体混合物。将其分成二等份,并进行下列转化:
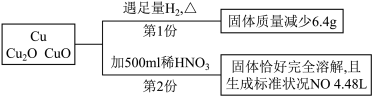
| A.1. 6mol/L | B.3.2mo/L | C.4.8mol/L | D.条件不足,无法计算 |
您最近一年使用:0次
2021-08-13更新
|
805次组卷
|
4卷引用:第27届(2013年)全国高中学生化学竞赛(江西赛区)高二预赛试题



