19. 甲醇既是重要的化工原料,又可作为燃料。利用CO
2、CO与H
2在一定条件下可反应生成甲醇。研究表明,在某催化剂作用下,发生的主要反应如下:
反应I:CO
2(g)+3H
2(g)
⇌CH
3OH(g)+H
2O(g) △H
1=-59kJ·mol
-1反应II:CO
2(g)+H
2(g)
⇌CO(g)+H
2O(g) △H
2反应III:CO(g)+2H
2(g)
⇌CH
3OH(g) △H
3其中,有关物质化学键的键能如表所示:
| 化学键 | C=O | H-H | C-O | C≡O | H-O | C-H |
| 键能/(kJ∙mol-1) | 805 | 436 | 343 | 1076 | 465 | 413 |
请回答下列问题:
(1)仅考虑反应I,有利于提高该反应平衡转化率的条件是___________。
(2)反应II的△H
2=
___________。
(3)当CO
2、CO与H
2以n(H
2)/n(CO+CO
2)=2.60的组成比通入时,体系中CO平衡转化率(a)与压强的关系如图1所示。请指出图1中压强由大到小顺序是
___________,判断理由是
___________。
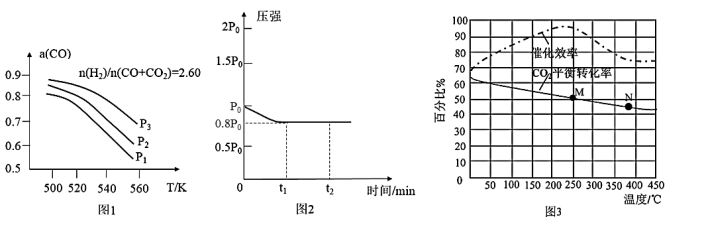
(4)某温度下,向1L固定容积的密闭容器中加入2.5molCO
2(g)和2.5molH
2(g),仅发生反应I,达到平衡,测得容器内气体的压强随着时间的变化如图2所示。
①请计算该温度下,反应I的平衡常数K=
___________(用具体数值表示);
②若保持其他条件不变,继续向容器中投入2.5molCO
2(g)和2.5molH
2(g),再次达到平衡,此时,
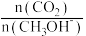
的值与原平衡相比,将
___________(填“增大”、“减小”或“不变”)。
③若采用0.5L固定容积的密闭容器,投料量(仍为2.5molCO
2和2.5molH
2)、催化剂和反应温度均保持不变,请在图2中画出0~t
2时刻,体系内的压强随时间变化的曲线
___________。
(5)在一定压强下,按n(CO
2):n(H
2)=1:3(总物质的量为4amol)的投料比充入密闭容器中仅发生反应I。测定温度对的CO
2的平衡转化率和催化剂催化效率影响情况如图3所示。下列说法不正确的是
___________。
A.生成CH
3OH的速率:ʋ(M)可能大于ʋ(N)
B.平衡常数:K
M>K
NC.其他条件相同时,适当增大催化剂的表面积,可提高CO
2的平衡转化率
D.若投料比不变,温度越低,反应一定时间后CO
2的转化率一定较高
E.若其他条件不变,投料比改为n(CO
2)∶n(H
2)=1∶4,可以提高CO
2的平衡转化率