1 . 某校化学兴趣小组为研究Cl2的性质,设计如图所示装置进行实验。装置Ⅲ中夹持装置已略去,其中a为干燥的品红试纸,b为湿润的品红试纸。
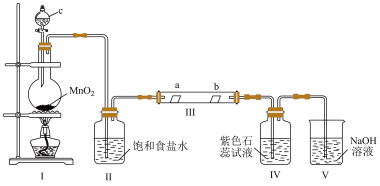
(1)装置Ⅰ中仪器c的名称是___________ ,反应中浓盐酸表现的性质有___________ ,实验室以二氧化锰和浓盐酸制备氯气的化学方程式为___________ 。
(2)装置Ⅱ的作用是___________ 。
(3)若产生Cl2足量,实验过程中装置Ⅳ中的实验现象___________ 。
(4)若Ⅳ中装有淀粉—碘化钾溶液,则观察到的现象是___________ ,写出Ⅳ中反应的离子方程式___________ 。
(5)若Ⅳ中装有硝酸银溶液,则观察到的现象是___________ ,写出Ⅳ中反应的离子方程式___________ 。
(6)写出V装置中发生化学反应的离子方程式:___________ 。
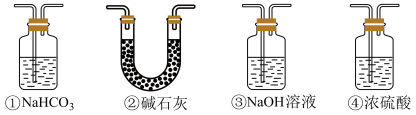
(7)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的___________ 装置(填序号)。

(1)装置Ⅰ中仪器c的名称是
(2)装置Ⅱ的作用是
(3)若产生Cl2足量,实验过程中装置Ⅳ中的实验现象
(4)若Ⅳ中装有淀粉—碘化钾溶液,则观察到的现象是
(5)若Ⅳ中装有硝酸银溶液,则观察到的现象是
(6)写出V装置中发生化学反应的离子方程式:
(7)实验结束后,该组同学在装置Ⅲ中观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在图中装置Ⅱ与Ⅲ之间添加图中的

您最近一年使用:0次
名校
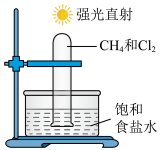
2 . 下列实验方案不能达到实验目的的是
| A.证明石蜡裂解产物中含有烯烃 | B.观察甲烷取代反应的现象 |
|
|
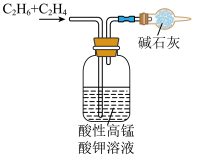
| C.除乙烷中乙烯,并得到纯净干燥的乙烷 | D.实验室制备乙酸乙酯 |
|
|
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . 为达到实验目的,下列实验方案合理的是
选项 | 实验目的 | 实验方案 |
| A | 测定氯水 | 将新制氯水滴于 试纸上,稍后与标准比色卡对比 试纸上,稍后与标准比色卡对比 |
| B | 比较 与 与 的酸性强弱 的酸性强弱 | 将 气体通入 气体通入 溶液中观察现象 溶液中观察现象 |
| C | 制备 | 将 固体置于向下倾斜的试管中加热 固体置于向下倾斜的试管中加热 |
| D | 制备 胶体 胶体 | 将饱和 溶液滴入 溶液滴入 溶液 溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
4 . 某研究性学习小组的甲、乙同学分别设计了以下实验来验证元素周期律。
Ⅰ.甲同学验证同一周期从左到右元素的金属性强弱。实验药品有小块钠,表面积相同的镁、铝,稀盐酸,氢氧化钠溶液,蒸馏水。
(1)请补充实验操作:取表面积相同的铝、镁投入到等量的__________ (填试剂名称)。
Ⅱ.乙同学利用如图所示装置可以验证非金属性的变化规律,实验室中药品有① 溶液、②
溶液、② 、③浓盐酸、④
、③浓盐酸、④ 。已知:硫为淡黄色固体,难溶于水。
。已知:硫为淡黄色固体,难溶于水。______________________________ 。
(3)用上述装置设计实验来验证氯的非金属性强于硫,装置A、B、C中所装药品分别为__________ 、__________ 、__________ (填序号)。
(4)装置C中的实验现象为______________________________ 。
Ⅰ.甲同学验证同一周期从左到右元素的金属性强弱。实验药品有小块钠,表面积相同的镁、铝,稀盐酸,氢氧化钠溶液,蒸馏水。
实验目的 | 实验操作 | 实验结论 |
比较钠、镁金属性强弱 | 取钠、镁投入到等量的蒸馏水中 |
|
比较镁、铝金属性强弱 | 取表面积相同的铝、镁投入到等量的__________中 |
|
(1)请补充实验操作:取表面积相同的铝、镁投入到等量的
Ⅱ.乙同学利用如图所示装置可以验证非金属性的变化规律,实验室中药品有①
 溶液、②
溶液、② 、③浓盐酸、④
、③浓盐酸、④ 。已知:硫为淡黄色固体,难溶于水。
。已知:硫为淡黄色固体,难溶于水。
(3)用上述装置设计实验来验证氯的非金属性强于硫,装置A、B、C中所装药品分别为
(4)装置C中的实验现象为
您最近一年使用:0次
名校
解题方法
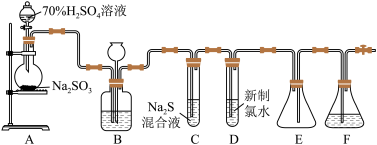
5 . 实验室可用如图装置(略去部分夹持仪器)制取SO2并验证其性质。____ 。
(2)装置B的作用之一是通过观察产生气泡的多少判断SO2生成的快慢,其中的液体最好选择______ (填代号)。
a.蒸馏水 b.饱和NaHCO3溶液 c.饱和NaHSO3溶液 d.饱和NaOH溶液
(3)C试管中的试剂可以验证二氧化硫的氧化性,现象为_______ 。
(4)为验证二氧化硫的还原性,充分反应后,取试管D中的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液中加入AgNO3溶液,有白色沉淀生成;
方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去;
方案Ⅲ:向第三份溶液中加入BaCl2溶液,产生白色沉淀。
上述方案中能达到实验目的的是方案____ (填“Ⅰ”“Ⅱ”或“Ⅲ”);试管D中发生反应的离子方程式为_____ 。
(5)装置E的作用是______ 。装置F中为_____ 溶液。
(2)装置B的作用之一是通过观察产生气泡的多少判断SO2生成的快慢,其中的液体最好选择
a.蒸馏水 b.饱和NaHCO3溶液 c.饱和NaHSO3溶液 d.饱和NaOH溶液
(3)C试管中的试剂可以验证二氧化硫的氧化性,现象为
(4)为验证二氧化硫的还原性,充分反应后,取试管D中的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液中加入AgNO3溶液,有白色沉淀生成;
方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去;
方案Ⅲ:向第三份溶液中加入BaCl2溶液,产生白色沉淀。
上述方案中能达到实验目的的是方案
(5)装置E的作用是
您最近一年使用:0次
2024-04-04更新
|
133次组卷
|
3卷引用:天津市静海区第一中学2023-2024学年高一下学期3月月考化学试题
名校
解题方法
6 . 较活泼金属与硝酸反应,产物复杂。如一定浓度的硝酸与镁反应,可同时得到 、
、 、
、 三种气体。某同学欲用下列仪器组装装置来直接验证有
三种气体。某同学欲用下列仪器组装装置来直接验证有 、
、 生成并制取氮化镁。(假设实验中每步转化均是完全的)
生成并制取氮化镁。(假设实验中每步转化均是完全的)
已知:① 沸点是21.1℃、熔点是
沸点是21.1℃、熔点是 ℃;
℃; 的沸点是
的沸点是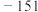 ℃、熔点是
℃、熔点是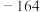 ℃;
℃;
②氮化镁遇水会发生水解。
回答下列问题:
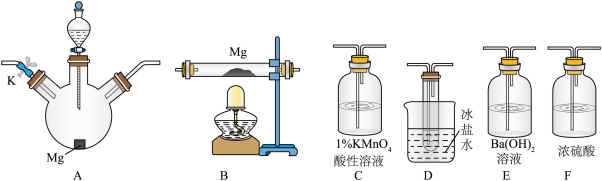
(1)为达到上述实验目的,所选用的仪器的正确连接方式是_________ (填序号)
a.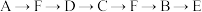 b.
b.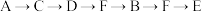
c.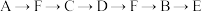 d.
d.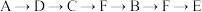
(2)实验中两次使用装置 ,第二次使用装置
,第二次使用装置 的作用是
的作用是_________ 。
(3)实验前需先打开开关 ,向装置内通
,向装置内通 气体,其目的是
气体,其目的是_________ ,当_________ 时停止通入 。
。
(4)实验过程中,发现在 中产生预期现象的同时,
中产生预期现象的同时, 中溶液颜色慢慢褪去,试写出
中溶液颜色慢慢褪去,试写出 中反应的离子方程式
中反应的离子方程式_________ 。
 、
、 、
、 三种气体。某同学欲用下列仪器组装装置来直接验证有
三种气体。某同学欲用下列仪器组装装置来直接验证有 、
、 生成并制取氮化镁。(假设实验中每步转化均是完全的)
生成并制取氮化镁。(假设实验中每步转化均是完全的)
已知:①
 沸点是21.1℃、熔点是
沸点是21.1℃、熔点是 ℃;
℃; 的沸点是
的沸点是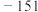 ℃、熔点是
℃、熔点是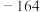 ℃;
℃;②氮化镁遇水会发生水解。
回答下列问题:
(1)为达到上述实验目的,所选用的仪器的正确连接方式是
a.
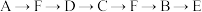 b.
b.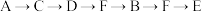
c.
 d.
d.
(2)实验中两次使用装置
 ,第二次使用装置
,第二次使用装置 的作用是
的作用是(3)实验前需先打开开关
 ,向装置内通
,向装置内通 气体,其目的是
气体,其目的是 。
。(4)实验过程中,发现在
 中产生预期现象的同时,
中产生预期现象的同时, 中溶液颜色慢慢褪去,试写出
中溶液颜色慢慢褪去,试写出 中反应的离子方程式
中反应的离子方程式
您最近一年使用:0次
7 . 甲同学通过查询资料知道,一定浓度的硝酸与镁反应时,可得到二氧化氮、一氧化氮、氮气三种气体。该同学用下列仪器组装装置来直接验证有二氧化氮,一氧化氮生成并制取氮化镁(假设实验中每步转化均是完全的)。
查阅文献得知:①二氧化氮沸点为21.1℃、熔点为-11℃,一氧化氮沸点为-151℃、熔点为-164℃;
②镁也能与二氧化碳反应;
③氮化镁遇水反应生成氢氧化镁和氨气。
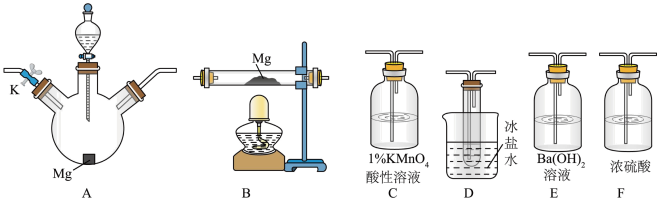
(1)实验中先打开开关K,通过导管向装置内通入二氧化碳气体以排出装置内的空气,停止通入二氧化碳的标志是___________ 。
(2)为实现上述实验目的,所选用的仪器的正确连接方式是A→___________ →E,确定还原产物中有二氧化氮的现象是___________ ,实验中要多次使用装置F,第二次使用F的目的是___________ 。
(3)实验过程中,发现在D中产生预期现象的同时,C中溶液颜色慢慢褪去,试写出C中反应的离子方程式:___________ 。
(4)甲同学在A中开始反应时,马上点燃B处的酒精灯,实验结束后通过测试发现B处的产品纯度不高,原因是___________ 。
(5)取少量氮化镁于试管中,加入足量稀硝酸,没有气体逸出。取少量反应后的溶液于试管中,加入足量NaOH浓溶液,加热,用镊子夹一块湿润的红色石蕊试纸接近试管口,试纸变蓝色。则氮化镁溶于足量稀硝酸中发生反应的化学方程式为___________ 。
查阅文献得知:①二氧化氮沸点为21.1℃、熔点为-11℃,一氧化氮沸点为-151℃、熔点为-164℃;
②镁也能与二氧化碳反应;
③氮化镁遇水反应生成氢氧化镁和氨气。

(1)实验中先打开开关K,通过导管向装置内通入二氧化碳气体以排出装置内的空气,停止通入二氧化碳的标志是
(2)为实现上述实验目的,所选用的仪器的正确连接方式是A→
(3)实验过程中,发现在D中产生预期现象的同时,C中溶液颜色慢慢褪去,试写出C中反应的离子方程式:
(4)甲同学在A中开始反应时,马上点燃B处的酒精灯,实验结束后通过测试发现B处的产品纯度不高,原因是
(5)取少量氮化镁于试管中,加入足量稀硝酸,没有气体逸出。取少量反应后的溶液于试管中,加入足量NaOH浓溶液,加热,用镊子夹一块湿润的红色石蕊试纸接近试管口,试纸变蓝色。则氮化镁溶于足量稀硝酸中发生反应的化学方程式为
您最近一年使用:0次
2023-04-16更新
|
391次组卷
|
2卷引用:湖北省孝感市重点高中教科研协作体2022-2023学年高一下学期4月期中考试化学试题
名校
8 . 下列装置或操作能达到相应实验目的的是
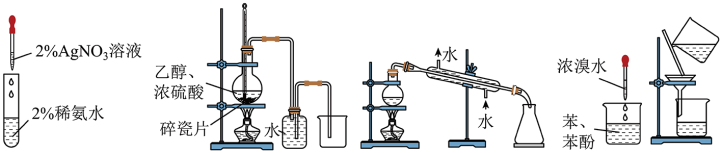
| A.配制银氨溶液 | B.实验室制备并收集乙烯 |
| C.分离乙醛和乙酸 | D.除去苯中的苯酚 |
您最近一年使用:0次
2021高三·全国·专题练习
解题方法
9 . 某兴趣小组在利用图所示装置做铜与稀硝酸反应的实验中,发现开始时气泡产生速率非常慢,一段时间后速率明显加快,烧瓶内溶液呈浅蓝色并不断加深,液面上方的气体颜色也在不断加深。该小组同学拟通过实验探究反应速率变化的原因。
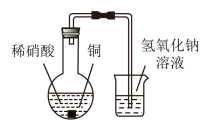
(1)图中铜与稀硝酸反应的离子方程式为___________ 。
(2)图中NaOH溶液能够吸收的有害气体是___________ 。
(3)小组同学提出了如下假设并设计实验探究:
I.甲同学认为反应速率变化的原因可能是反应放热导致溶液温度升高所致,故测定反应过程中溶液不同时间的温度,结果如下表:
结合实验目的和表中数据,你得出的结论是___________ 。
II.乙同学认为生成的Cu2+对反应有催化作用,为验证此假设,取A、B两支试管分别加入等量的铜片和稀硝酸,那么最好是在其中一支试管中加入少量的___________ (填序号)。
A.硝酸铜晶体 B.硝酸铜溶液 C.硫酸铜晶体 D.硫酸铜溶液
然后对比两支试管的反应,发现现象基本相同。故得出结论:Cu2+并不是反应的催化剂
III.丙同学根据现象推测反应过程中还有少量______ 生成,进而认为该物质对反应有催化作用,如图所示,丙同学从a处通入该物质后,发现左管中产生气泡速率明显快于右管。小组同学得出最后结论:这种物质对铜和稀硝酸的反应有催化作用。
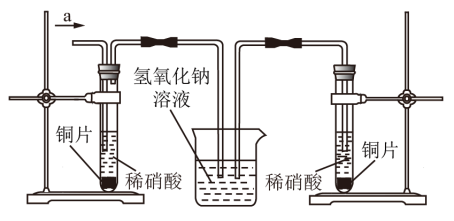
(4)实验结束后,发现试管中溶液呈绿色,而不显蓝色。部分同学认为是该溶液中Cu2+的浓度较高所致,另一部分同学认为是该溶液中溶解了通入的物质。丁同学设计了一个实验方案证明后者的推测更为合理。(在表格中写出该同学可能的实验操作和实验现象)

(1)图中铜与稀硝酸反应的离子方程式为
(2)图中NaOH溶液能够吸收的有害气体是
(3)小组同学提出了如下假设并设计实验探究:
I.甲同学认为反应速率变化的原因可能是反应放热导致溶液温度升高所致,故测定反应过程中溶液不同时间的温度,结果如下表:
| 时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 35 | 50 | 60 | 70 | 80 |
| 温度/℃ | 25 | 26 | 26 | 26 | 26 | 26 | 26.5 | 27 | 27 | 27 | 27 |
II.乙同学认为生成的Cu2+对反应有催化作用,为验证此假设,取A、B两支试管分别加入等量的铜片和稀硝酸,那么最好是在其中一支试管中加入少量的
A.硝酸铜晶体 B.硝酸铜溶液 C.硫酸铜晶体 D.硫酸铜溶液
然后对比两支试管的反应,发现现象基本相同。故得出结论:Cu2+并不是反应的催化剂
III.丙同学根据现象推测反应过程中还有少量

(4)实验结束后,发现试管中溶液呈绿色,而不显蓝色。部分同学认为是该溶液中Cu2+的浓度较高所致,另一部分同学认为是该溶液中溶解了通入的物质。丁同学设计了一个实验方案证明后者的推测更为合理。(在表格中写出该同学可能的实验操作和实验现象)
| 操作 | 现象 |
您最近一年使用:0次
10 . 下列实验方案中,操作正确且可以达到实验目的的是
| 序号 | 实验目的 | 实验操作和现象 |
| ① | 除去苯中混有的苯酚 | 向溶液中滴加少量浓溴水充分反应后过滤弃去沉淀 |
| ② | 检验CH3CH2Br中存在的溴元素 | 将CH3CH2Br与NaOH溶液共热,冷却后,取出上层水 溶液,加入AgNO3溶液,观察是否产生淡黄色沉淀 |
| ③ | 蔗糖未水解 | 向20%蔗糖溶液中加入少量稀H2SO4,加热;再加入银 氨溶液;未出现银镜 |
| ④ | 证明溴乙烷发生消去反应有乙烯生成 | 向试管中加入适量的溴乙烷和NaOH的乙醇溶液,加热, 将反应产生的气体通入溴水中,溴水褪色 |
| ⑤ | 检验绿茶中是否含有酚类物质 | 向茶水中滴加FeCl3溶液 |
| ⑥ | 实验室制备乙酸乙酯 | 向试管中依次加入浓硫酸、乙醇、乙酸和碎瓷片,加热 |
| A.②③④⑤ | B.④⑤ | C.①⑤⑥ | D.②④⑤ |
您最近一年使用:0次